Clear Sky Science · es
La metástasis linfática mediada por TGF-α/EGFR revela un objetivo terapéutico reposicionable en el cáncer de mama
Por qué este estudio importa para los pacientes
Cuando el cáncer de mama se expande más allá de la mama, a menudo aparece primero en los ganglios linfáticos. Los médicos saben que los tumores con niveles altos de una molécula llamada EGFR tienden a comportarse de forma agresiva, pero los fármacos que bloquean EGFR no han funcionado bien contra el cáncer de mama. Este estudio descubre una pieza faltante del rompecabezas: EGFR puede no impulsar principalmente el crecimiento tumoral, sino ayudar a las células tumorales a “navegar” hacia los vasos linfáticos y los ganglios. Ese cambio de perspectiva podría abrir la puerta a nuevas formas de detener la metástasis de forma temprana, antes de que se vuelva potencialmente mortal.
Una autopista oculta para las células tumorales
Los investigadores se centraron en el cáncer de mama triple negativo, un subtipo difícil de tratar que con frecuencia presenta niveles altos de EGFR e implicación temprana de los ganglios linfáticos. En un modelo de ratón, diseñaron células de cáncer de mama para sobreproducir EGFR e implantaron esas células en la glándula mamaria. Sorprendentemente, estos tumores ricos en EGFR no crecieron más rápido ni enviaron más metástasis a los pulmones que los tumores de control. En cambio, muchas más células cancerosas aparecieron en ganglios linfáticos cercanos, incluso en puntos temporales tempranos. La microscopía mostró que los vasos linfáticos se situaban mayormente en el borde externo del tumor, lo que sugiere que las células tumorales deben moverse activamente hacia afuera para encontrar y entrar en esos vasos. 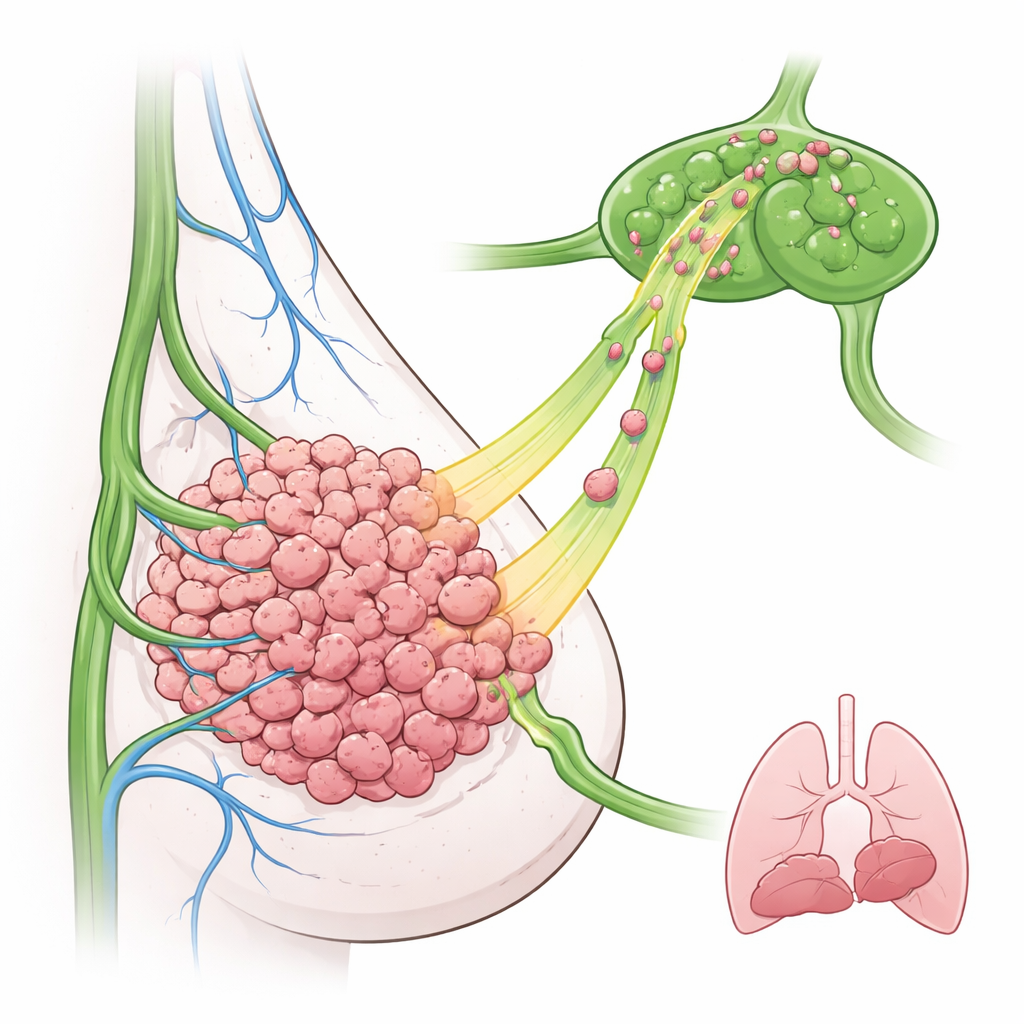
Señales procedentes de los propios vasos linfáticos
El equipo preguntó entonces si los vasos linfáticos son meros conductos pasivos o guías activas. Estudiaron las células endoteliales linfáticas, las células que recubren los vasos linfáticos, tanto en ratones como en tumores humanos de mama. Cuando estas células se expusieron a otra molécula relacionada con el tumor, TGF‑β, empezaron a producir factores de crecimiento que pueden activar EGFR. Un factor, TGF‑α, destacó: se incrementó con fuerza, se liberó al fluido circundante y en tejido tumoral se concentró en vasos linfáticos, no en vasos sanguíneos. Datos humanos mostraron que los cánceres de mama con niveles más altos de TGFA, especialmente el subtipo basal relacionado con la enfermedad triple negativa, se asociaban con peores resultados en los pacientes. Esto apuntó a TGF‑α como una probable “traza olfativa” que guía a las células tumorales EGFR‑positivas hacia los linfáticos.
Cómo las células tumorales siguen la traza
Para poner a prueba esta idea, los investigadores utilizaron ensayos de invasión y de migración celular en tiempo real. Colocaron células tumorales con sobreexpresión de EGFR sobre un gel y suministraron, por debajo, ya sea fluido procedente de células linfáticas o factores de crecimiento purificados. Las células ricas en EGFR invadieron con fuerza hacia el fluido de las células linfáticas y hacia TGF‑α sola, moviéndose de forma clara y dirigida en lugar de errar al azar. Otro factor, CTGF, más asociado a vasos sanguíneos, no promovió el movimiento direccional e incluso pudo atenuar el efecto de TGF‑α. Dentro de las células tumorales, TGF‑α activó una molécula de señalización llamada STAT3, junto con otras vías. Cuando STAT3 fue bloqueado químicamente, las células tumorales perdieron en gran medida su capacidad de moverse hacia señales linfáticas. La misma quimiotaxis dependiente de EGFR impulsada por TGF‑α se observó en una línea celular humana de cáncer de mama triple negativo, confirmando que este comportamiento no está limitado a ratones. 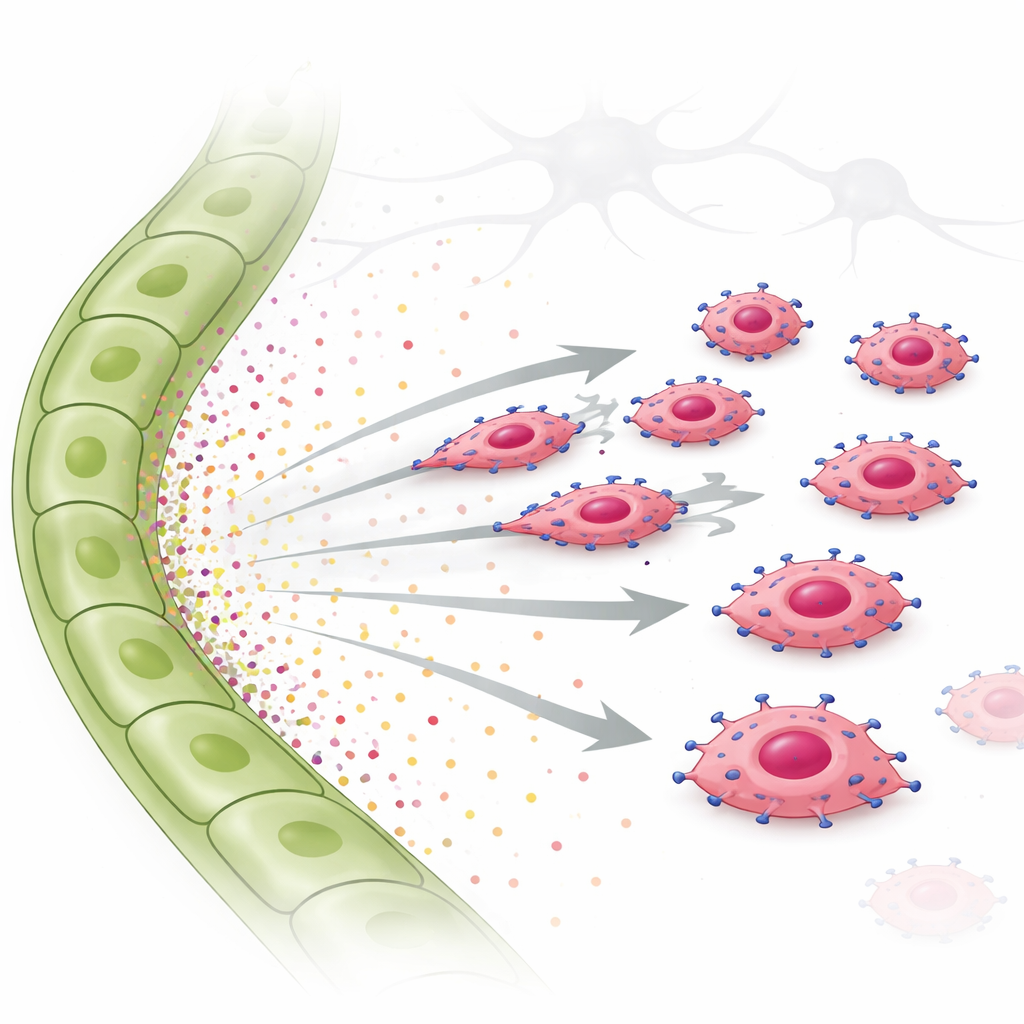
Reposicionando un anticuerpo existente
El estudio también exploró si se puede interrumpir este sistema de guía con un fármaco. Los autores usaron Fepixnebart, un anticuerpo de laboratorio desarrollado inicialmente para neutralizar TGF‑α y un factor relacionado en condiciones no cancerosas. En ensayos de invasión, este anticuerpo redujo de forma marcada la capacidad de las células EGFR‑positivas para moverse hacia el fluido derivado de linfáticos. En ratones, una única dosis administrada al implantar las células tumorales disminuyó significativamente el número de células cancerosas encontradas posteriormente en ganglios linfáticos cercanos, sin afectar el tamaño del tumor primario. Al mismo tiempo, los tumores con alto EGFR se asociaron con ganglios linfáticos que drenaban el tumor que contenían más células totales pero una escasez relativa de células T CD8 “asesinas” y un aumento de células T reguladoras, lo que sugiere un cambio hacia un microambiente inmune más supresor donde el cáncer puede establecerse con mayor facilidad.
Qué significa esto para tratamientos futuros
En conjunto, el trabajo replantea el papel de EGFR en el cáncer de mama triple negativo: en lugar de ser simplemente un acelerador del crecimiento, EGFR ayuda a las células tumorales a detectar y seguir una señal de TGF‑α emitida por vasos linfáticos, orientándolas hacia los ganglios linfáticos y acompañada de un cambio inmune que puede favorecer la metástasis. Dado que Fepixnebart y otros agentes dirigidos a EGFR ya existen y se han probado en humanos por seguridad, esta vía representa un objetivo terapéutico “reposicionable”. En lugar de esperar que estos fármacos reduzcan tumores establecidos por sí solos, los clínicos podrían en el futuro usarlos para bloquear la diseminación linfática temprana y mejorar la efectividad de terapias basadas en el sistema inmune, cambiando potencialmente la forma en que se manejan los cánceres de mama de alto riesgo.
Cita: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Palabras clave: cáncer de mama triple negativo, metástasis linfática, señalización EGFR, TGF-alpha, microambiente inmune tumoral