Clear Sky Science · tr
TGF-α/EGFR aracılı lenfatik metastaz, meme kanserinde yeniden konumlandırılabilir bir terapötik hedef ortaya koyuyor
Bu çalışma hastalar için neden önemli
Meme kanseri memeden yayıldığında, genellikle ilk olarak lenf düğümlerinde görünür. Doktorlar, EGFR adlı molekülün yüksek düzeyde bulunduğu tümörlerin genellikle agresif davrandığını biliyor, ancak EGFR’yi kapatan ilaçlar meme kanserinde iyi sonuç vermedi. Bu çalışma, eksik bir parçayı ortaya çıkarıyor: EGFR’nin esas olarak tümör büyümesini sürdürmekten ziyade, tümör hücrelerinin lenfatik damarlara ve lenf düğümlerine “yönelmelerine” yardımcı olabileceği anlaşılıyor. Bu bakış açısındaki değişim, metastazı yaşamı tehdit etmeden önce erken durdurmanın yeni yollarını açabilir.
Tümör hücreleri için gizli bir otoyol
Araştırmacılar, genellikle yüksek EGFR düzeyleri ve erken lenf nodu tutulumu görülen tedavisi zor bir alt tip olan üçlü negatif meme kanserine odaklandı. Bir fare modelinde, meme kanseri hücrelerini aşırı EGFR üretecek şekilde değiştirdiler ve memenin içerisine yerleştirdiler. İlginç bir şekilde, bu EGFR zengin tümörler daha hızlı büyümedi ve akciğere daha fazla metastaz göndermedi. Bunun yerine, çok daha fazla kanser hücresi yakın lenf düğümlerinde, hatta erken zaman noktalarında görüldü. Mikroskopik inceleme, lenfatik damarların çoğunlukla tümörün dış çeperi etrafında bulunduğunu gösterdi; bu da tümör hücrelerinin bu damarlara ulaşmak ve girmek için aktif olarak dışa doğru hareket etmesi gerektiğini düşündürdü. 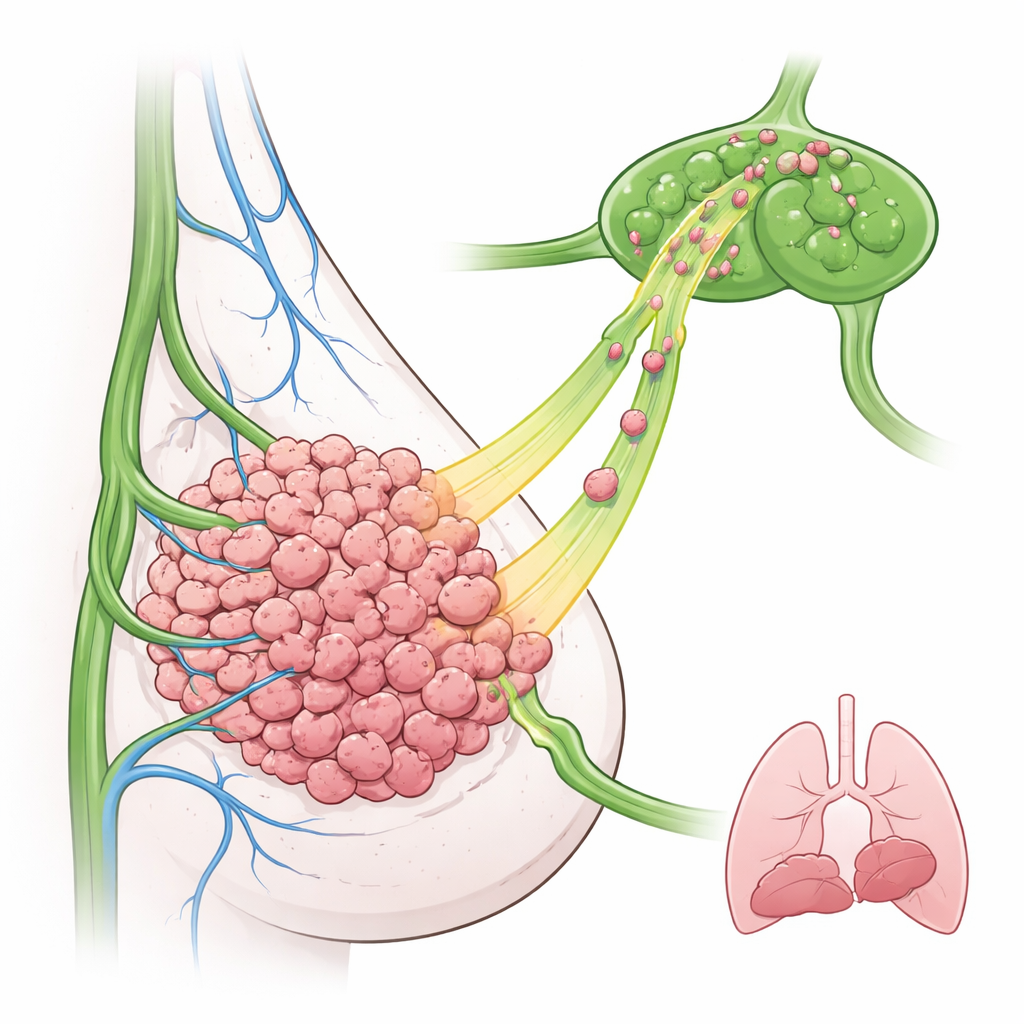
Lenf damarlarının kendisinden gelen sinyaller
Araştırma ekibi, lenfatik damarların yalnızca pasif borular mı yoksa aktif rehberler mi olduğunu sordu. Hem farelerde hem de insan meme tümörlerinde lenfatik damarı döşeyen hücreler olan lenfatik endotel hücrelerini incelediler. Bu hücreler başka bir tümörle ilişkili molekül olan TGF-β’ye maruz kaldığında, EGFR’yi aktive edebilecek büyüme faktörleri üretmeye başladı. Bir faktör olarak TGF-α öne çıktı: güçlü biçimde artmış, çevre sıvısına salınmış ve tümör dokusunda kan damarları değil lenfatik damarlar üzerinde yoğunlaşmıştı. İnsan verileri, özellikle üçlü negatif hastalıkla ilişkili bazal-benzeri alt tipte, daha yüksek TGFA düzeyine sahip meme kanserlerinin daha kötü hasta sonuçlarıyla ilişkili olduğunu gösterdi. Bu durum, TGF-α’yı EGFR-pozitif tümör hücrelerini lenfatiklere yönlendiren muhtemel bir “koku izi” olarak işaretledi.
Tümör hücreleri iz izini nasıl takip ediyor
Bu fikri test etmek için araştırmacılar invazyon ve canlı hücre göçü deneyleri kullandılar. EGFR fazladan üreten tümör hücrelerini bir jelin üzerine yerleştirdiler ve alt tarafta ya lenfatik hücre sıvısı ya da saflaştırılmış büyüme faktörleri sağladılar. EGFR zengin hücreler, lenfatik hücre sıvısına ve yalnızca TGF-α’ya doğru güçlü bir şekilde ilerledi; rastgele dolaşmak yerine açık, yönlendirilmiş bir hareket sergilediler. Kan damarlarıyla daha çok ilişkili olan CTGF adlı başka bir faktör ise yönlendirilmiş hareketi teşvik etmedi ve hatta TGF-α’nın etkisini azaltabiliyordu. Tümör hücrelerinin içinde TGF-α, STAT3 adlı bir sinyal molekülünü ve diğer yolakları etkinleştirdi. STAT3 kimyasal olarak bloke edildiğinde, tümör hücreleri büyük ölçüde lenfatik sinyallere doğru hareket etme yeteneklerini kaybetti. Aynı TGF-α kaynaklı, EGFR bağımlı kemotaksis insan üçlü negatif meme kanseri hücre hattında da gözlemlendi; bu bulgu bu davranışın farelerle sınırlı olmadığını doğruladı. 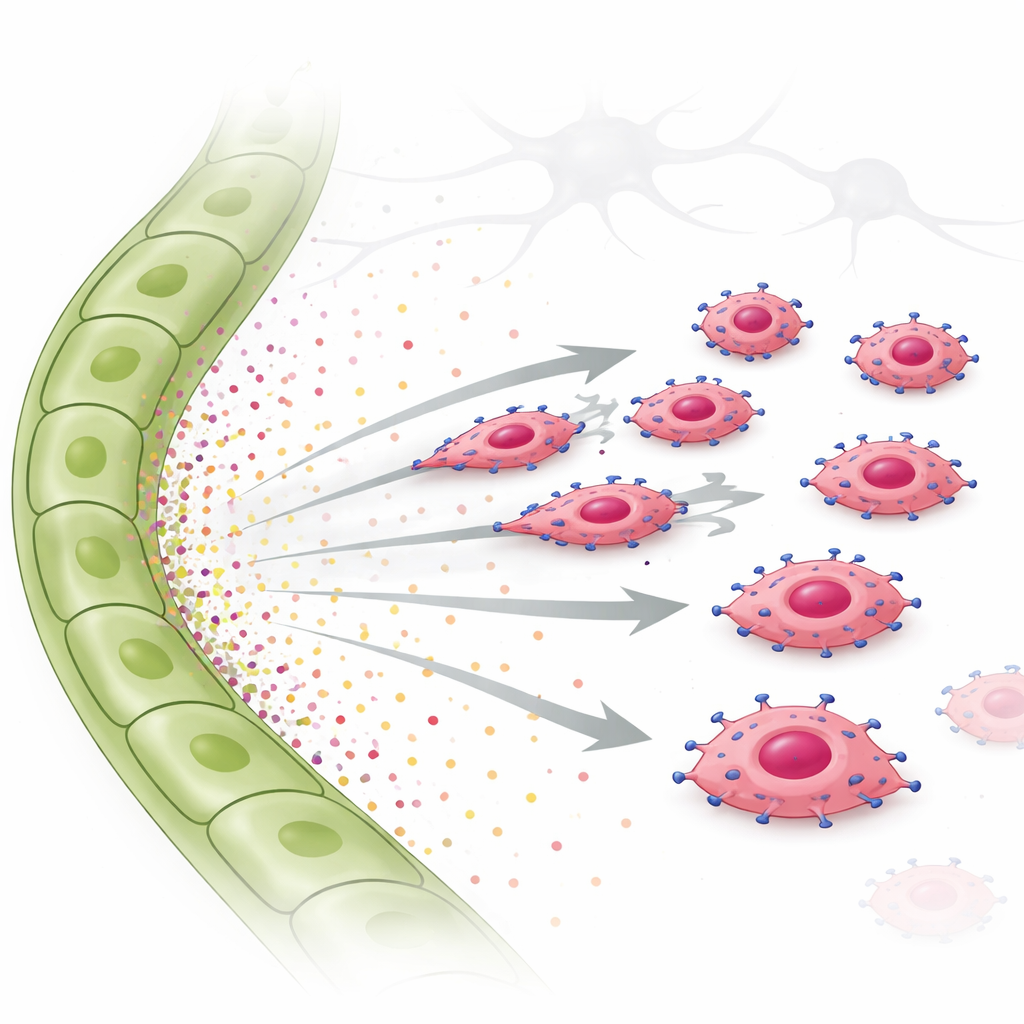
Mevcut bir antikoru yeniden kullanmak
Çalışma ayrıca bu rehberlik sisteminin bir ilaçla kesilip kesilemeyeceğini araştırdı. Yazarlar, başlangıçta kanser dışı durumlarda TGF-α ve ilişkili bir faktörü nötralize etmek için geliştirilen laboratuvar antikoru Fepixnebart’ı kullandılar. İnvazyon deneylerinde bu antikor, EGFR-pozitif hücrelerin lenfatik kaynaklı sıvıya doğru hareket etme yeteneğini keskin bir şekilde azalttı. Farelerde, tümör hücreleri implante edildiğinde tek bir doz verilmesi, ileri bir zaman noktasında yakın lenf düğümlerinde bulunan kanser hücresi sayısını önemli ölçüde düşürdü; bu durum primer tümörün boyutunu etkilemedi. Aynı zamanda, yüksek EGFR’ye sahip tümörler, tümörleri drene eden lenf düğümlerinde toplam hücre sayısının artması ancak CD8 “katil” T hücrelerinin görece azalması ve düzenleyici T hücrelerinin artması ile ilişkiliydi; bu da kanserin daha kolay yerleşebileceği daha baskılayıcı bir immün ortama doğru bir kaymayı düşündürüyor.
Gelecek tedavi için anlamı
Bir arada ele alındığında, bu çalışma üçlü negatif meme kanserinde EGFR’nin konumunu yeniden tanımlıyor: EGFR yalnızca bir büyüme hızlandırıcısı olmak yerine, lenfatik damarlar tarafından yayılan TGF-α sinyalini algılayıp takip ederek tümör hücrelerini lenf düğümlerine yönlendiriyor ve metastazı kolaylaştırabilecek bir immün değişimle birlikte oluyor. Fepixnebart ve diğer EGFR hedefli ajanlar zaten mevcut ve insanlarda güvenlikleri test edildiği için bu yolak “yeniden konumlandırılabilir” bir terapötik hedef sunuyor. Bu ilaçlardan, yerleşik tümörleri tek başına küçültmeleri beklenmek yerine, klinisyenler bir gün erken lenfatik yayılmayı engellemek ve immün temelli terapilerin etkinliğini artırmak için faydalanabilir; bu da yüksek riskli meme kanserlerinin yönetimini değiştirme potansiyeline sahip olabilir.
Atıf: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Anahtar kelimeler: üçlü negatif meme kanseri, lenfatik metastaz, EGFR sinyalizasyonu, TGF-alpha, tümör immün mikroçevresi