Clear Sky Science · fr
Métastase lymphatique médiée par TGF-α/EGFR révèle une cible thérapeutique repositionnable dans le cancer du sein
Pourquoi cette étude est importante pour les patients
Lorsque le cancer du sein se propage au-delà du sein, il apparaît souvent d’abord dans les ganglions lymphatiques. Les médecins savent que les tumeurs présentant des niveaux élevés d’une molécule appelée EGFR ont tendance à être agressives, mais les médicaments qui inhibent EGFR n’ont pas donné de bons résultats contre le cancer du sein. Cette étude révèle un élément manquant du puzzle : EGFR ne stimulerait pas principalement la croissance tumorale, mais aiderait plutôt les cellules cancéreuses à « s’orienter » vers les vaisseaux lymphatiques et les ganglions. Ce changement de perspective pourrait ouvrir la voie à de nouvelles façons d’empêcher la métastase tôt, avant qu’elle ne devienne mortelle.
Une autoroute cachée pour les cellules tumorales
Les chercheurs se sont concentrés sur le cancer du sein triple négatif, un sous-type difficile à traiter qui présente souvent des niveaux élevés d’EGFR et une atteinte précoce des ganglions. Dans un modèle murin, ils ont modifié des cellules de cancer du sein pour surexprimer EGFR et les ont implantées dans la glande mammaire. Étonnamment, ces tumeurs riches en EGFR ne croissaient pas plus vite et n’envoyaient pas plus de métastases aux poumons que les tumeurs témoins. En revanche, beaucoup plus de cellules cancéreuses apparaissaient dans les ganglions lymphatiques voisins, même à des temps précoces. La microscopie montrait que les vaisseaux lymphatiques se situaient principalement autour de la périphérie de la tumeur, ce qui suggère que les cellules tumorales doivent se déplacer activement vers l’extérieur pour trouver et pénétrer ces vaisseaux. 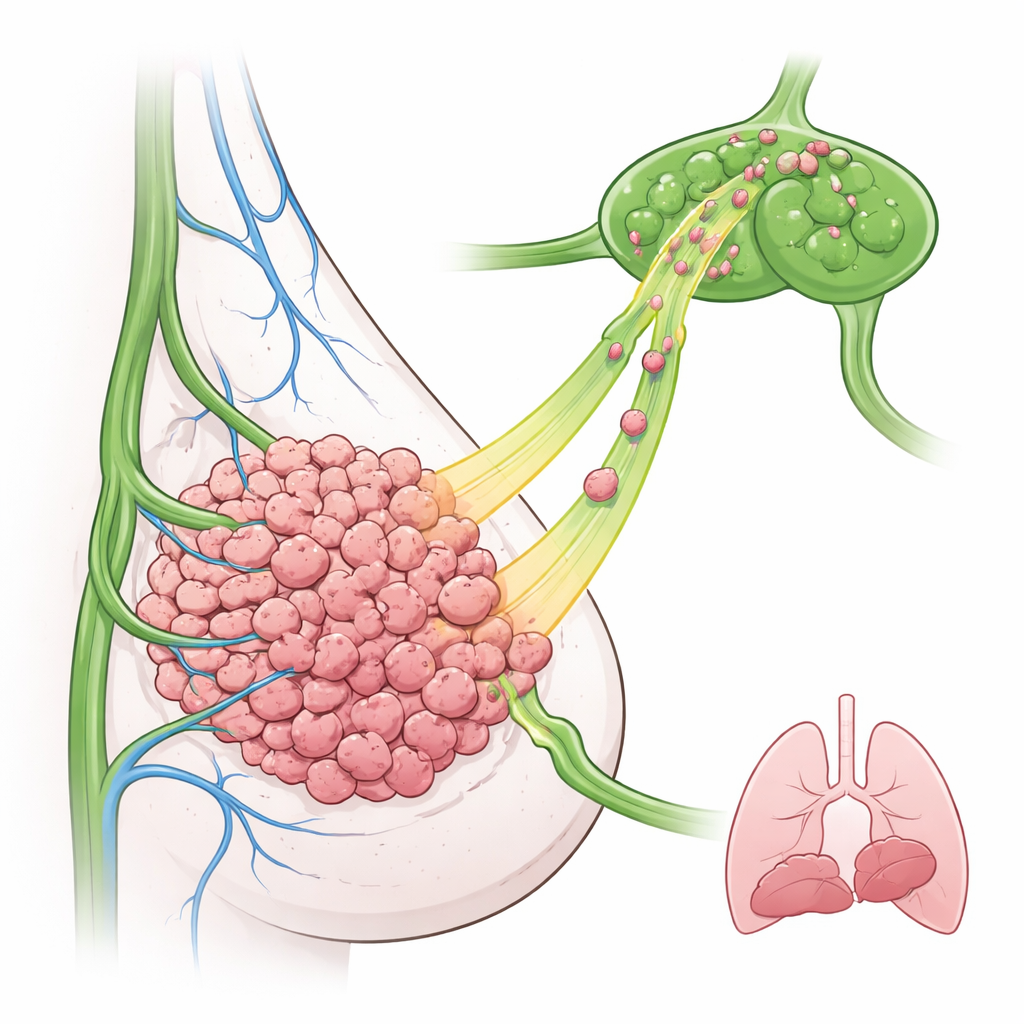
Des signaux provenant des vaisseaux lymphatiques eux‑mêmes
L’équipe s’est ensuite interrogée pour savoir si les vaisseaux lymphatiques sont de simples conduits passifs ou des guides actifs. Ils ont étudié les cellules endothéliales lymphatiques, qui tapissent les vaisseaux lymphatiques, chez la souris et dans des tumeurs mammaires humaines. Lorsque ces cellules étaient exposées à une autre molécule liée à la tumeur, le TGF‑β, elles commençaient à produire des facteurs de croissance capables d’activer EGFR. Un facteur, le TGF‑α, est apparu comme particulièrement important : il était fortement augmenté, libéré dans le fluide environnant et, dans le tissu tumoral, concentré sur les vaisseaux lymphatiques plutôt que sur les vaisseaux sanguins. Les données humaines montraient que les cancers du sein ayant des niveaux plus élevés de TGFA, en particulier le sous‑type basaloïde lié à la maladie triple négative, étaient associés à de moins bons résultats pour les patientes. Cela désignait le TGF‑α comme une « piste olfactive » probable conduisant les cellules tumorales EGFR‑positives vers les lymphatiques.
Comment les cellules tumorales suivent la piste
Pour tester cette idée, les chercheurs ont utilisé des essais d’invasion et de migration de cellules vivantes. Ils ont placé des cellules tumorales surexprimant EGFR au‑dessus d’un gel et ont fourni soit du fluide de cellules lymphatiques soit des facteurs de croissance purifiés en dessous. Les cellules riches en EGFR envahissaient fortement en direction du fluide de cellules lymphatiques et vers le TGF‑α seul, se déplaçant de façon claire et dirigée plutôt qu’en errance aléatoire. Un autre facteur, CTGF, davantage associé aux vaisseaux sanguins, ne favorisait pas un mouvement directionnel et pouvait même atténuer l’effet du TGF‑α. À l’intérieur des cellules tumorales, le TGF‑α activait une molécule de signalisation appelée STAT3, ainsi que d’autres voies. Lorsque STAT3 était bloqué chimiquement, les cellules tumorales perdaient en grande partie leur capacité à se déplacer vers les signaux lymphatiques. La même chimio‑taxis dépendante d’EGFR et induite par le TGF‑α a été observée dans une lignée humaine de cancer du sein triple négatif, confirmant que ce comportement n’est pas limité à la souris. 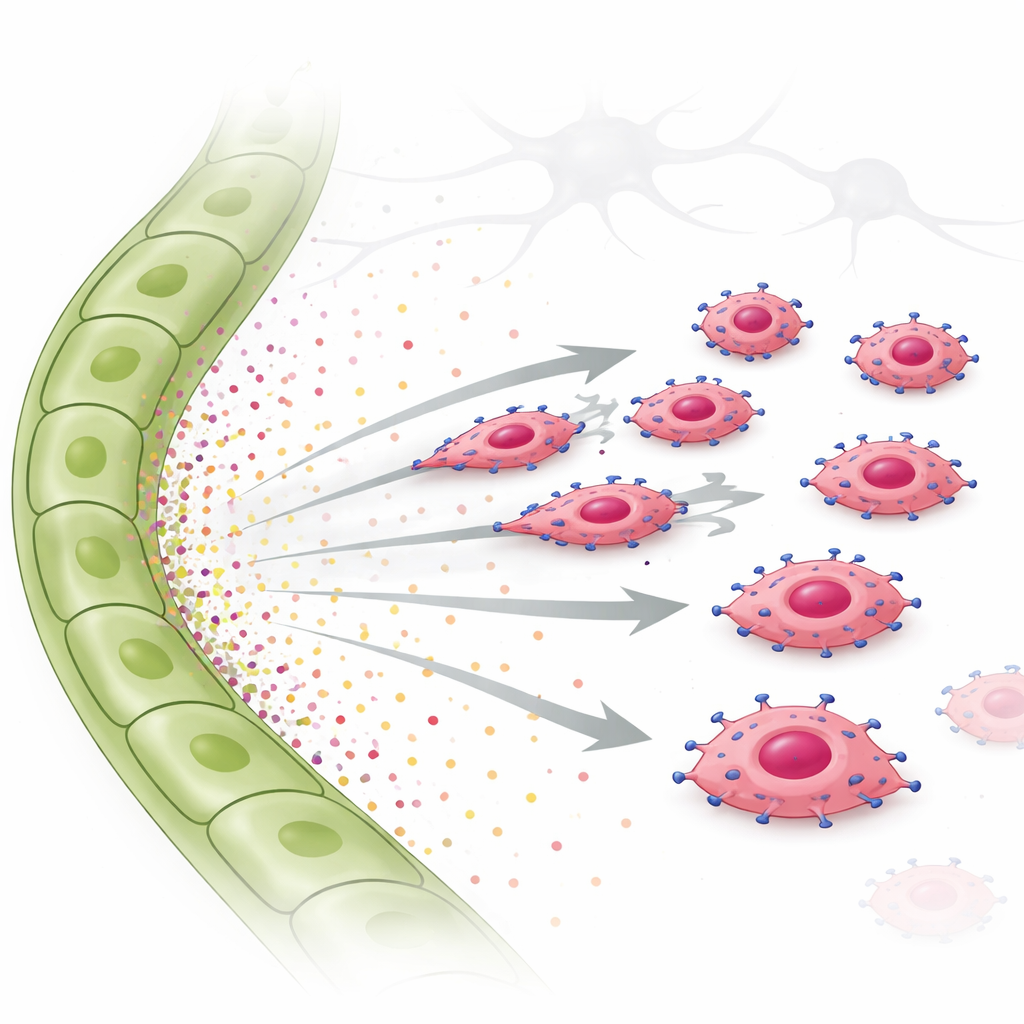
Repositionner un anticorps existant
L’étude a également exploré si ce système de guidage peut être interrompu par un médicament. Les auteurs ont utilisé Fepixnebart, un anticorps de laboratoire initialement développé pour neutraliser le TGF‑α et un facteur apparenté dans des pathologies non cancéreuses. Dans les essais d’invasion, cet anticorps a fortement réduit la capacité des cellules EGFR‑positives à se diriger vers le fluide dérivé des cellules lymphatiques. Chez la souris, une dose unique administrée au moment de l’implantation des cellules tumorales a significativement diminué le nombre de cellules cancéreuses retrouvées ultérieurement dans les ganglions lymphatiques voisins, sans affecter la taille de la tumeur primaire. Parallèlement, les tumeurs à haute expression d’EGFR étaient associées à des ganglions lymphatiques drainant la tumeur contenant plus de cellules totales mais une relative pénurie de cellules CD8 « tueuses » et une augmentation des cellules T régulatrices, suggérant un basculement vers un environnement immunitaire plus suppressif où le cancer peut s’implanter plus facilement.
Que cela signifie pour les traitements futurs
Dans l’ensemble, ce travail requalifie le rôle d’EGFR dans le cancer du sein triple négatif : au lieu d’être uniquement un accélérateur de croissance, EGFR aide les cellules tumorales à percevoir et suivre un signal de TGF‑α émis par les vaisseaux lymphatiques, les orientant vers les ganglions lymphatiques et s’accompagnant d’un basculement immunitaire favorable à la métastase. Parce que Fepixnebart et d’autres agents ciblant EGFR existent déjà et ont été évalués pour leur sécurité chez l’humain, cette voie représente une cible thérapeutique « repositionnable ». Plutôt que d’attendre que ces médicaments réduisent seuls des tumeurs établies, les cliniciens pourraient un jour les utiliser pour bloquer la diffusion lymphatique précoce et améliorer l’efficacité des thérapies immunitaires, changeant potentiellement la prise en charge des cancers du sein à haut risque.
Citation: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Mots-clés: cancer du sein triple négatif, métastase lymphatique, signalisation EGFR, TGF-alpha, microenvironnement immunitaire tumoral