Clear Sky Science · zh
由分子伴护蛋白组织者 HOP1 解除抑制蛋白磷酸酶 5 从而激活植物 NLR 免疫
植物如何在生长与自我防御之间抉择
植物不断面临潜在侵袭者——细菌、真菌和病毒——但不能为了对抗每一个威胁就放弃生长。本文揭示了模式植物拟南芥中一个微小的分子“刹车与触发”系统,如何决定何时释放一种极端的免疫反应:这种反应可以拯救植物,但也会抑制其生长。理解这个开关有助于指导作物在不付出过高产量代价的情况下,培育或改造为抗病品种。
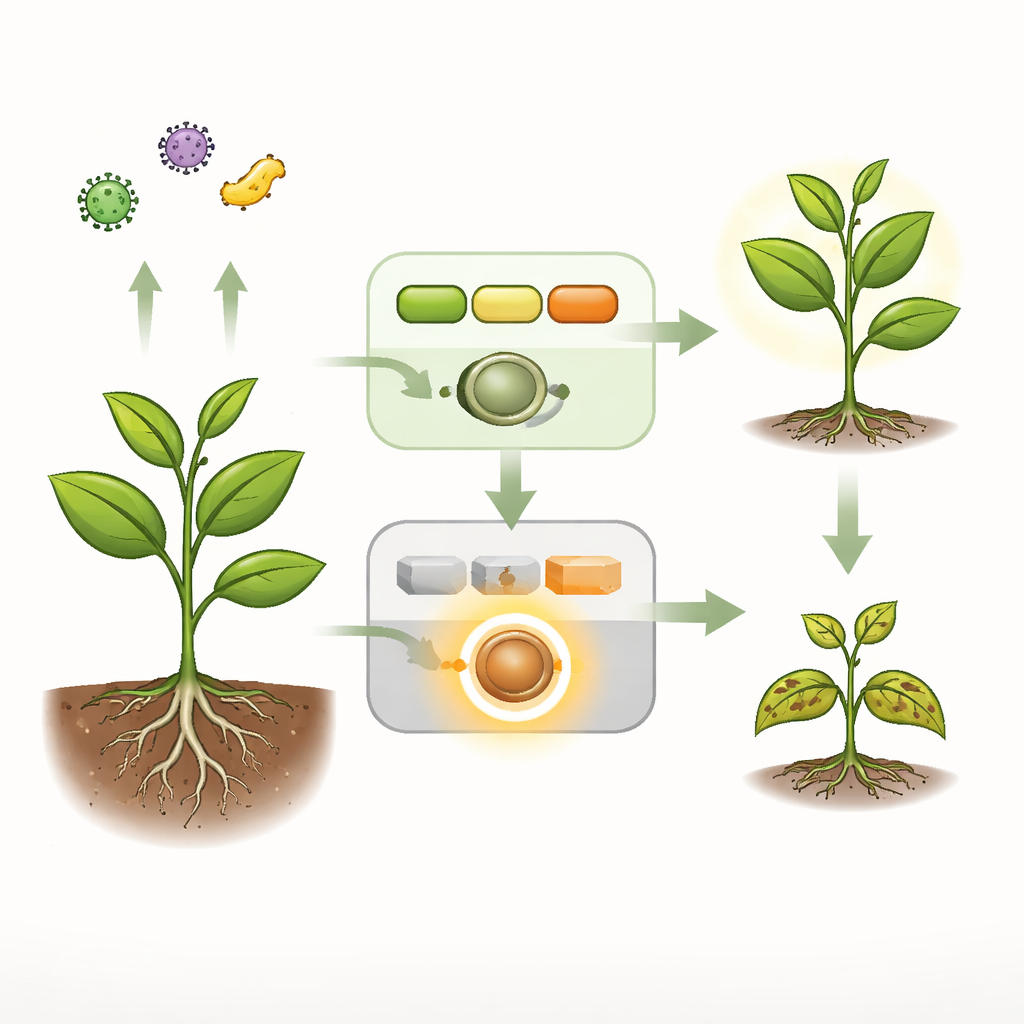
日常警报与紧急警笛
植物运行两套主要安保系统。第一套是快速且广泛的警报,在细胞表面识别一般微生物特征并启动防御反应。第二层更为激烈,依赖内部哨兵——称为 NLR 的受体,它们在检测到病原体的细胞中可触发强烈且常致死的防御反应。在健康的拟南芥中,一条由三种酶组成的信号链——统称为 MEKK1–MKK1/2–MPK4 级联——既传递第一道警报,又悄然抑制一个特定的 NLR 受体 SUMM2,使其不在无原因时触发。当该级联被突变或细菌效应蛋白破坏时,植物会出现自发细胞死亡、防御基因高表达和严重矮化等失控免疫的迹象。
一株隐藏的酶被唤醒
作者发现,一种名为 LET7 的磷酸酶——植物中的 PP5 同源物——位于这场失控反应的核心。LET7 本身结构像一把折叠的小刀:一段 TPR 结构域回折覆盖催化区,使其大体处于关闭状态。遗传筛选显示,缺失 LET7 的植物在上游信号链被抑制时不再出现致命症状,表明 LET7 位于该级联下游。生化实验证明,当 LET7 的催化区被释放或通过特定突变变得过度活跃时,植物会出现强烈的防御反应和细胞死亡;而催化失活的版本则无法诱导这些效应。因此,LET7 的磷酸酶活性既是驱动自身免疫所必需的,也是充分的。
一个分子组织者释放刹车
这把分子“折刀”如何打开?研究团队鉴定出一个名为 HOP1 的共分子伴护蛋白,作为关键的组织者。HOP1 通常协助热休克蛋白折叠并稳定其他蛋白。在此情形下,它结合 LET7 的 TPR 区,竞争性地取代了使 LET7 处于关闭状态的内部接触。结构建模与两者的精确氨基酸互换实验表明,这一结合界面经过精细调节:减弱 HOP1 与 LET7 的相互作用会降低 LET7 的活化。当 MEKK1–MKK1/2–MPK4 级联完整时,HOP1 与 LET7 的结合较少,LET7 保持受抑;当该级联被破坏——无论是由突变、另一支架蛋白过量,还是细菌效应子——HOP1–LET7 相互作用加强,释放 LET7 的催化活性。值得注意的是,人类的 HOP1 与 PP5 同源物能够替代植物这对蛋白,提示该激活机制在不同生物界间具有保守性。
切断关键开关并守护传感器
一旦被激活,LET7 的靶点是一个名为 CRCK3 的激酶,此酶此前已与同一路径相关。CRCK3 存在磷酸化和去磷酸化两种形式,在蛋白凝胶上可分为两条带。在植物细胞和体外试验中,活性 LET7 选择性地去除 CRCK3 的磷酸标记,而非活性 LET7 则不能。增强 LET7 活性或与 CRCK3 共表达会促进去磷酸化并导致细胞死亡和典型免疫标志,但在缺失 HOP1 或 NLR 受体 SUMM2 的情况下,这些效应被削弱。与此同时,作者发现 LET7 与 HOP1 均通过其 TPR 区与 SUMM2 发生物理结合,并增加 SUMM2 的蛋白丰度,而并非广泛稳定其他 NLR 受体。因此,同一模块既去除 CRCK3 的磷酸标记,也有助于维持读取该信号的传感器。
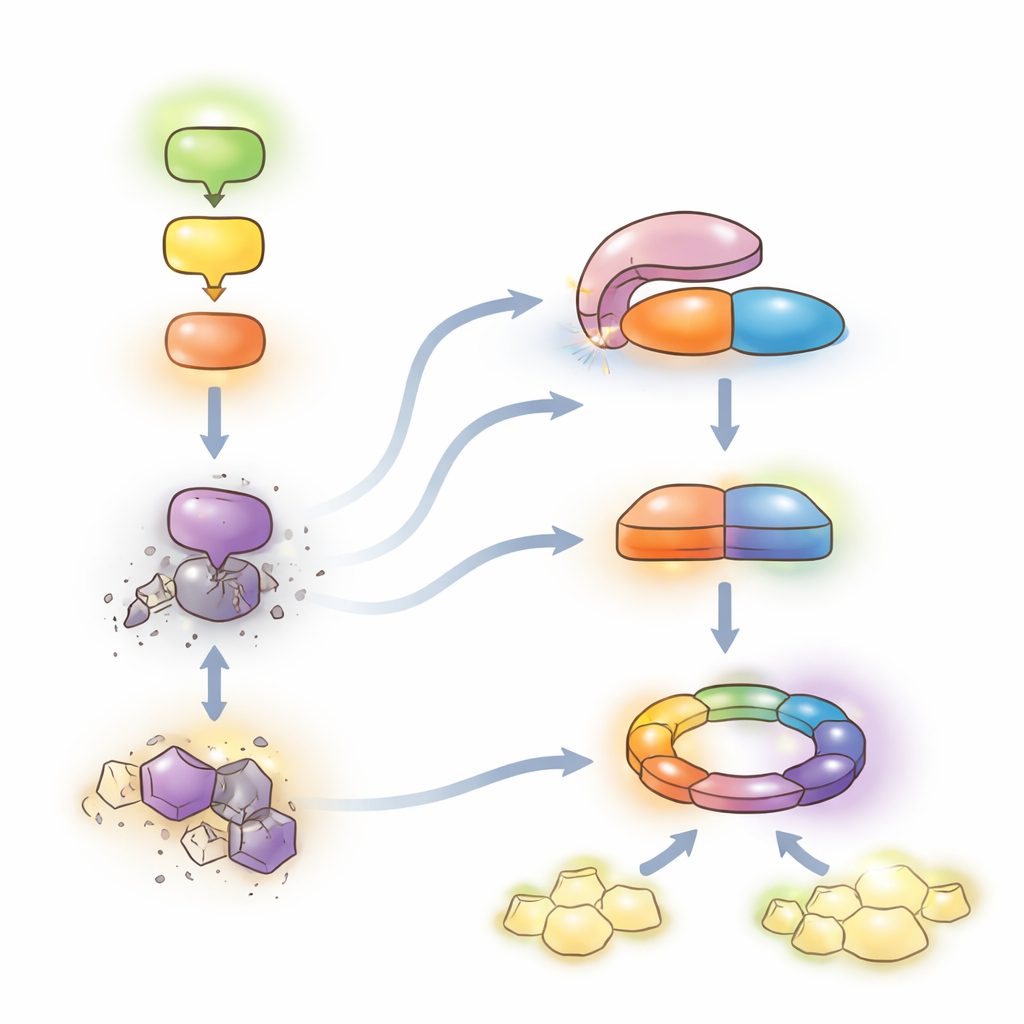
保护与生长之间的微妙平衡
总体上,这些发现支持这样一个模型:MEKK1–MKK1/2–MPK4 级联抑制第二道强有力的防线。当该级联完整时,LET7 保持自抑,SUMM2 水平被控制,从而使植物主要依赖日常的警报系统并继续生长。当病原体破坏该级联时,HOP1 与 LET7 结合,解锁其磷酸酶活性。随后 LET7 去磷酸化 CRCK3,并与 HOP1 一道稳定 SUMM2,将系统推向由 NLR 介导的全面免疫和局部细胞死亡——这种反应防护性强但代价高昂。通过揭示 PP5 酶类的这一保守“解除抑制”机制,这项工作勾画出一个分子杠杆,理论上可以在作物中调整以增强抗病性,同时尽量减少有害的自身免疫反应。
引用: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
关键词: 植物免疫, 蛋白磷酸酶5, NLR 受体, 信号传导, 拟南芥