Clear Sky Science · sv
Avlastning av proteinfosfatas 5 från repression av chaperon‑organisatören HOP1 aktiverar växtens NLR‑immunitet
Hur växter väljer mellan tillväxt och självförsvar
Växter möter ständigt potentiella angripare — bakterier, svampar och virus — men kan inte enkelt överge tillväxt för att bekämpa varje hot. Denna artikel avslöjar hur ett litet molekylärt ”broms‑och‑utlösar” system i modellväxten Arabidopsis hjälper till att avgöra när en extrem immunreaktion ska släppas lös; en reaktion som kan rädda växten men också hämma dess tillväxt. Att förstå denna växel ger insikt i hur grödor kan avlas eller konstrueras för att vara sjukdomsresistenta utan att betala för hög avkastningskostnad.
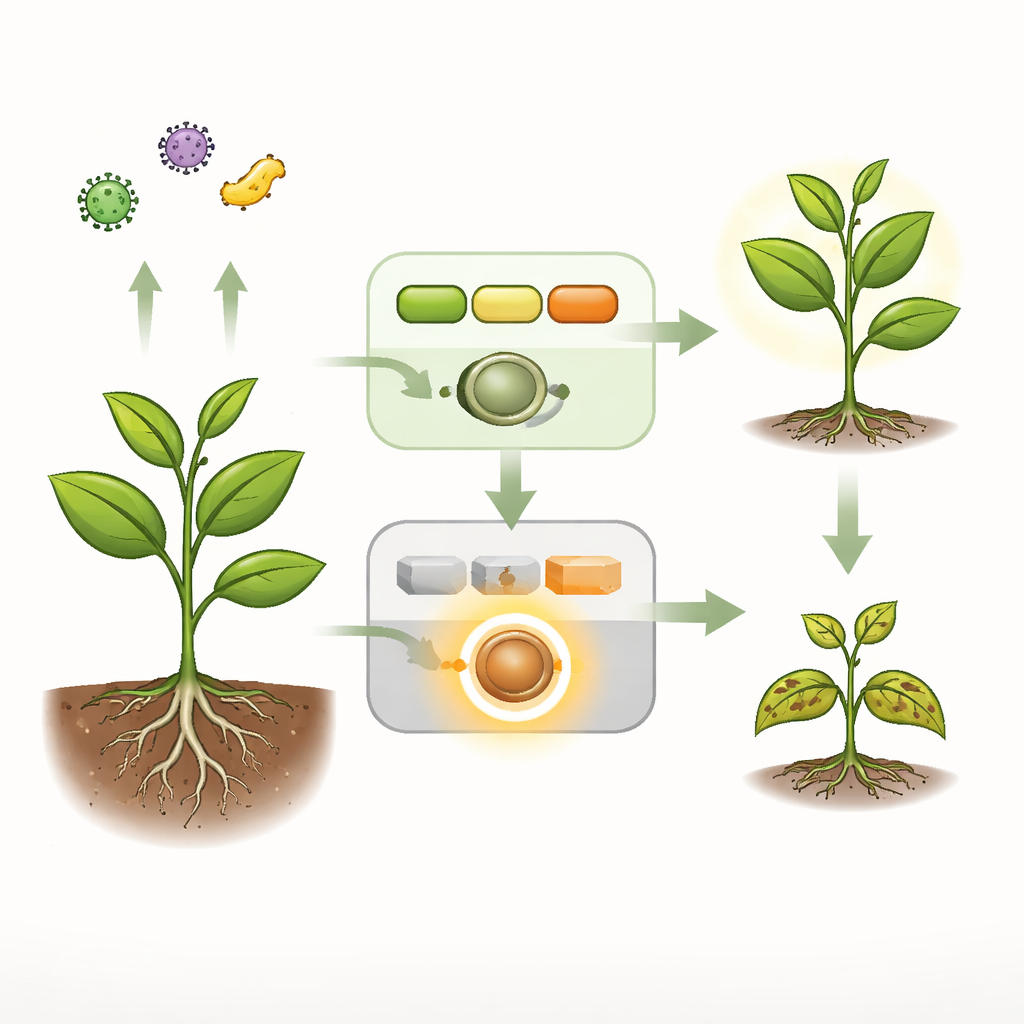
Vardagliga larm kontra nödsirener
Växter driver två huvudsakliga säkerhetssystem. Det första är ett snabbt, brett larm som upptäcker allmänna mikrobiella fingeravtryck vid cellytan och aktiverar skyddssvar. Ett andra, mer drastiskt lager förlitar sig på interna väktare kallade NLR‑receptorer som kan utlösa kraftfullt, ofta dödligt, försvar i celler där patogener upptäcks. I friska Arabidopsis förmedlar en signalserie av tre enzymer — kollektivt kallad MEKK1–MKK1/2–MPK4‑kaskaden — både det första larmet och håller i det tysta en särskild NLR‑receptor, SUMM2, från att aktiveras utan anledning. När denna kaskad bryts genom mutation eller genom ett bakteriellt effektorprotein visar växterna spontana celldödsfenomen, hög försvarsgensaktivitet och svår dvärgväxtlighet — alla tecken på okontrollerad immunitet.
En dold enzym väcks
Författarna upptäckte att ett fosfatasenzym kallat LET7, en växtversion av det konservade proteinet PP5, står i centrum för denna okontrollerade respons. På egen hand är LET7 uppbyggt som en hopfälld fällkniv: en region (en TPR‑domän) böjer sig tillbaka över den katalytiska regionen och håller den i stort sett avstängd. Genetiska screens visade att växter som saknar LET7 inte längre led av de dödliga symtomen som uppstår när den uppströms signalvägen tystas, vilket placerar LET7 nedströms om den kaskaden. Biokemiska tester visade att när LET7:s katalytiska region frigörs eller görs hyperaktiv genom specifika mutationer, utvecklar växterna starka försvarssvar och celldöd, medan en katalytiskt död version inte kan utlösa dessa effekter. Således är LET7:s fosfatasaktivitet både nödvändig och tillräcklig för att driva autoimmunitet.
En molekylär organisatör släpper bromsen
Hur öppnas den molekylära fällkniven? Forskargruppen identifierade ett co‑chaperonprotein kallat HOP1 som en nyckelorganisatör. HOP1 hjälper normalt värmestressproteiner att vika och stabilisera andra proteiner. Här fäster det på TPR‑regionen av LET7 och konkurrerar ut den interna kontakten som håller LET7 stängd. Strukturell modellering och precisa aminosyrabyten i båda parterna visade att denna bindningsyta är finjusterad: en försvagning av kontakten mellan HOP1 och LET7 minskar LET7‑aktiveringen. När MEKK1–MKK1/2–MPK4‑kaskaden är intakt är associationen mellan HOP1 och LET7 låg och LET7 förblir repressed. När kaskaden störs — genom mutationer, genom ett överskott av ett annat scaffold‑protein eller genom ett bakteriellt effektorprotein — intensifieras HOP1–LET7‑interaktionen och frigör LET7:s katalytiska aktivitet. Anmärkningsvärt nog kan de mänskliga motsvarigheterna till HOP1 och PP5 ersätta växtparet, vilket tyder på en konservativ aktiveringsmekanism över riken.
Klipper en nyckelström och vaktar en sensor
När LET7 är aktiv riktar den in sig på en kinas kallad CRCK3, ett enzym som tidigare kopplats till samma immunväg. CRCK3 finns i fosforylerade och defosforylerade former som kan särskiljas som två band på proteingeler. I växtceller och i provrörsassay tar aktiv LET7 selektivt bort fosfatmärken från CRCK3, medan inaktiv LET7 inte gör det. Att öka LET7‑aktiviteten eller samuttrycka den med CRCK3 ökar defosforylering och leder till celldöd och klassiska immunmarkörer, men dessa effekter dämpas när HOP1 eller NLR‑receptorn SUMM2 saknas. Parallellt fann författarna att både LET7 och HOP1, via sina TPR‑regioner, fysiskt binder till SUMM2 och ökar dess proteinmängd utan att generellt stabilisera andra NLR‑receptorer. Således hjälper samma modul som tar bort fosfat från CRCK3 också till att upprätthålla sensorn som läser det signalen.
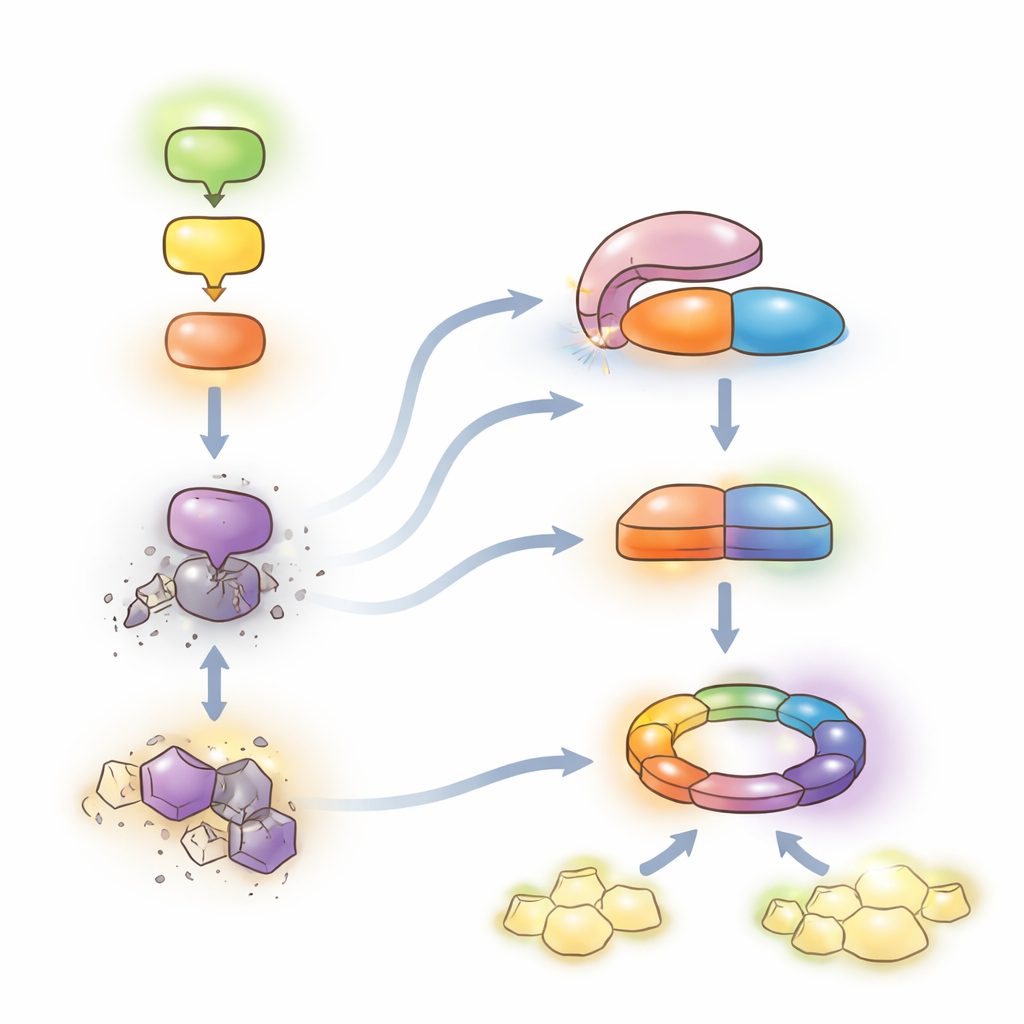
En ömtålig balans mellan skydd och tillväxt
Tillsammans stöder resultaten en modell där MEKK1–MKK1/2–MPK4‑kaskaden begränsar ett kraftfullt andrahandsförsvar. När denna kaskad är intakt förblir LET7 autoinhiberat och SUMM2‑nivåerna hålls i schack, vilket tillåter växter att förlita sig huvudsakligen på sitt vardagslarm samtidigt som de fortsätter att växa. När patogener stör kaskaden engagerar HOP1 LET7 och låser upp dess fosfatasaktivitet. LET7 defosforylerar då CRCK3 och, tillsammans med HOP1, stabiliserar SUMM2, vilket tippar systemet över i full NLR‑medierad immunitet och lokal celldöd — mycket skyddande men kostsamt för tillväxten. Genom att avslöja denna konservativa ”de‑repression”‑mekanism för PP5‑enzymer utpekar arbetet en molekylär spak som i princip skulle kunna justeras i grödor för att stärka sjukdomsresistens samtidigt som skadlig autoimmunitet minimeras.
Citering: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
Nyckelord: växtimmunitet, proteinfosfatas 5, NLR‑receptorer, signaltransduktion, Arabidopsis