Clear Sky Science · it
De-repression della fosfatasi proteica 5 da parte dell’organizzatore chaperone HOP1 attiva l’immunità NLR nelle piante
Come le piante scelgono tra crescita e autodifesa
Le piante affrontano costantemente potenziali invasori — batteri, funghi e virus — ma non possono semplicemente interrompere la crescita per combattere ogni minaccia. Questo articolo svela come un piccolo sistema molecolare a “freno e innesco” nella pianta modello Arabidopsis aiuti a decidere quando scatenare una reazione immunitaria estrema che può salvare la pianta ma anche limitarne la crescita. Comprendere questo interruttore fornisce indicazioni su come colture agricole potrebbero essere selezionate o ingegnerizzate per resistere alle malattie senza pagare un prezzo eccessivo in termini di resa.
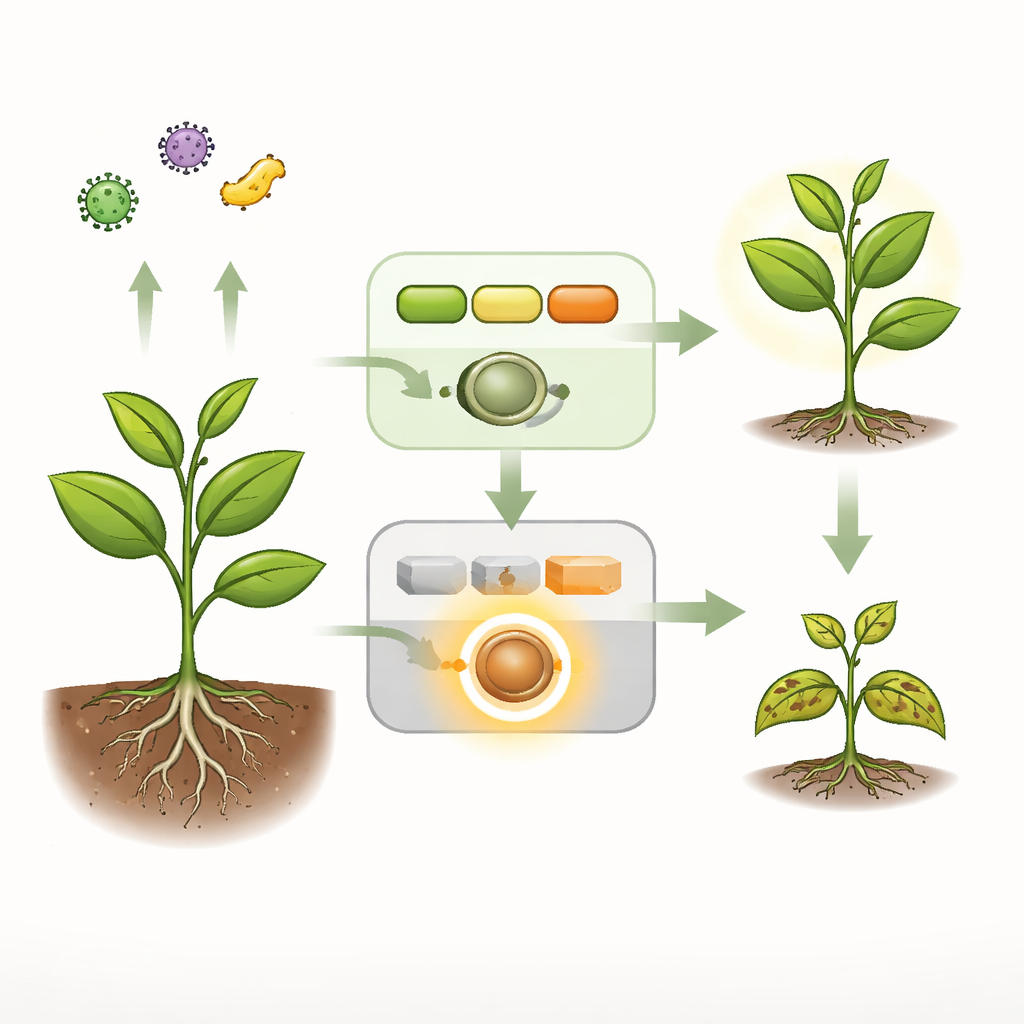
Allarmi quotidiani contro sirene d’emergenza
Le piante hanno due principali sistemi di sicurezza. Il primo è un allarme rapido e generale che riconosce firme microbiche al livello della superficie cellulare e attiva risposte protettive. Un secondo strato, più drastico, si basa su sentinelle interne chiamate recettori NLR che possono innescare difese potenti e spesso letali nelle cellule dove vengono rilevati i patogeni. In Arabidopsis sana, una catena di segnalazione composta da tre enzimi — collettivamente nota come la cascata MEKK1–MKK1/2–MPK4 — trasmette il primo allarme e al contempo mantiene silenziato un recettore NLR particolare, denominato SUMM2, impedendogli di attivarsi senza motivo. Quando questa catena è interrotta da mutazioni o da una proteina effector batterica, le piante mostrano morte cellulare spontanea, elevata attività di geni di difesa e grave nanismo, tutti segni di un’immunità fuori controllo.
Un enzima nascosto si risveglia
Gli autori hanno scoperto che una fosfatasi chiamata LET7, versione vegetale della conservata proteina PP5, è al centro di questa risposta incontrollata. Di per sé, LET7 è costruita come un coltellino a serramanico: una regione (dominio TPR) si ripiega sulla regione catalitica e la mantiene in gran parte inattiva. Schermi genetici hanno mostrato che le piante prive di LET7 non soffrono più dei sintomi letali causati quando la catena di segnalazione a monte è silenziata, collocando LET7 a valle di quella cascata. Test biochimici hanno rivelato che quando la regione catalitica di LET7 viene liberata o resa iperattiva da mutazioni specifiche, le piante sviluppano forti risposte di difesa e morte cellulare, mentre una versione cataliticamente inattiva non può produrre questi effetti. Dunque, l’attività fosfatasica di LET7 è sia necessaria sia sufficiente per guidare l’autoimmunità.
Un organizzatore molecolare rilascia il freno
Come si apre il “coltellino” molecolare? Il gruppo ha identificato una co-chaperone chiamata HOP1 come organizzatore chiave. HOP1 normalmente aiuta le proteine heat‑shock a ripiegarsi e stabilizzare altre proteine. Qui, HOP1 si lega alla regione TPR di LET7 e compete con il contatto interno che mantiene LET7 chiusa. Modellizzazione strutturale e scambi mirati di aminoacidi su entrambi i partner hanno dimostrato che questa superficie di legame è finemente sintonizzata: indebolire il contatto tra HOP1 e LET7 riduce l’attivazione di LET7. Quando la catena MEKK1–MKK1/2–MPK4 è integra, l’associazione tra HOP1 e LET7 è bassa e LET7 rimane repressa. Quando la catena è interrotta — per mutazioni, per sovrabbondanza di un altro protein scaffold o per un effector batterico — l’interazione HOP1–LET7 si intensifica, liberando l’attività catalitica di LET7. Sorprendentemente, i corrispettivi umani di HOP1 e PP5 possono sostituire la coppia vegetale, suggerendo un meccanismo di attivazione conservato tra i regni.
Tagliare un interruttore chiave e proteggere un sensore
Una volta attivata, LET7 prende di mira una chinasi chiamata CRCK3, un enzima precedentemente collegato alla stessa via immunitaria. CRCK3 esiste in forme fosforilate e defosforilate, distinguibili come due bande sui gel proteici. Nelle cellule vegetali e in saggi in vitro, LET7 attiva rimuove selettivamente i gruppi fosfato da CRCK3, mentre LET7 inattiva non lo fa. Aumentare l’attività di LET7 o co‑esprimerla con CRCK3 aumenta la defosforilazione e porta a morte cellulare e marcatori immunitari classici, ma questi effetti sono attenuati quando mancano HOP1 o il recettore NLR SUMM2. Parallelamente, gli autori hanno trovato che sia LET7 sia HOP1, tramite i loro domini TPR, si legano fisicamente a SUMM2 e ne aumentano l’abbondanza proteica senza stabilizzare in modo generale altri recettori NLR. Così, lo stesso modulo che rimuove il fosfato da CRCK3 contribuisce anche a mantenere il sensore che legge quel segnale.
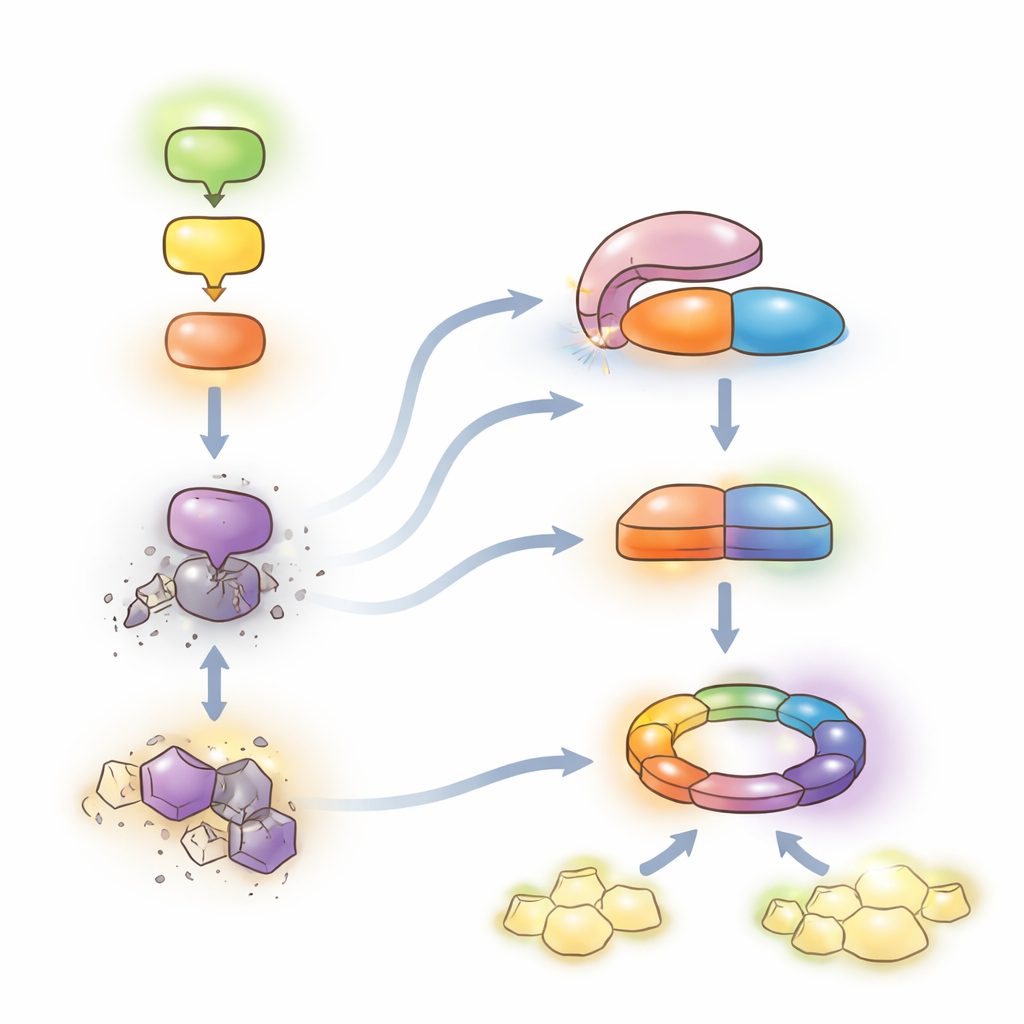
Un delicato equilibrio tra protezione e crescita
Complessivamente, i risultati supportano un modello in cui la catena MEKK1–MKK1/2–MPK4 frena una potente difesa di seconda linea. Quando questa catena è integra, LET7 rimane autoinibita e i livelli di SUMM2 sono tenuti sotto controllo, permettendo alle piante di fare affidamento principalmente sul sistema di allarme quotidiano continuando a crescere. Quando i patogeni interrompono la catena, HOP1 coinvolge LET7, sbloccandone l’attività fosfatasica. LET7 defosforila quindi CRCK3 e, insieme a HOP1, stabilizza SUMM2, facendo pendere il sistema verso un’immunità NLR completa e morte cellulare locale — altamente protettiva ma costosa per la crescita. Rivelando questo meccanismo conservato di “de-repressione” per le fosfatasi PP5, il lavoro delinea una leva molecolare che, in linea di principio, potrebbe essere modulata nelle colture per rafforzare la resistenza alle malattie minimizzando l’autoimmunità dannosa.
Citazione: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
Parole chiave: immunità delle piante, fosfatasi proteica 5, recettori NLR, trasduzione del segnale, Arabidopsis