Clear Sky Science · de
Derepression der Proteinphosphatase 5 durch den Chaperon‑Organisator HOP1 aktiviert die NLR‑Immunität von Pflanzen
Wie Pflanzen zwischen Wachstum und Selbstverteidigung entscheiden
Pflanzen sind ständig möglichen Eindringlingen ausgesetzt – Bakterien, Pilzen und Viren – können aber nicht einfach das Wachstum einstellen, um jede Bedrohung zu bekämpfen. Diese Studie legt offen, wie ein winziges molekulares „Bremse‑und‑Auslöser“-System in der Modellpflanze Arabidopsis darüber entscheidet, wann eine extreme Immunreaktion entfesselt wird, die die Pflanze retten, aber auch ihr Wachstum hemmen kann. Das Verständnis dieses Schalters liefert Hinweise darauf, wie Kulturpflanzen gezüchtet oder gentechnisch verändert werden könnten, um krankheitsresistent zu sein, ohne zu hohe Ertragsverluste in Kauf zu nehmen.
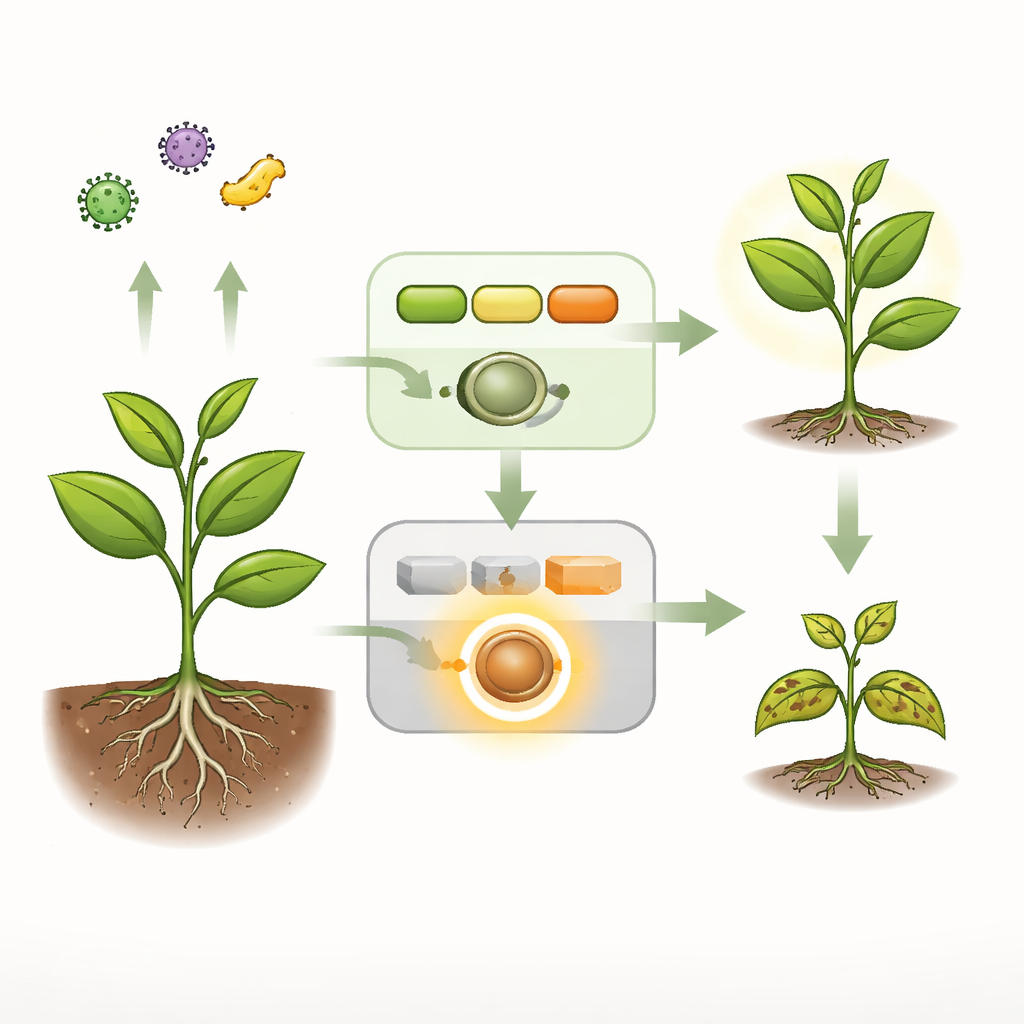
Alltägliche Alarme versus Notfallsirenen
Pflanzen betreiben zwei Hauptsicherheitssysteme. Das erste ist ein schneller, breit angelegter Alarm, der allgemeine mikrobielle Signaturen an der Zelloberfläche erkennt und Schutzreaktionen aktiviert. Eine zweite, drastischere Ebene stützt sich auf interne Wächter, die NLR‑Rezeptoren genannt werden und in Zellen, in denen Pathogene entdeckt werden, eine starke, oft tödliche Abwehr auslösen können. In gesundem Arabidopsis vermittelt eine Signalkette aus drei Enzymen – zusammengefasst als MEKK1–MKK1/2–MPK4‑Kaskade – sowohl den ersten Alarm als auch die stille Unterdrückung eines bestimmten NLR‑Rezeptors namens SUMM2. Wird diese Kette durch Mutation oder ein bakterielles Effektorprotein unterbrochen, zeigen Pflanzen spontane Zellsterben, hohe Aktivität von Abwehrgenen und starken Zwergwuchs – alles Anzeichen einer entgleisten Immunantwort.
Ein verborgenes Enzym erwacht
Die Autorinnen und Autoren entdeckten, dass eine Phosphatase namens LET7, die pflanzliche Version des konservierten Proteins PP5, im Zentrum dieser entgleisten Reaktion steht. LET7 selbst ist wie ein gefaltetes Taschenmesser aufgebaut: Eine Region (TPR‑Domäne) klappt über die katalytische Region und hält diese weitgehend abgeschaltet. Genetische Screens zeigten, dass Pflanzen ohne LET7 nicht mehr an den tödlichen Symptomen leiden, die auftreten, wenn die upstream Signalkette stillgelegt ist, womit LET7 hinter dieser Kaskade eingeordnet wird. Biochemische Tests ergaben, dass, wenn die katalytische Region von LET7 befreit oder durch spezifische Mutationen hyperaktiviert wird, Pflanzen starke Abwehrreaktionen und Zellsterben entwickeln, während eine katalytisch tote Variante diese Effekte nicht auslöst. Somit ist die Phosphataseaktivität von LET7 sowohl notwendig als auch ausreichend, um Autoimmunität anzutreiben.
Ein molekularer Organisator löst die Bremse
Wie öffnet sich das molekulare Taschenmesser? Das Team identifizierte ein Co‑Chaperon namens HOP1 als wichtigen Organisator. HOP1 hilft normalerweise Hitzeschockproteinen beim Falten und Stabilisieren anderer Proteine. Hier bindet es an die TPR‑Region von LET7 und verdrängt die interne Kontaktstelle, die LET7 geschlossen hält. Strukturelle Modellierung und gezielte Aminosäureaustausche an beiden Partnern zeigten, dass diese Bindungsfläche fein abgestimmt ist: Abschwächung der Wechselwirkung zwischen HOP1 und LET7 reduziert die Aktivierung von LET7. Wenn die MEKK1–MKK1/2–MPK4‑Kette intakt ist, ist die Assoziation zwischen HOP1 und LET7 gering und LET7 bleibt repressed. Wird die Kette gestört – durch Mutationen, durch Übermaß eines anderen Scaffold‑Proteins oder durch ein bakterielles Effektorprotein – intensiviert sich die HOP1–LET7‑Interaktion und entfesselt die katalytische Aktivität von LET7. Bemerkenswerterweise können die menschlichen Gegenstücke von HOP1 und PP5 das Pflanzenpaar ersetzen, was auf einen konservierten Aktivierungsmechanismus über die Reiche hinweist.
Schneiden eines Schlüsselschalters und Bewachen eines Sensors
Einmal aktiv, zielt LET7 auf eine Kinase namens CRCK3, ein Enzym, das zuvor mit demselben Immunweg in Verbindung gebracht wurde. CRCK3 liegt in phosphorylierter und dephosphorylierter Form vor, die sich als zwei Banden auf Proteingele nacheinander unterscheiden lassen. In Pflanzenzellen und Reagenzglas‑Assays entfernt aktives LET7 selektiv Phosphatmarken von CRCK3, während inaktives LET7 dies nicht tut. Die Verstärkung der LET7‑Aktivität oder Koexpression mit CRCK3 fördert die Dephosphorylierung und führt zu Zellsterben und typischen Immunmarkern, doch diese Effekte sind abgeschwächt, wenn HOP1 oder der NLR‑Rezeptor SUMM2 fehlen. Parallel dazu fanden die Autorinnen und Autoren, dass sowohl LET7 als auch HOP1 über ihre TPR‑Regionen physisch an SUMM2 binden und dessen Proteinmenge erhöhen, ohne allgemein andere NLR‑Rezeptoren zu stabilisieren. Somit hilft dasselbe Modul, das Phosphat von CRCK3 entfernt, zugleich, den Sensor zu erhalten, der dieses Signal abliest.
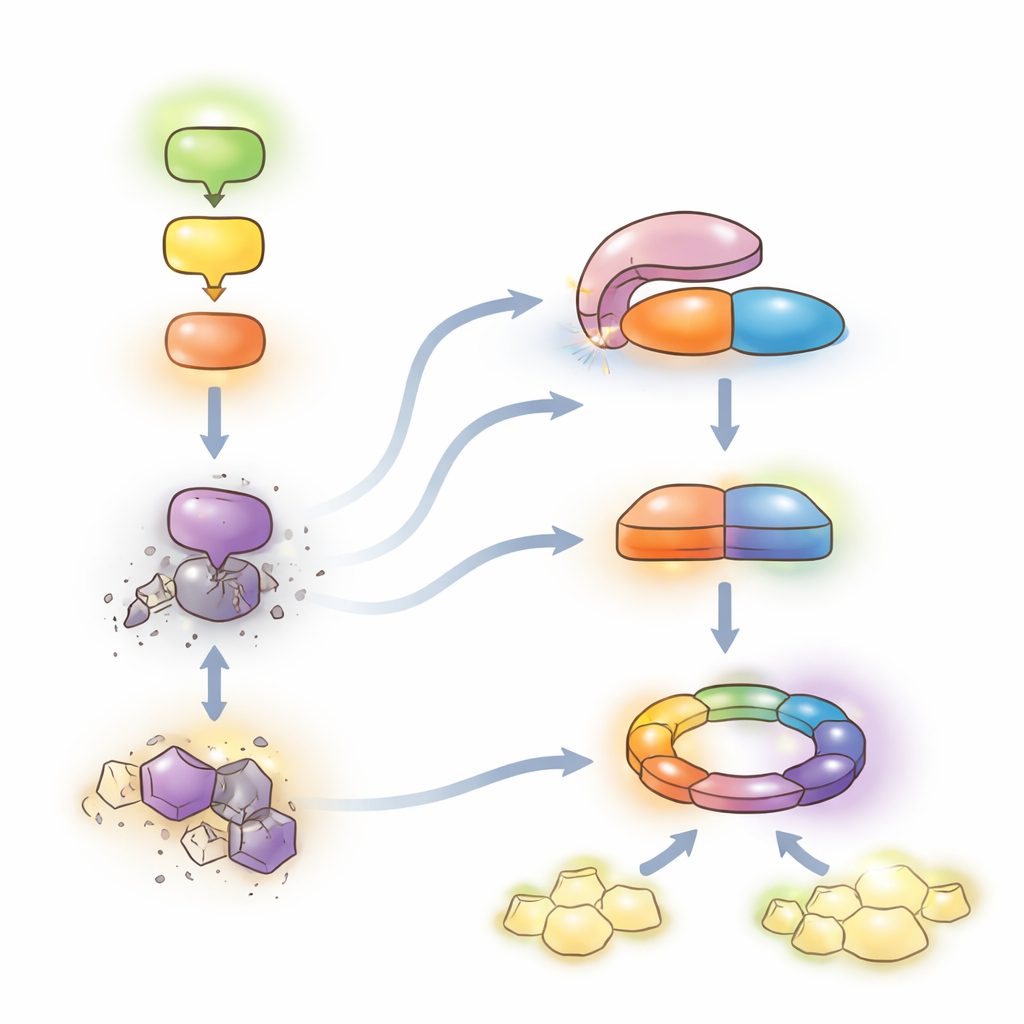
Ein empfindliches Gleichgewicht zwischen Schutz und Wachstum
Zusammen stützen die Befunde ein Modell, in dem die MEKK1–MKK1/2–MPK4‑Kette eine mächtige zweite Verteidigungslinie zurückhält. Ist diese Kette intakt, bleibt LET7 autoinhibiert und die SUMM2‑Spiegel werden kontrolliert, sodass Pflanzen hauptsächlich auf ihr alltägliches Alarmsystem vertrauen und weiter wachsen können. Stören Pathogene die Kette, aktiviert HOP1 LET7 und schaltet dessen Phosphataseaktivität frei. LET7 dephosphoryliert dann CRCK3 und stabilisiert zusammen mit HOP1 SUMM2, wodurch das System in eine voll ausgeprägte NLR‑vermittelte Immunantwort mit lokalem Zellsterben kippt – hochgradig schützend, aber wachstumsintensiv kostspielig. Indem diese konservierte „De‑Repressions“‑Mechanik für PP5‑Enzyme offenbart wird, skizziert die Arbeit einen molekularen Hebel, der prinzipiell in Kulturpflanzen angepasst werden könnte, um die Krankheitsresistenz zu stärken und schädliche Autoimmunität zu minimieren.
Zitation: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
Schlüsselwörter: Pflanzenimmunität, Proteinphosphatase 5, NLR‑Rezeptoren, Signaltransduktion, Arabidopsis