Clear Sky Science · pt
Desrepressão da fosfatase de proteína 5 pelo organizador de chaperona HOP1 ativa a imunidade NLR em plantas
Como as plantas decidem entre crescimento e autodefesa
As plantas enfrentam constantemente invasores em potencial — bactérias, fungos e vírus —, mas não podem simplesmente abandonar o crescimento para combater toda ameaça. Este artigo revela como um minúsculo sistema molecular de “freio e gatilho” na planta modelo Arabidopsis ajuda a decidir quando desencadear uma reação imune extrema que pode salvar a planta, mas também retardar seu crescimento. Entender esse interruptor oferece insights sobre como cultivar ou engenheirar lavouras resistentes a doenças sem pagar um preço excessivo em produtividade.
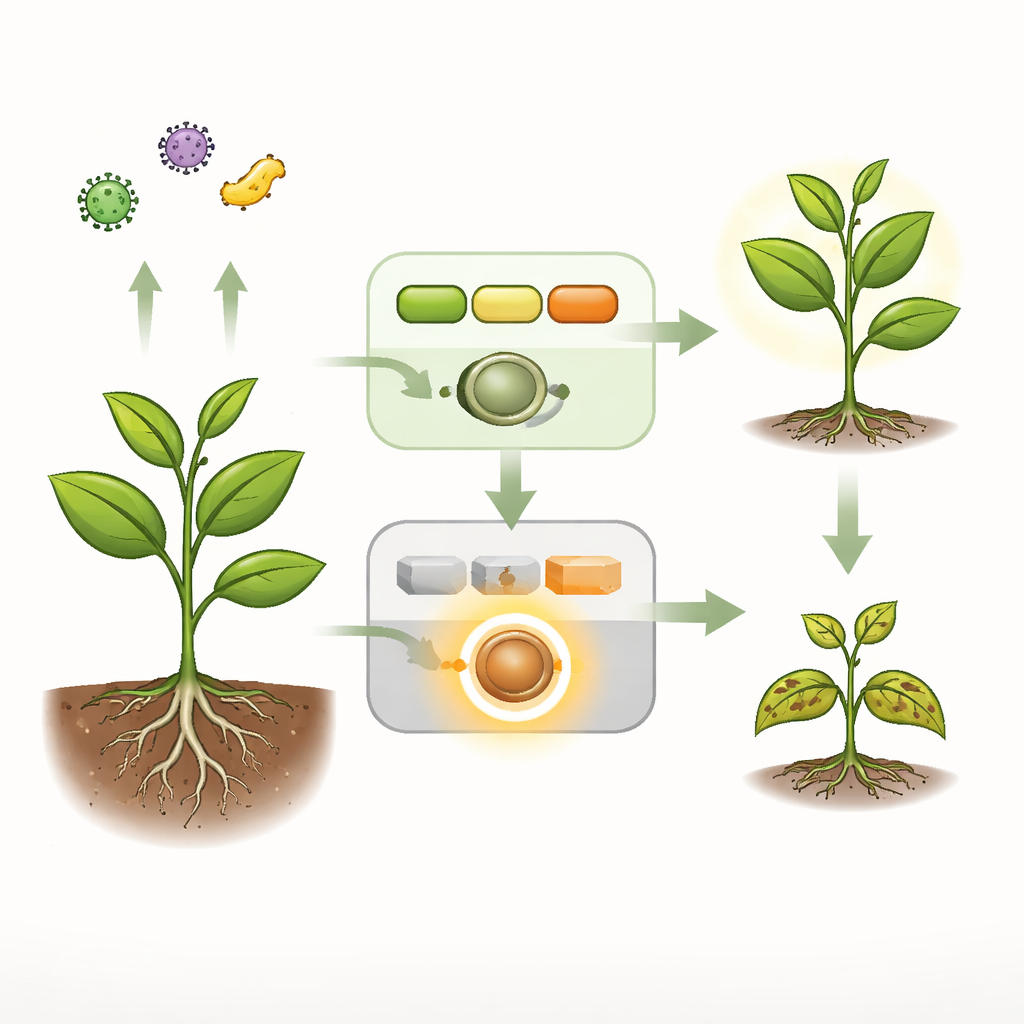
Alarmes cotidianos versus sirenes de emergência
As plantas operam dois principais sistemas de segurança. O primeiro é um alarme rápido e amplo que detecta sinais microbianos gerais na superfície celular e ativa respostas protetoras. Uma segunda camada, mais drástica, depende de sentinelas internas chamadas receptores NLR, que podem desencadear defesas potentes e frequentemente letais nas células onde patógenos são detectados. Em Arabidopsis saudável, uma cadeia de sinalização composta por três enzimas — coletivamente chamada de cascata MEKK1–MKK1/2–MPK4 — tanto transmite o primeiro alarme quanto mantém, de forma silenciosa, um receptor NLR em particular, chamado SUMM2, desativado quando não há motivo. Quando essa cadeia é interrompida por mutação ou por uma proteína efetora bacteriana, as plantas exibem morte celular espontânea, alta atividade de genes de defesa e nanismo severo — todos sinais de imunidade descontrolada.
Uma enzima oculta desperta
Os autores descobriram que uma fosfatase chamada LET7, uma versão vegetal da proteína conservada PP5, está no centro dessa resposta fora de controle. Por si só, LET7 é construída como um canivete dobrável: uma região (domínio TPR) dobra-se sobre a região catalítica e a mantém amplamente inativa. Triagens genéticas mostraram que plantas sem LET7 deixaram de sofrer os sintomas letais causados quando a cadeia de sinalização a montante é silenciada, situando LET7 a jusante dessa cascata. Testes bioquímicos revelaram que, quando a região catalítica de LET7 é liberada ou tornada hiperativa por mutações específicas, as plantas desenvolvem fortes respostas de defesa e morte celular, enquanto uma versão cataliticamente inativa não provoca esses efeitos. Assim, a atividade da fosfatase LET7 é ao mesmo tempo necessária e suficiente para impulsionar a autoimunidade.
Um organizador molecular solta o freio
Como o canivete molecular se abre? A equipe identificou uma co‑chaperona chamada HOP1 como um organizador chave. HOP1 normalmente ajuda proteínas de choque térmico a dobrar e estabilizar outras proteínas. Aqui, ela se liga à região TPR de LET7 e vence o contato interno que mantém LET7 fechado. Modelagem estrutural e trocas precisas de aminoácidos em ambos os parceiros mostraram que essa superfície de interação é finamente ajustada: enfraquecer o contato entre HOP1 e LET7 reduz a ativação de LET7. Quando a cadeia MEKK1–MKK1/2–MPK4 está intacta, a associação entre HOP1 e LET7 é baixa e LET7 permanece reprimida. Quando a cadeia é perturbada — por mutações, por superabundância de outra proteína andaime, ou por um efetor bacteriano — a interação HOP1–LET7 se intensifica, liberando a atividade catalítica de LET7. Notavelmente, os homólogos humanos de HOP1 e PP5 podem substituir o par vegetal, apontando para um mecanismo de ativação conservado entre reinos.
Cortando um interruptor chave e protegendo um sensor
Uma vez ativa, LET7 tem como alvo uma quinase chamada CRCK3, uma enzima anteriormente ligada à mesma via imune. CRCK3 existe em formas fosforilada e desfosforilada, que podem ser distinguidas como duas bandas em géis de proteínas. Em células vegetais e em ensaios in vitro, LET7 ativa remove seletivamente marcas de fosfato de CRCK3, enquanto LET7 inativa não o faz. Aumentar a atividade de LET7 ou coexpressá‑la com CRCK3 eleva a desfosforilação e leva à morte celular e a marcadores clássicos de imunidade, mas esses efeitos são atenuados quando HOP1 ou o receptor NLR SUMM2 está ausente. Em paralelo, os autores descobriram que tanto LET7 quanto HOP1, por meio de seus domínios TPR, ligam‑se fisicamente a SUMM2 e aumentam sua abundância proteica sem estabilizar amplamente outros receptores NLR. Assim, o mesmo módulo que remove o fosfato de CRCK3 também ajuda a manter o sensor que lê esse sinal.
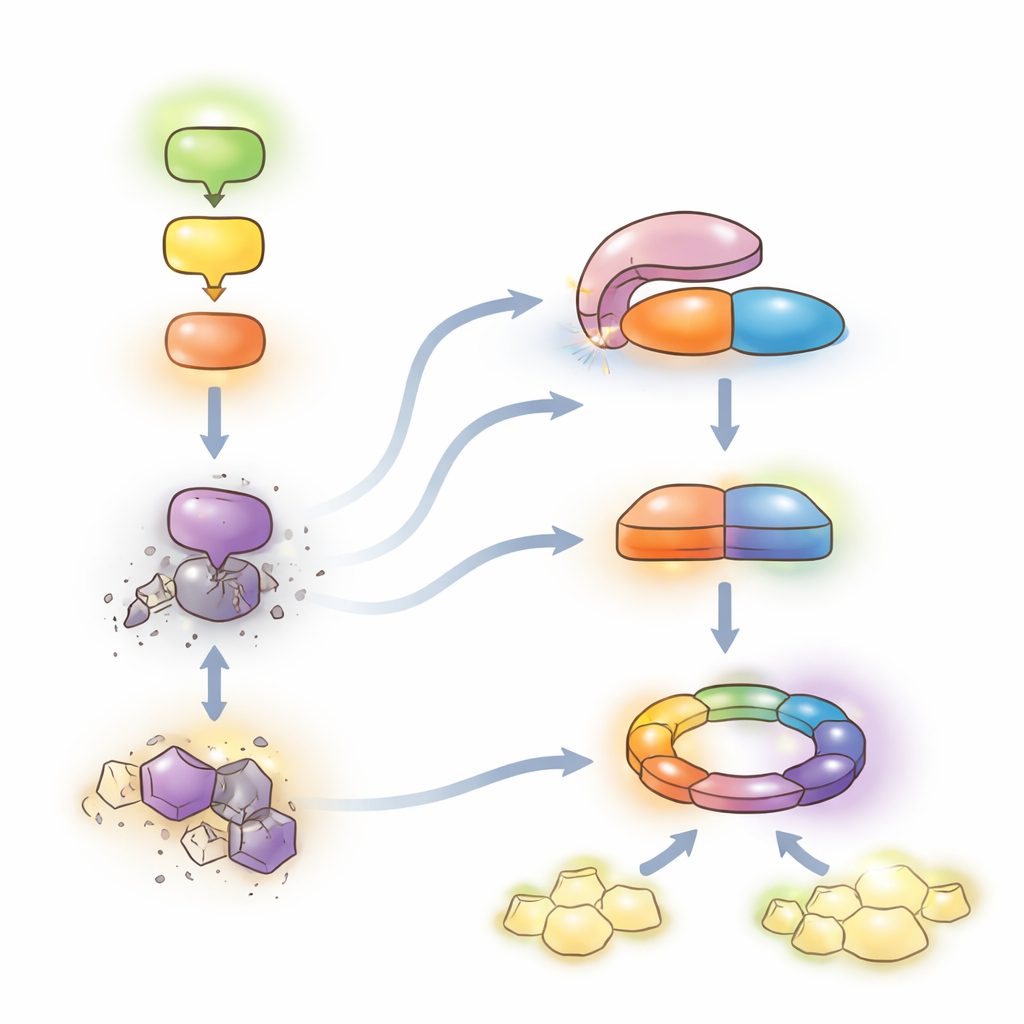
Um equilíbrio delicado entre proteção e crescimento
Em conjunto, os achados sustentam um modelo no qual a cadeia MEKK1–MKK1/2–MPK4 reprime uma defesa poderosa de segunda linha. Quando essa cadeia está intacta, LET7 permanece autoinibida e os níveis de SUMM2 ficam controlados, permitindo que as plantas dependam principalmente do seu sistema de alarme cotidiano enquanto continuam a crescer. Quando patógenos perturbam a cadeia, HOP1 engaja LET7, desbloqueando sua atividade de fosfatase. LET7 então desfosforila CRCK3 e, junto com HOP1, estabiliza SUMM2, deslocando o sistema para uma imunidade NLR completa e morte celular local — altamente protetora, porém custosa ao crescimento. Ao revelar esse mecanismo conservado de “desrepressão” para enzimas PP5, o trabalho descreve uma alavanca molecular que, em princípio, poderia ser ajustada em culturas para fortalecer a resistência a doenças minimizando a autoimunidade prejudicial.
Citação: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
Palavras-chave: imunidade vegetal, fosfatase de proteína 5, receptores NLR, transdução de sinal, Arabidopsis