Clear Sky Science · fr
Dérépression de la phosphatase protéique 5 par l’organisateur chaperon HOP1 active l’immunité NLR des plantes
Comment les plantes choisissent entre croissance et autodéfense
Les plantes font face en permanence à de potentiels envahisseurs — bactéries, champignons et virus — mais elles ne peuvent pas simplement abandonner la croissance pour combattre chaque menace. Cet article révèle comment un petit système moléculaire « frein et déclencheur » chez la plante modèle Arabidopsis aide à décider quand libérer une réaction immunitaire extrême qui peut sauver la plante mais aussi freiner sa croissance. Comprendre cet interrupteur apporte un éclairage sur la façon dont les cultures pourraient être sélectionnées ou modifiées pour résister aux maladies sans payer un trop lourd tribut en rendement.
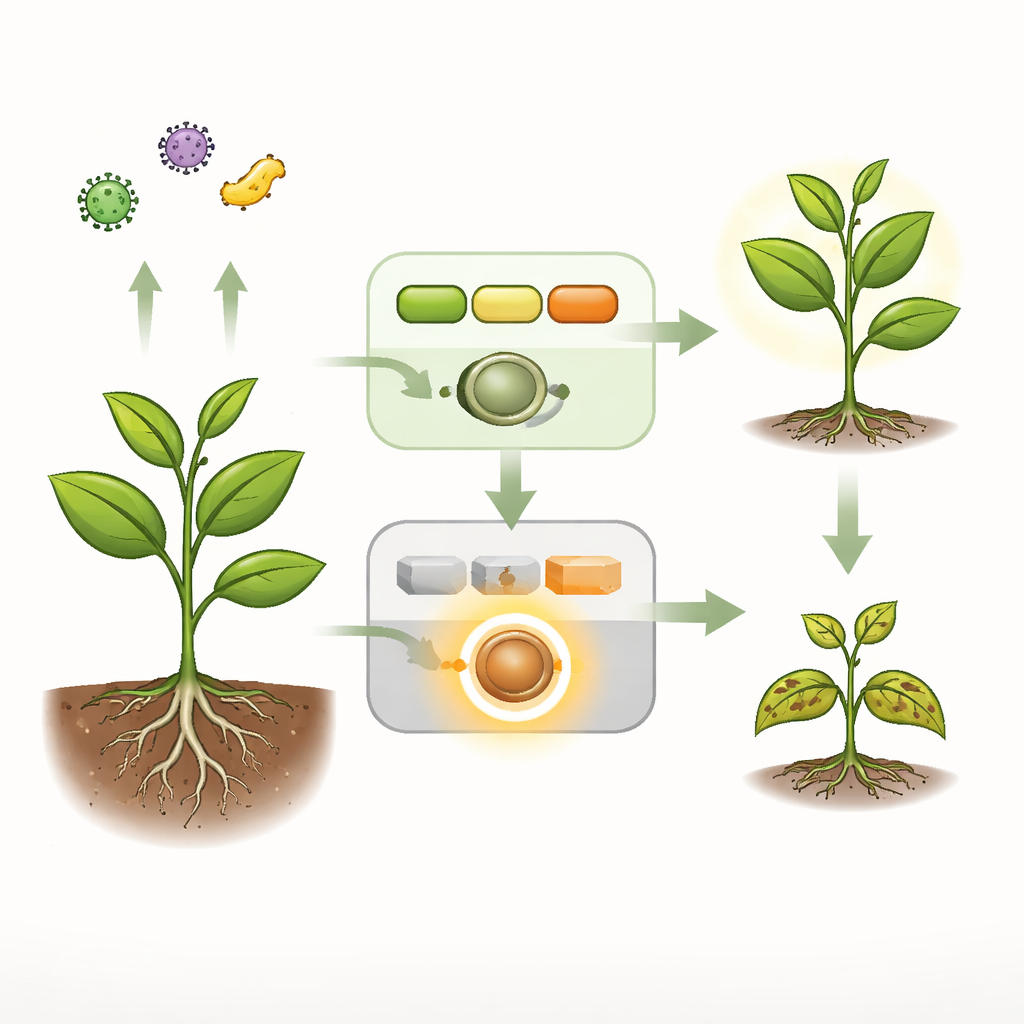
Alarmes quotidiennes contre sirènes d’urgence
Les plantes utilisent deux systèmes de sécurité principaux. Le premier est une alarme rapide et générale qui détecte des signatures microbiennes à la surface cellulaire et déclenche des réponses protectrices. Une seconde couche, plus radicale, repose sur des sentinelles internes appelées récepteurs NLR capables de déclencher des défenses puissantes, souvent létales, dans les cellules où des pathogènes sont détectés. Chez Arabidopsis sain, une chaîne de signalisation composée de trois enzymes — collectivement appelée cascade MEKK1–MKK1/2–MPK4 — relaie la première alarme tout en empêchant discrètement qu’un récepteur NLR particulier, nommé SUMM2, ne s’active sans raison. Lorsque cette chaîne est rompue par une mutation ou par une protéine effectrice bactérienne, les plantes présentent une mort cellulaire spontanée, une forte activité des gènes de défense et un nanisme sévère, autant de signes d’une immunité incontrôlée.
Une enzyme cachée s’éveille
Les auteurs ont découvert qu’une phosphatase appelée LET7, version végétale de la protéine conservée PP5, se trouve au cœur de cette réponse incontrôlée. À elle seule, LET7 est construite comme un couteau de poche replié : une région (domaine TPR) replie sur la région catalytique et la maintient largement inactive. Des cribles génétiques ont montré que les plantes dépourvues de LET7 ne souffraient plus des symptômes létaux causés lorsque la chaîne de signalisation en amont est inhibée, plaçant LET7 en aval de cette cascade. Des tests biochimiques ont révélé que lorsque la région catalytique de LET7 est libérée ou rendue hyperactive par des mutations spécifiques, les plantes développent de fortes réponses de défense et une mort cellulaire, alors qu’une version catalytiquement inactive ne peut pas déclencher ces effets. Ainsi, l’activité phosphatase de LET7 est à la fois nécessaire et suffisante pour provoquer l’auto-immunité.
Un organisateur moléculaire libère le frein
Comment le couteau de poche moléculaire s’ouvre-t-il ? L’équipe a identifié une protéine co-chaperonne appelée HOP1 comme organisateur clé. HOP1 aide normalement les protéines de choc thermique (heat-shock proteins) à plier et stabiliser d’autres protéines. Ici, elle se lie à la région TPR de LET7 et concurrence le contact interne qui maintient LET7 fermé. La modélisation structurale et des échanges d’acides aminés précis sur les deux partenaires ont montré que cette surface de liaison est finement réglée : affaiblir le contact entre HOP1 et LET7 réduit l’activation de LET7. Lorsque la chaîne MEKK1–MKK1/2–MPK4 est intacte, l’association entre HOP1 et LET7 est faible et LET7 reste réprimée. Quand la cascade est perturbée — par des mutations, par un excès d’une autre protéine échafaud ou par un effecteur bactérien — l’interaction HOP1–LET7 s’intensifie, déchaînant l’activité catalytique de LET7. Remarquablement, les homologues humains de HOP1 et PP5 peuvent se substituer au couple végétal, ce qui suggère un mécanisme d’activation conservé entre règnes.
Couper un interrupteur clé et protéger un détecteur
Une fois active, LET7 cible une kinase appelée CRCK3, une enzyme précédemment liée à la même voie immunitaire. CRCK3 existe sous formes phosphorylée et déphosphorylée, distinguables comme deux bandes sur des gels protéiques. Dans les cellules végétales et dans des essais in vitro, LET7 active enlève sélectivement les marques de phosphate de CRCK3, tandis que LET7 inactive ne le fait pas. Augmenter l’activité de LET7 ou co‑exprimer LET7 avec CRCK3 favorise la déphosphorylation et conduit à la mort cellulaire et à des marqueurs immunitaires classiques, mais ces effets sont atténués lorsque HOP1 ou le récepteur NLR SUMM2 font défaut. Parallèlement, les auteurs ont montré que LET7 et HOP1, via leurs régions TPR, se lient physiquement à SUMM2 et augmentent son abondance protéique sans stabiliser de façon générale d’autres récepteurs NLR. Ainsi, le même module qui retire le phosphate de CRCK3 contribue aussi à maintenir le détecteur qui lit ce signal.
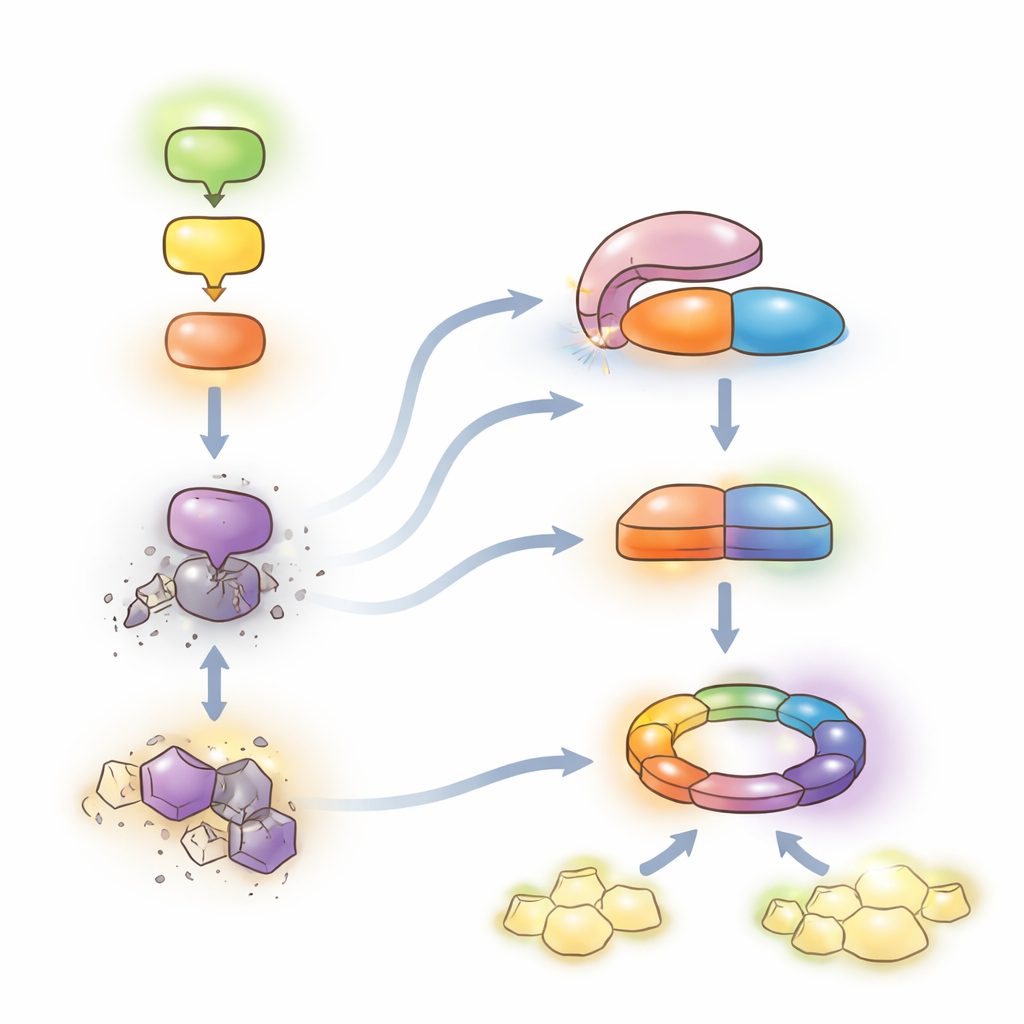
Un équilibre délicat entre protection et croissance
Au total, ces résultats soutiennent un modèle dans lequel la chaîne MEKK1–MKK1/2–MPK4 freine une défense de second rang puissante. Quand cette chaîne est intacte, LET7 reste auto-inhibée et les niveaux de SUMM2 sont contenus, permettant aux plantes de s’appuyer principalement sur leur système d’alarme quotidien tout en poursuivant leur croissance. Lorsque des pathogènes perturbent la chaîne, HOP1 engage LET7 et libère son activité phosphatase. LET7 déphosphoryle alors CRCK3 et, avec HOP1, stabilise SUMM2, faisant basculer le système vers une immunité NLR complète et une mort cellulaire locale — très protectrice mais coûteuse pour la croissance. En révélant ce mécanisme de « dérépression » conservé pour les enzymes PP5, le travail décrit un levier moléculaire qui pourrait, en principe, être modulé dans les cultures pour renforcer la résistance aux maladies tout en minimisant l’auto-immunité nuisible.
Citation: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
Mots-clés: immunité des plantes, phosphatase protéique 5, récepteurs NLR, transduction du signal, Arabidopsis