Clear Sky Science · pl
De-represja fosfatazy białkowej 5 przez organizator chaperonowy HOP1 aktywuje odporność NLR u roślin
Jak rośliny wybierają między wzrostem a samoobroną
Rośliny nieustannie stają w obliczu potencjalnych najeźdźców — bakterii, grzybów i wirusów — ale nie mogą po prostu porzucić wzrostu, by zwalczać każde zagrożenie. W artykule opisano, jak niewielki molekularny system „hamulca i spustu” w roślinie modelowej Arabidopsis pomaga zdecydować, kiedy uwolnić ekstremalną reakcję odpornościową, która może uratować roślinę, a jednocześnie zahamować jej wzrost. Zrozumienie tego przełącznika daje wgląd w to, jak uprawy można by hodować lub genetycznie modyfikować, by były odporne na choroby bez nadmiernego obniżania plonów.
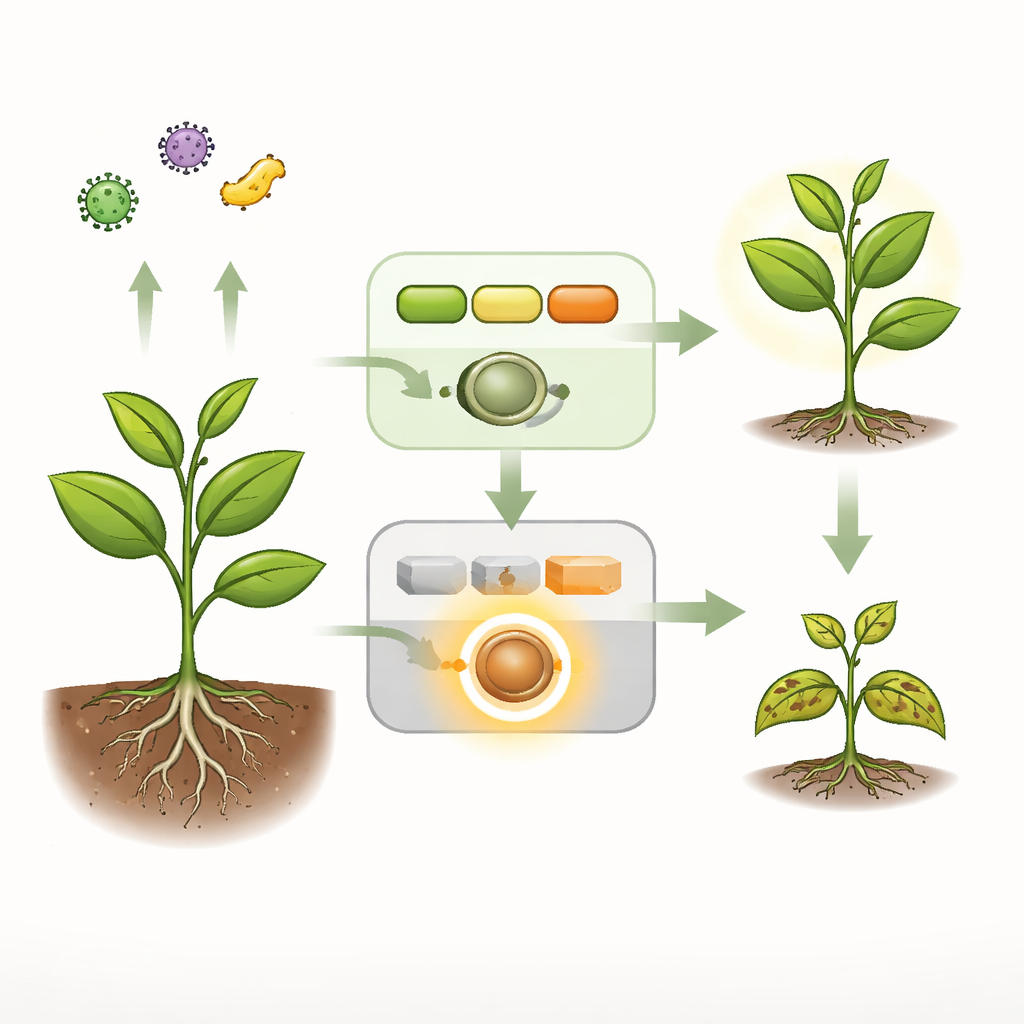
Codzienne alarmy kontra syreny awaryjne
Rośliny mają dwa główne systemy bezpieczeństwa. Pierwszy to szybki, szeroki alarm wykrywający ogólne odciski mikroorganizmów na powierzchni komórki i uruchamiający odpowiedzi ochronne. Druga, bardziej drastyczna warstwa opiera się na wewnętrznych strażnikach zwanych receptorami NLR, które mogą wywołać potężną, często śmiertelną obronę w komórkach, gdzie wykryto patogeny. U zdrowego Arabidopsis łańcuch sygnałowy złożony z trzech enzymów — zbiorczo nazywany kaskadą MEKK1–MKK1/2–MPK4 — zarówno przekazuje pierwszy alarm, jak i cicho powstrzymuje jeden szczególny receptor NLR, nazwany SUMM2, przed bezpodstawnym uruchomieniem. Gdy łańcuch ten zostanie przerwany przez mutację lub przez białko efektorowe bakterii, rośliny wykazują spontaniczną śmierć komórek, wysoką aktywność genów obronnych i silny karłowaty wzrost — wszystko objawy niekontrolowanej odporności.
Budzący się ukryty enzym
Autorzy odkryli, że fosfataza o nazwie LET7, roślinna wersja konserwowanego białka PP5, stoi w centrum tej odpowiedzi. Sama LET7 przypomina złożony scyzoryk: jeden region (domena TPR) zagina się na region katalityczny i w dużej mierze go blokuje. Badania genetyczne wykazały, że rośliny pozbawione LET7 nie doświadczają już śmiertelnych objawów powodowanych wyciszeniem łańcucha sygnałowego upstream, co umieszcza LET7 poniżej tej kaskady. Testy biochemiczne ujawniły, że kiedy region katalityczny LET7 zostaje uwolniony lub wymuszony do nadaktywności przez konkretne mutacje, rośliny rozwijają silne reakcje obronne i śmierć komórek, podczas gdy katalitycznie nieaktywny wariant nie wywołuje tych efektów. Zatem aktywność fosfatazowa LET7 jest jednocześnie niezbędna i wystarczająca do napędzenia autoimmunizacji.
Molekularny organizator zwalnia hamulec
Jak otwiera się molekularny scyzoryk? Zespół zidentyfikował białko współchaperonowe o nazwie HOP1 jako kluczowego organizatora. HOP1 zwykle pomaga białkom szoku termicznego w fałdowaniu i stabilizacji innych białek. Tutaj przyłącza się do regionu TPR LET7 i konkurencyjnie wypiera wewnętrzny kontakt utrzymujący LET7 w stanie zamkniętym. Modelowanie strukturalne i precyzyjne zamiany aminokwasów po obu stronach pokazały, że ta powierzchnia wiązania jest delikatnie dostrojona: osłabienie kontaktu między HOP1 a LET7 zmniejsza aktywację LET7. Gdy łańcuch MEKK1–MKK1/2–MPK4 jest nieuszkodzony, stowarzyszenie HOP1 i LET7 jest niskie i LET7 pozostaje zahamowana. Gdy łańcuch zostaje zakłócony — przez mutacje, nadmiar innego białka rusztowania lub przez efektor bakteryjny — interakcja HOP1–LET7 nasila się, uwalniając aktywność katalityczną LET7. Co godne uwagi, ludzkie odpowiedniki HOP1 i PP5 mogą zastąpić parę roślinną, co wskazuje na zachowany mechanizm aktywacji w różnych królestwach życia.
Przecięcie kluczowego przełącznika i ochrona sensora
Po aktywacji LET7 celuje w kinazę nazwaną CRCK3, enzym wcześniej powiązany z tą samą ścieżką immunologiczną. CRCK3 występuje w formach fosforylowanej i defosforylowanej, które można rozróżnić jako dwa pasma na żelach białkowych. W komórkach roślinnych i testach in vitro aktywna LET7 selektywnie usuwa reszty fosforanowe z CRCK3, podczas gdy nieaktywna LET7 tego nie robi. Zwiększenie aktywności LET7 lub współekspresja z CRCK3 nasila defosforylację i prowadzi do śmierci komórek oraz klasycznych markerów odporności, ale efekty te są stłumione, gdy brakuje HOP1 lub receptora NLR SUMM2. Równocześnie autorzy wykazali, że zarówno LET7, jak i HOP1, poprzez swoje domeny TPR, fizycznie wiążą się z SUMM2 i zwiększają jego obfitość białkową, nie stabilizując przy tym szeroko innych receptorów NLR. Tak więc ten sam moduł, który usuwa fosfor z CRCK3, pomaga też utrzymać czujnik odczytujący ten sygnał.
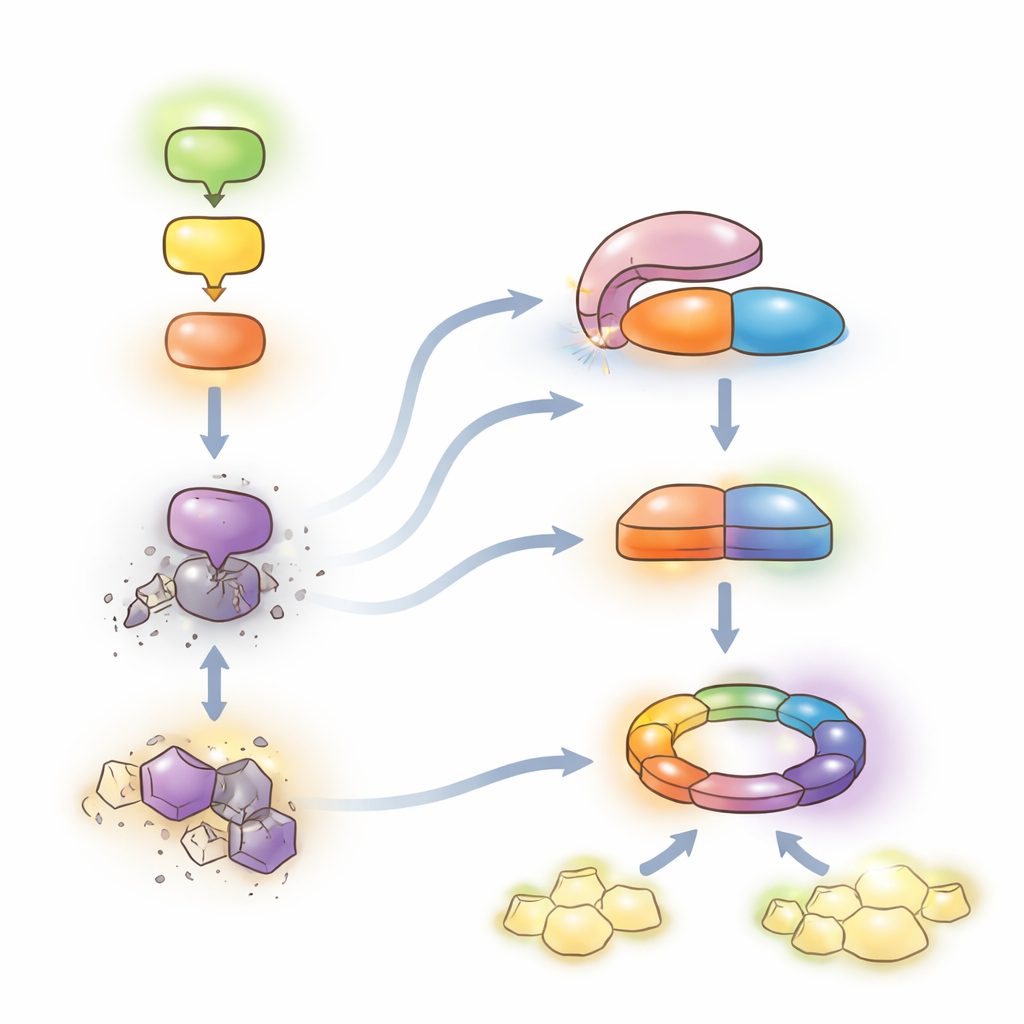
Delikatna równowaga między ochroną a wzrostem
Razem wyniki wspierają model, w którym łańcuch MEKK1–MKK1/2–MPK4 powstrzymuje potężną obronę drugiej linii. Gdy łańcuch jest nienaruszony, LET7 pozostaje autozaintynyktowany, a poziomy SUMM2 są kontrolowane, co pozwala roślinom polegać głównie na codziennym systemie alarmowym, kontynuując wzrost. Gdy patogeny zakłócają łańcuch, HOP1 angażuje LET7, odblokowując jego aktywność fosfatazową. LET7 defosforyluje wtedy CRCK3 i, razem z HOP1, stabilizuje SUMM2, przechylając system w stronę pełnej odporności mediowanej przez NLR i lokalnej śmierci komórek — wysoce ochronnej, ale kosztownej dla wzrostu. Poprzez ujawnienie tego konserwowanego mechanizmu „de-represji” dla enzymów PP5, praca wskazuje molekularną dźwignię, którą w zasadzie można by dostroić w uprawach, by wzmocnić odporność na choroby przy jednoczesnym zminimalizowaniu szkodliwej autoimmunizacji.
Cytowanie: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
Słowa kluczowe: odporność roślin, fosfataza białkowa 5, receptory NLR, transdukcja sygnału, Arabidopsis