Clear Sky Science · nl
De-repressie van proteïnefosfatase 5 door de chaperone-organisator HOP1 activeert plant-NLR-immuniteit
Hoe planten kiezen tussen groei en zelfverdediging
Planten worden voortdurend geconfronteerd met potentiële indringers — bacteriën, schimmels en virussen — maar ze kunnen niet simpelweg hun groei opgeven om elke dreiging te bestrijden. Dit artikel onthult hoe een klein moleculair "rem- en ontstekingssysteem" in de modelplant Arabidopsis helpt beslissen wanneer een extreme immuunreactie losgelaten moet worden: een reactie die de plant kan redden maar ook de groei kan remmen. Inzicht in deze schakel geeft aanknopingspunten voor hoe gewassen gefokt of gemodificeerd zouden kunnen worden om ziektebestendigheid te verbeteren zonder te veel opbrengstverlies.
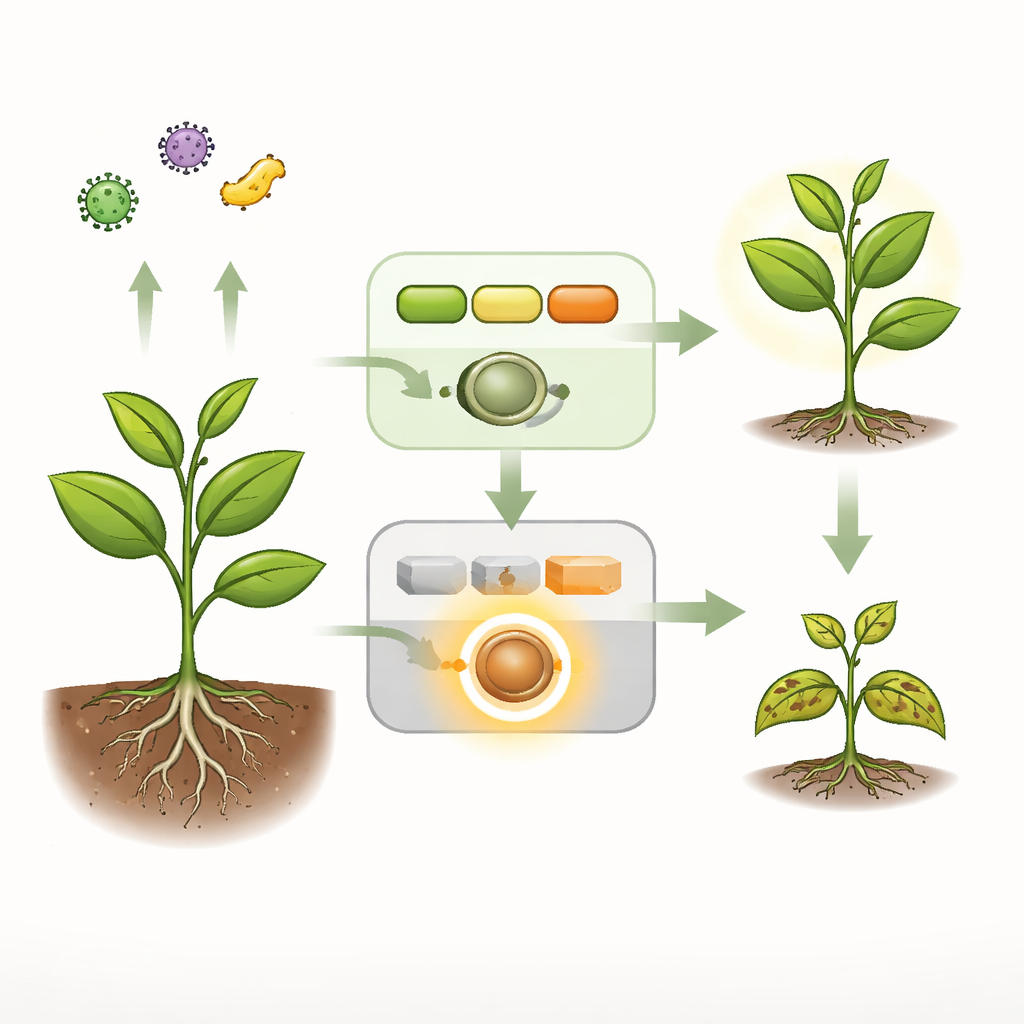
Dagelijkse alarmen versus noodsirènes
Planten hanteren twee hoofdbeveiligingssystemen. Het eerste is een snel, breed alarm dat algemene microbiale signatuur op het celoppervlak detecteert en beschermende reacties activeert. Een tweede, ingrijpendere laag berust op interne wachters genaamd NLR-receptoren die krachtige, vaak levensbedreigende verdedigingsreacties kunnen uitlokken in cellen waar pathogenen worden gedetecteerd. In gezonde Arabidopsis zorgt een signaalketen van drie enzymen — gezamenlijk het MEKK1–MKK1/2–MPK4-cascade genoemd — zowel voor het doorgeven van het eerste alarm als voor het stilletjes onderdrukken van één specifieke NLR-receptor, SUMM2, zodat die niet zonder reden afgaat. Wanneer deze keten wordt verbroken door mutatie of door een bacterieel effector-eiwit, vertonen planten spontane celdood, hoge activiteit van verdedigingsgenen en ernstige dwerggroei, allemaal aanwijzingen van ontspoorde immuniteit.
Een verborgen enzym ontwaakt
De auteurs ontdekten dat een fosfatase-enzym genaamd LET7, een plantaardige variant van het geconserveerde eiwit PP5, centraal staat in deze ontspoorde reactie. LET7 heeft van zichzelf de vorm van een opgevouwen zakmes: een regio (een TPR-domein) vouwt zich terug op de katalytische regio en houdt die grotendeels uitgeschakeld. Genetische screens toonden aan dat planten zonder LET7 de dodelijke symptomen niet langer vertonen wanneer de upstream signaalketen wordt stilgelegd, wat LET7 stroomafwaarts van die cascade plaatst. Biochemische testen lieten zien dat wanneer de katalytische regio van LET7 vrijgemaakt of hyperactief gemaakt wordt door specifieke mutaties, planten sterke verdedigingsreacties en celdood ontwikkelen, terwijl een catalytisch dood variant deze effecten niet kan opwekken. De fosfatase-activiteit van LET7 is dus zowel noodzakelijk als voldoende om auto-immuniteit te veroorzaken.
Een moleculaire organisator haalt de rem weg
Hoe opent het moleculaire zakmes zich? Het team identificeerde een co-chaperone-eiwit genaamd HOP1 als sleutelorganisator. HOP1 helpt normaal gesproken bij het vouwen en stabiliseren van andere eiwitten door heat-shock-eiwitten. Hier hecht het zich aan het TPR-domein van LET7 en concurreert met de interne contactpunten die LET7 gesloten houden. Structurele modellering en nauwkeurige aminozuurwisselingen in beide partners toonden aan dat dit bindingsvlak fijn is afgesteld: het verzwakken van het contact tussen HOP1 en LET7 vermindert LET7-activatie. Wanneer de MEKK1–MKK1/2–MPK4-keten intact is, is de associatie tussen HOP1 en LET7 laag en blijft LET7 onderdrukt. Wanneer de keten wordt verstoord — door mutaties, door een overschot van een ander scaffold-eiwit, of door een bacterieel effector — intensiveert de HOP1–LET7-interactie en komt de katalytische activiteit van LET7 vrij. Opmerkelijk is dat de humane tegenhangers van HOP1 en PP5 voor de plantparen kunnen substitueren, wat wijst op een geconserveerd activatiemechanisme over de rijken heen.
Een belangrijke schakel doorsnijden en een sensor bewaken
Eens actief richt LET7 zich op een kinase genaamd CRCK3, een enzym dat eerder aan hetzelfde immuunpad werd gekoppeld. CRCK3 komt voor in gefosforyleerde en gede-fosforyleerde vormen, die als twee banden op proteïnegelelektroforese te onderscheiden zijn. In plantencellen en testbuisassays verwijdert actieve LET7 selectief fosfaatgroepen van CRCK3, terwijl inactieve LET7 dat niet doet. Versterking van LET7-activiteit of co-expressie met CRCK3 verhoogt de defosforylering en leidt tot celdood en klassieke immuunmarkers, maar deze effecten worden afgezwakt wanneer HOP1 of de NLR-receptor SUMM2 ontbreekt. Tegelijkertijd ontdekten de auteurs dat zowel LET7 als HOP1, via hun TPR-domeinen, fysiek binden aan SUMM2 en de eiwithoeveelheid daarvan verhogen zonder andere NLR-receptoren algemeen te stabiliseren. Zo helpt hetzelfde module dat fosfaat van CRCK3 verwijdert ook de sensor te onderhouden die dat signaal leest.
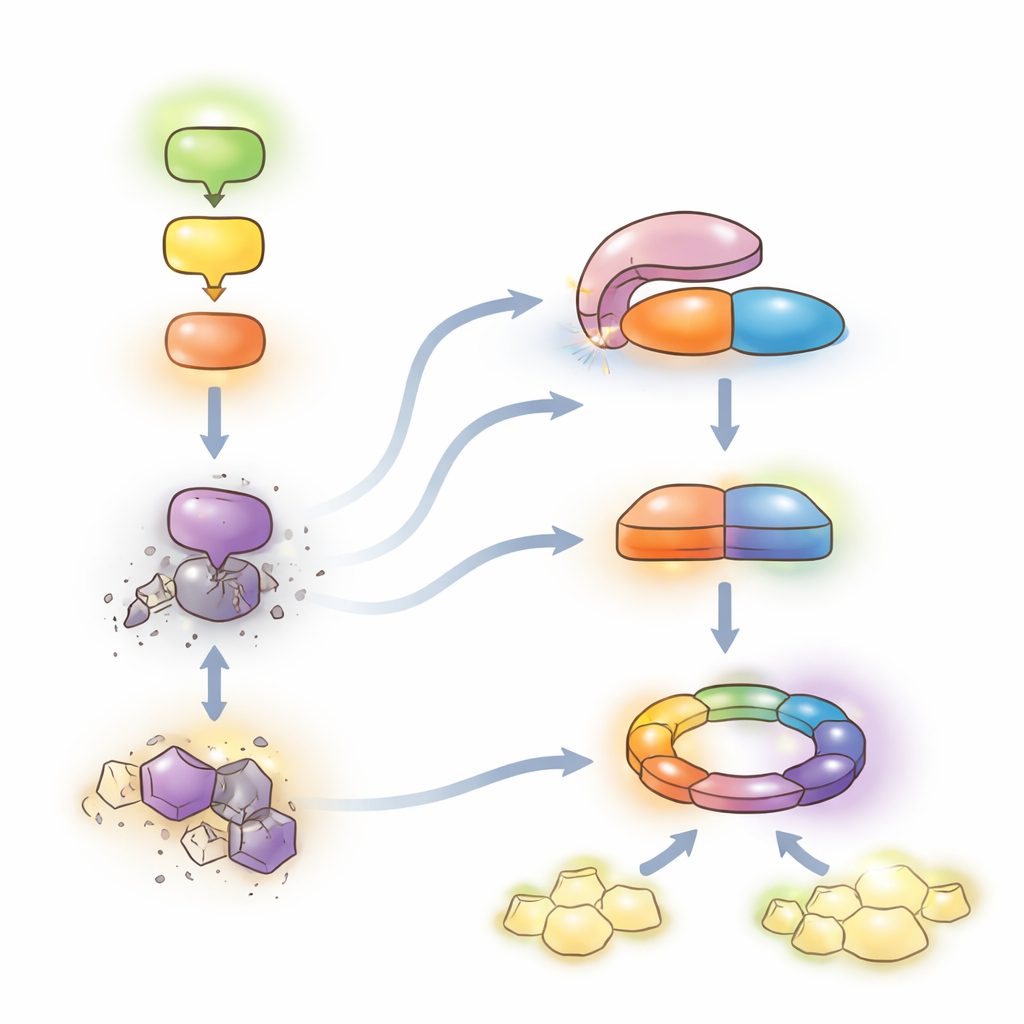
Een delicaat evenwicht tussen bescherming en groei
Gezamenlijk ondersteunen de bevindingen een model waarbij de MEKK1–MKK1/2–MPK4-keten een krachtige tweede linie van verdediging onderdrukt. Wanneer deze keten intact is, blijft LET7 auto-geïnactiveerd en worden SUMM2-niveaus onder controle gehouden, zodat planten voornamelijk op hun dagelijkse alarmsysteem kunnen vertrouwen en kunnen blijven groeien. Wanneer pathogenen de keten verstoren, activeert HOP1 LET7 en ontgrendelt diens fosfatase-activiteit. LET7 defosforyleert vervolgens CRCK3 en stabiliseert samen met HOP1 SUMM2, waardoor het systeem doorslaat naar volledige NLR-gemedieerde immuniteit en lokale celdood — zeer beschermend maar kostbaar voor de groei. Door dit geconserveerde "de-repressie"-mechanisme voor PP5-enzymen bloot te leggen, schetst het werk een moleculaire hefboom die in principe in gewassen aangepast zou kunnen worden om ziekteresistentie te versterken en schadelijke auto-immuniteit te minimaliseren.
Bronvermelding: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
Trefwoorden: plantenimmuniteit, proteïnefosfatase 5, NLR-receptoren, signaaltransductie, Arabidopsis