Clear Sky Science · es
Desrepresión de la fosfatasa de proteínas 5 por el organizador de chaperonas HOP1 activa la inmunidad NLR en plantas
Cómo las plantas deciden entre crecimiento y autodefensa
Las plantas se enfrentan constantemente a posibles invasores —bacterias, hongos y virus—, pero no pueden abandonar el crecimiento para combatir cada amenaza. Este artículo revela cómo un pequeño sistema molecular de «freno y disparador» en la planta modelo Arabidopsis ayuda a decidir cuándo desencadenar una reacción inmune extrema que puede salvar a la planta pero también frenar su crecimiento. Comprender este interruptor ofrece información sobre cómo se podrían criar o diseñar cultivos resistentes a enfermedades sin pagar un precio excesivo en rendimiento.
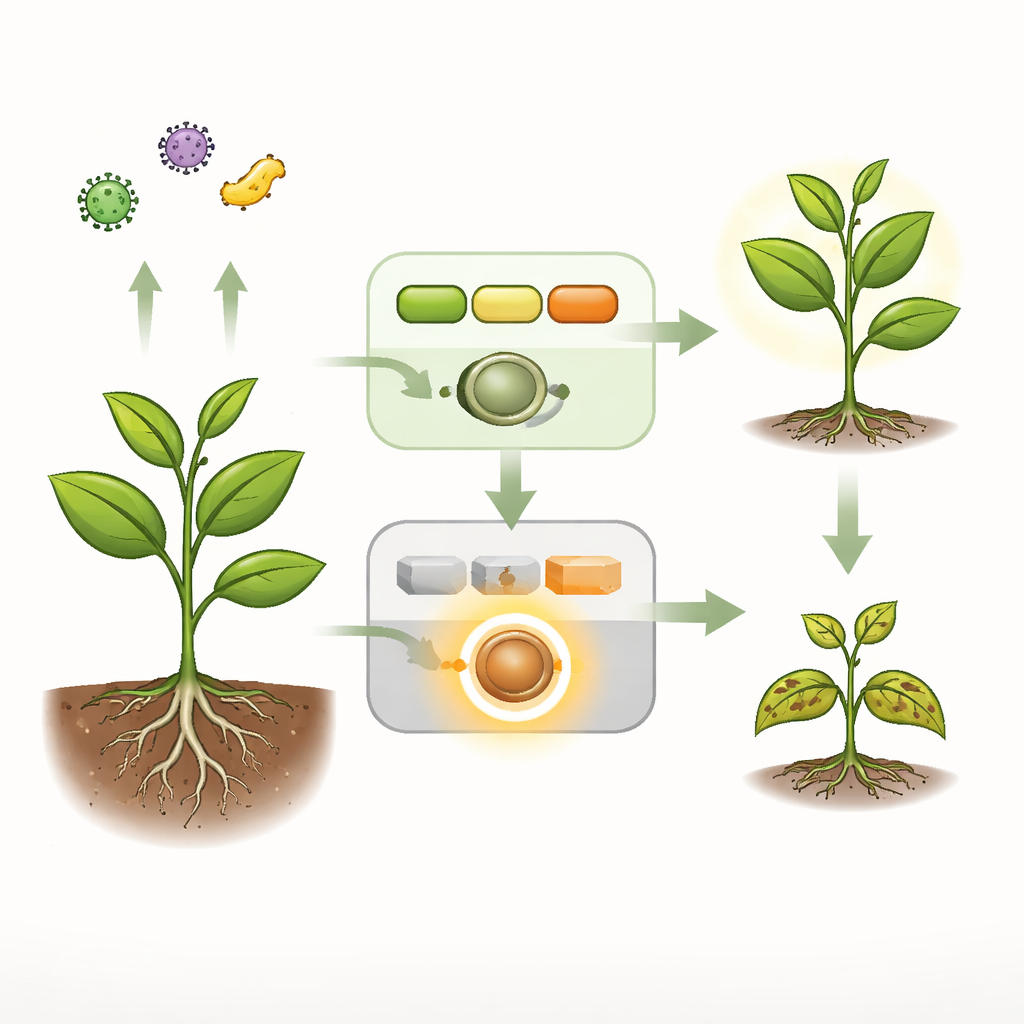
Alarmas cotidianas frente a sirenas de emergencia
Las plantas gestionan dos sistemas de seguridad principales. El primero es una alarma rápida y amplia que detecta huellas microbianas generales en la superficie celular y activa respuestas protectoras. Una segunda capa, más drástica, depende de centinelas internos llamados receptores NLR que pueden desencadenar defensas potentes, a menudo letales, en las células donde se detectan patógenos. En Arabidopsis sana, una cadena de señalización de tres enzimas —colectivamente llamada la cascada MEKK1–MKK1/2–MPK4— transmite la primera alarma y, al mismo tiempo, mantiene en silencio a un receptor NLR específico, denominado SUMM2, para que no se active sin motivo. Cuando esta cadena se rompe por una mutación o por una proteína efectora bacteriana, las plantas muestran muerte celular espontánea, alta actividad de genes de defensa y enanismo severo, todos signos de una inmunidad descontrolada.
Despierta una enzima oculta
Los autores descubrieron que una enzima fosfatasa llamada LET7, una versión vegetal de la proteína conservada PP5, ocupa el centro de esta respuesta descontrolada. Por sí sola, LET7 está diseñada como una navaja plegable: una región (dominio TPR) se pliega sobre la región catalítica y la mantiene en gran medida apagada. Cribados genéticos mostraron que las plantas sin LET7 ya no sufrían los síntomas letales causados cuando la cadena de señalización upstream está silenciada, situando a LET7 aguas abajo de esa cascada. Pruebas bioquímicas revelaron que cuando la región catalítica de LET7 se libera o se vuelve hiperactiva por mutaciones específicas, las plantas desarrollan respuestas defensivas fuertes y muerte celular, mientras que una versión catalíticamente muerta no puede desencadenar estos efectos. Así, la actividad fosfatasa de LET7 es a la vez necesaria y suficiente para impulsar la autoinmunidad.
Un organizador molecular libera el freno
¿Cómo se abre la navaja molecular? El equipo identificó una proteína co‑chaperona llamada HOP1 como organizador clave. HOP1 normalmente ayuda a las proteínas de choque térmico a plegar y estabilizar otras proteínas. Aquí, se une a la región TPR de LET7 y compite con el contacto interno que mantiene a LET7 cerrada. La modelización estructural y cambios precisos en aminoácidos en ambos socios mostraron que esta superficie de unión está finamente ajustada: debilitar el contacto entre HOP1 y LET7 reduce la activación de LET7. Cuando la cadena MEKK1–MKK1/2–MPK4 está intacta, la asociación entre HOP1 y LET7 es baja y LET7 permanece reprimida. Cuando la cadena se ve interrumpida —por mutaciones, por sobreabundancia de otra proteína andamio, o por un efector bacteriano— la interacción HOP1–LET7 se intensifica, desatando la actividad catalítica de LET7. De manera notable, los contrapartes humanas de HOP1 y PP5 pueden substituir al par vegetal, lo que apunta a un mecanismo de activación conservado entre los reinos.
Cortar un interruptor clave y proteger un sensor
Una vez activa, LET7 tiene como blanco a una quinasa llamada CRCK3, una enzima previamente vinculada a la misma vía inmune. CRCK3 existe en formas fosforilada y desfosforilada, que se distinguen como dos bandas en geles de proteínas. En células vegetales y ensayos in vitro, LET7 activa elimina selectivamente marcas de fosfato de CRCK3, mientras que LET7 inactiva no lo hace. Potenciar la actividad de LET7 o coexpresarla con CRCK3 aumenta la desfosforilación y conduce a muerte celular y marcadores clásicos de la respuesta inmune, pero estos efectos se atenúan cuando falta HOP1 o el receptor NLR SUMM2. Paralelamente, los autores encontraron que tanto LET7 como HOP1, a través de sus regiones TPR, se unen físicamente a SUMM2 y aumentan su abundancia proteica sin estabilizar de forma general otros receptores NLR. Así, el mismo módulo que elimina el fosfato de CRCK3 también ayuda a mantener el sensor que detecta esa señal.
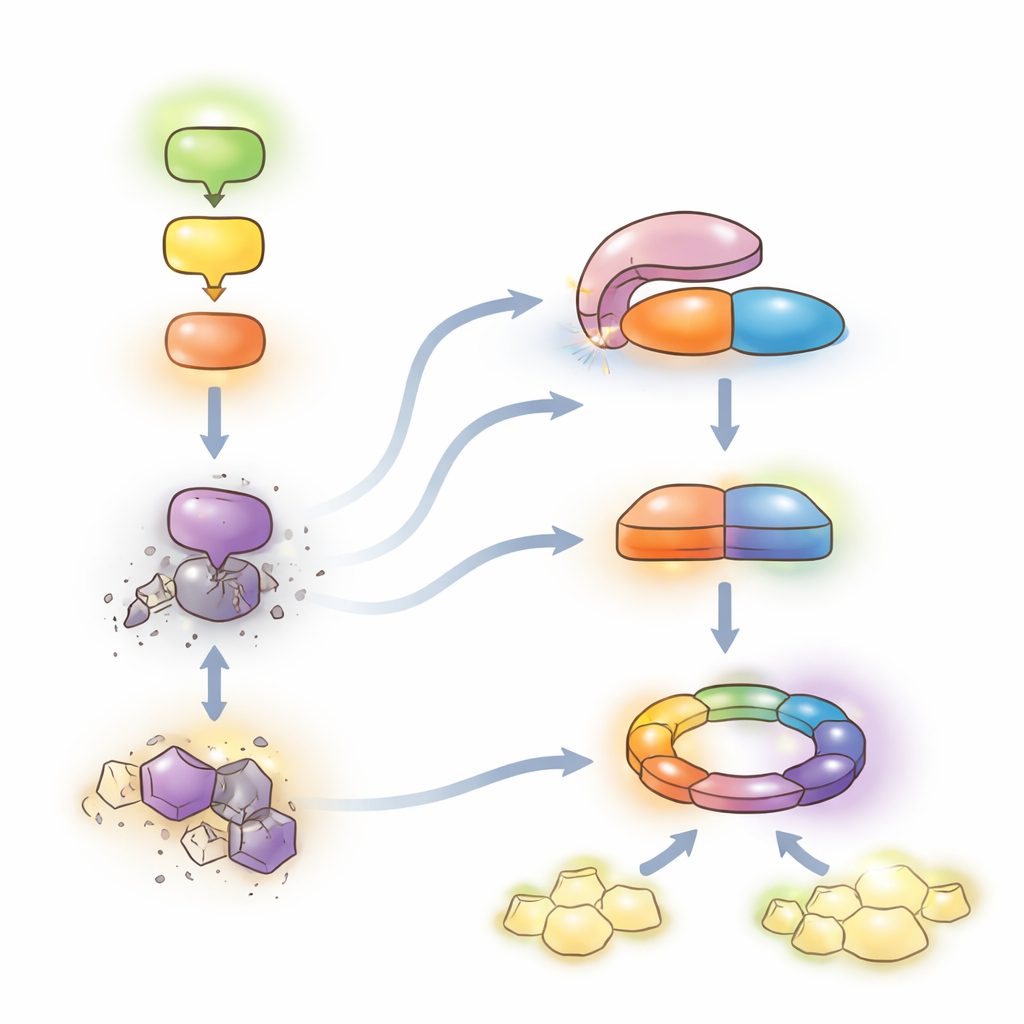
Un equilibrio delicado entre protección y crecimiento
En conjunto, los hallazgos respaldan un modelo en el que la cadena MEKK1–MKK1/2–MPK4 restringe una poderosa defensa de segunda línea. Cuando esta cadena está intacta, LET7 permanece autoinhibida y los niveles de SUMM2 se mantienen controlados, lo que permite a las plantas confiar principalmente en su sistema de alarma cotidiano mientras continúan creciendo. Cuando los patógenos interrumpen la cadena, HOP1 activa LET7, desbloqueando su actividad fosfatasa. LET7 desfosforila entonces a CRCK3 y, junto con HOP1, estabiliza SUMM2, inclinando el sistema hacia la inmunidad mediada por NLR y la muerte celular local —altamente protectora pero costosa para el crecimiento. Al revelar este mecanismo conservado de «desrepresión» para las enzimas PP5, el trabajo describe una palanca molecular que podría, en principio, ajustarse en cultivos para reforzar la resistencia a enfermedades minimizando la autoinmunidad perjudicial.
Cita: Yan, Y., Zhao, Z., Yeo, IC. et al. De-repression of protein phosphatase 5 by the chaperone organizer HOP1 activates plant NLR immunity. Nat. Plants 12, 802–817 (2026). https://doi.org/10.1038/s41477-026-02253-4
Palabras clave: inmunidad vegetal, fosfatasa de proteínas 5, receptores NLR, transducción de señales, Arabidopsis