Clear Sky Science · zh
MeCP2 通过非经典、依赖 AR 的 Mef2c 调控,控制由母体高雄激素引起的皮层缺陷和行为改变
这项研究对家庭为何重要
许多影响学习、社交技能和行为的疾病在男孩中比女孩更常见,但这种性别差异的原因仍不清楚。本研究使用小鼠模型探讨孕期高水平男性激素如何微妙地重塑雄性后代的脑发育,以及一种广为人知的脑内蛋白 MeCP2 如何将这些激素信号转化为持久的脑结构和行为改变。
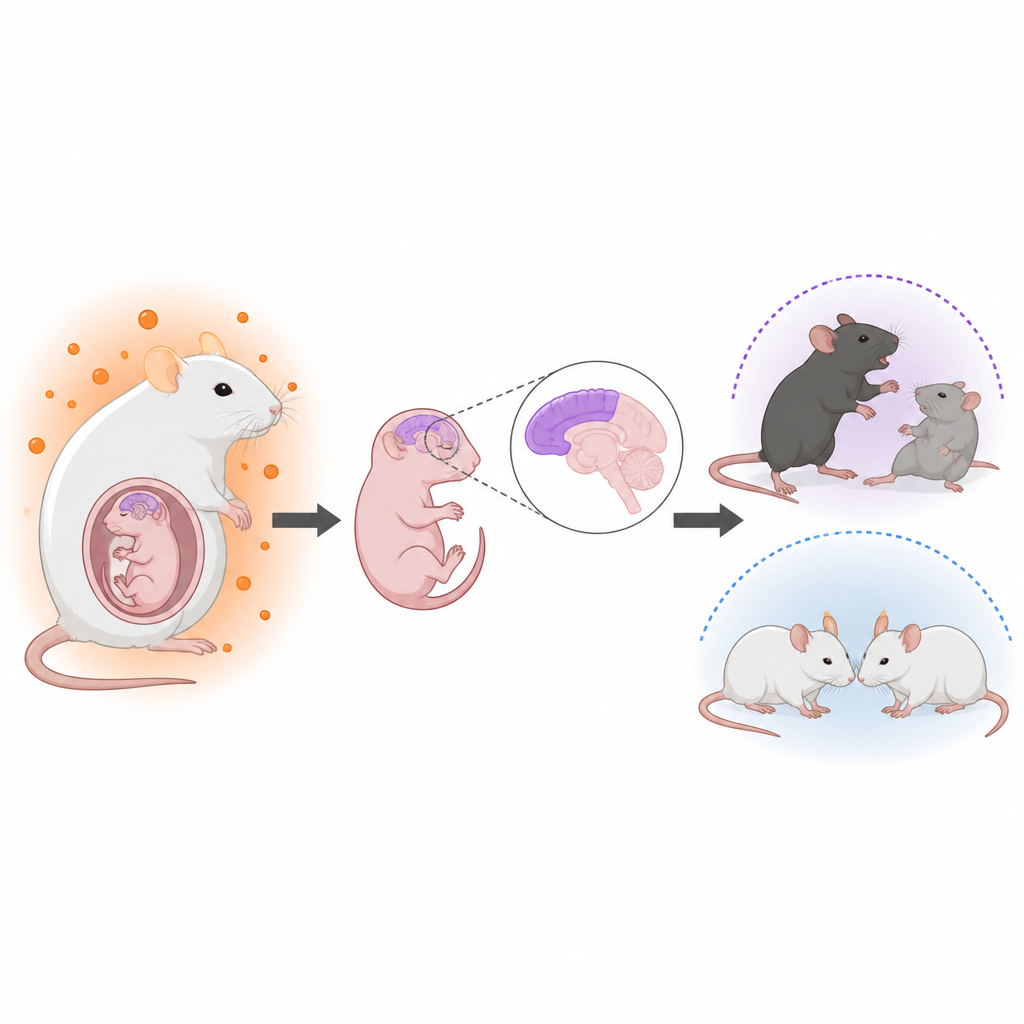
产前激素与成年大脑健康
医生长期观察到宫内雄激素升高与诸如自闭症等神经发育状况风险增加有关。例如,多囊卵巢综合征的女性常伴随较高的雄激素水平,其子女自闭症风险略有上升。然而,这些激素如何作用于胎儿大脑,以及为什么儿子似乎比女儿更易受影响,尚不清楚。作者构建了一个现实的母体高雄激素小鼠模型,随后追踪后代的大脑发育和行为变化。
团队如何模拟激素暴露
研究者用一种抑制芳香化酶的药物处理怀孕小鼠,该酶通常将睾酮转换为雌激素。此举提高了母体、羊水和胎儿脑中的睾酮水平,但并未改变总体妊娠结局或出生体重。通过遗传标记和显微镜观察,他们聚焦于大脑外层负责思考与社交行为的大脑皮层。在雄性后代中(女性仅表现轻微),他们发现神经干/祖细胞更早并更多地分化为神经元,而干细胞库和某些晚期细胞类型(如星形胶质细胞)减少。尽管总体脑体积未变,皮层神经元的正常层次排列明显变得不那么有序。
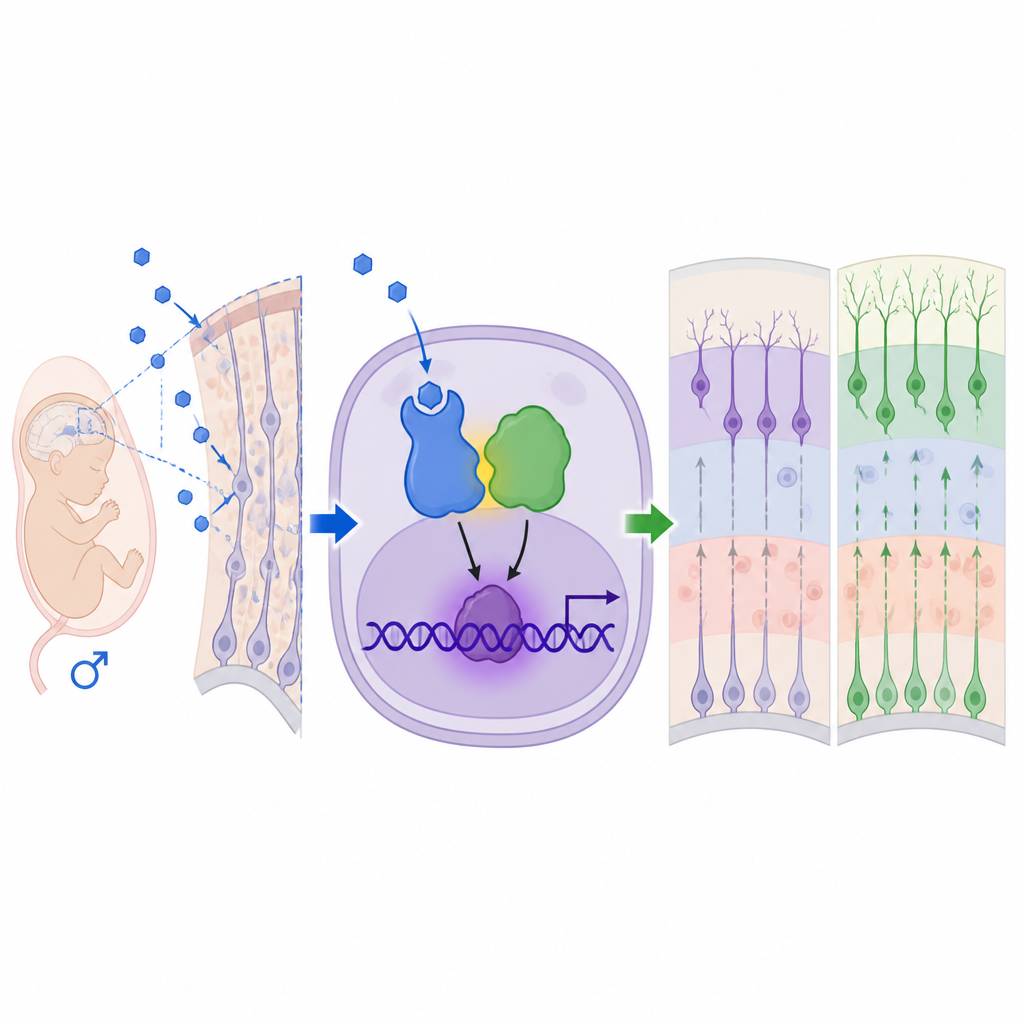
从改变的皮层到行为差异
成年后,来自高雄激素母体的雄性后代在行为上表现出若干与自闭症常见特征相似的差异。在社交测试中,这些雄鼠与其他鼠互动的时间减少,对新社交对象的兴趣也降低,而其运动水平保持正常。它们还表现出更多重复性行为,如掩埋更多弹珠,并在开放场与高架十字迷宫测试中表现出更强的焦虑迹象。在相同条件下饲养并在出生后交叉养育到对照母鼠的雌性后代,行为改变要轻得多或没有,凸显出雄性易感性的偏向。
发育中细胞内的非典型通路
为了解雄激素如何产生这些效应,团队聚焦于感知激素的雄激素受体(AR)。他们发现在雄性胎儿皮层中 AR 水平升高并更多定位于细胞核,用药物氟他胺阻断该受体可以逆转过度的神经发生及大部分行为改变。基因表达分析指出转录因子 MEF2C(已与神经发育障碍相关)是关键下游靶点。令人意外的是,AR 并非单独通过其典型的 DNA 结合位点发挥作用,而是与 X 染色体上的 MeCP2 蛋白物理结合——MeCP2 因 Rett 综合征和 MeCP2 重复综合征而广为人知。AR 与 MeCP2 形成激活复合体,结合于 Mef2c 调控区中 MeCP2 识别位点,上调 MEF2C 水平并促使神经干细胞向神经元分化。
当 MeCP2 本身增加时会怎样
作者随后使用携带 MeCP2 额外拷贝的小鼠模型,这些小鼠此前已显示皮层神经发生增加和类似自闭症的行为。他们发现这些 MeCP2 重复的雄鼠即使在没有额外产前雄激素的情况下也具有升高的 MEF2C 水平和类似的皮层改变。在这些小鼠中降低 Mef2c 表达或阻断雄激素受体可以恢复皮层层次结构并缓解许多社交、重复性和焦虑样行为。这表明过量的 MeCP2 可以启动相同的激素敏感通路,在存在雄激素信号时放大雄性特异的风险。
这项工作如何改变我们对性别差异的看法
总体而言,该研究揭示了一条先前未被认识的途径,说明母体雄激素暴露如何塑造雄性胎儿皮层及其后续行为。雄激素受体并非仅通过经典靶点作用,而是可以利用 MeCP2 激活 MEF2C,从而改变神经干细胞命运的平衡并微妙重接皮层回路。由于 MeCP2 位于 X 染色体上并已与若干人类神经发育综合征相关联,这一对激素敏感的合作关系为为什么男孩更易患某些脑源性疾病提供了具体的分子解释,同时也表明基因与产前激素环境需共同考虑。
引用: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
关键词: 产前雄激素, MeCP2, 皮层发育, MEF2C, 自闭症风险