Clear Sky Science · it
MeCP2 governa i difetti corticali e i cambiamenti comportamentali indotti da iperandrogenismo materno tramite la regolazione non canonica dipendente da AR di Mef2c
Perché questa ricerca conta per le famiglie
Molte condizioni che influenzano l'apprendimento, le abilità sociali e il comportamento sono più comuni nei maschi che nelle femmine, ma le ragioni di questa differenza sessuale restano poco chiare. Questo studio usa topi per esplorare come alti livelli di ormoni maschili durante la gravidanza possano rimodellare sottilmente il cervello in sviluppo dei nati maschi, e come una proteina cerebrale nota, MeCP2, aiuti a tradurre quei segnali ormonali in cambiamenti duraturi nella struttura cerebrale e nel comportamento.
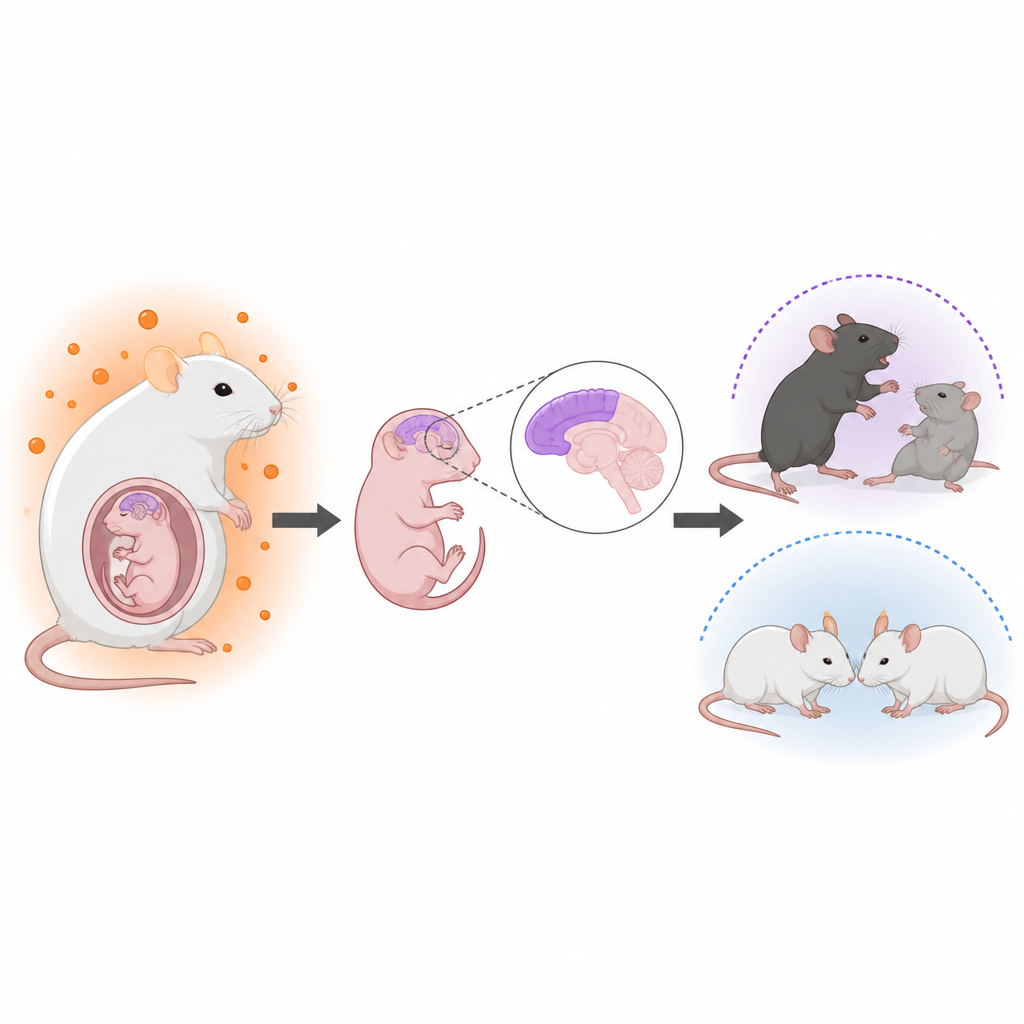
Ormoni prima della nascita e salute cerebrale futura
I medici hanno da tempo osservato collegamenti tra androgeni elevati nell'utero e una maggiore probabilità di condizioni neuroevolutive come l'autismo. Per esempio, le donne con sindrome dell'ovaio policistico spesso hanno livelli più alti di androgeni e i loro figli mostrano un rischio di autismo leggermente aumentato. Tuttavia non era chiaro come questi ormoni agissero sul cervello fetale o perché i figli maschi sembrino più colpiti rispetto alle figlie. Gli autori hanno quindi costruito un modello murino realistico di iperandrogenismo materno e hanno poi seguito lo sviluppo cerebrale e il comportamento della prole.
Come il team ha modellato l'esposizione agli ormoni
I ricercatori hanno trattato le topine gravide con un farmaco che blocca l'aromatasi, l'enzima che normalmente converte il testosterone in estrogeni. Questo ha aumentato i livelli di testosterone nelle madri, nel liquido amniotico e nei cervelli fetali, senza modificare gli esiti generali della gravidanza o il peso alla nascita. Usando marcature genetiche e microscopia, si sono concentrati sulla corteccia cerebrale, lo strato esterno del cervello che supporta il pensiero e il comportamento sociale. Nella prole maschile, ma solo lievemente nelle femmine, hanno riscontrato che le cellule staminali e progenitrici neurali venivano spinte a generare neuroni prima e in maggiore numero, mentre il pool di cellule staminali e alcuni tipi cellulari tardivi come gli astrociti risultavano ridotti. L'ordinamento a strati delle cellule corticali è diventato visibilmente meno regolare, pur senza cambiamenti nelle dimensioni complessive del cervello.
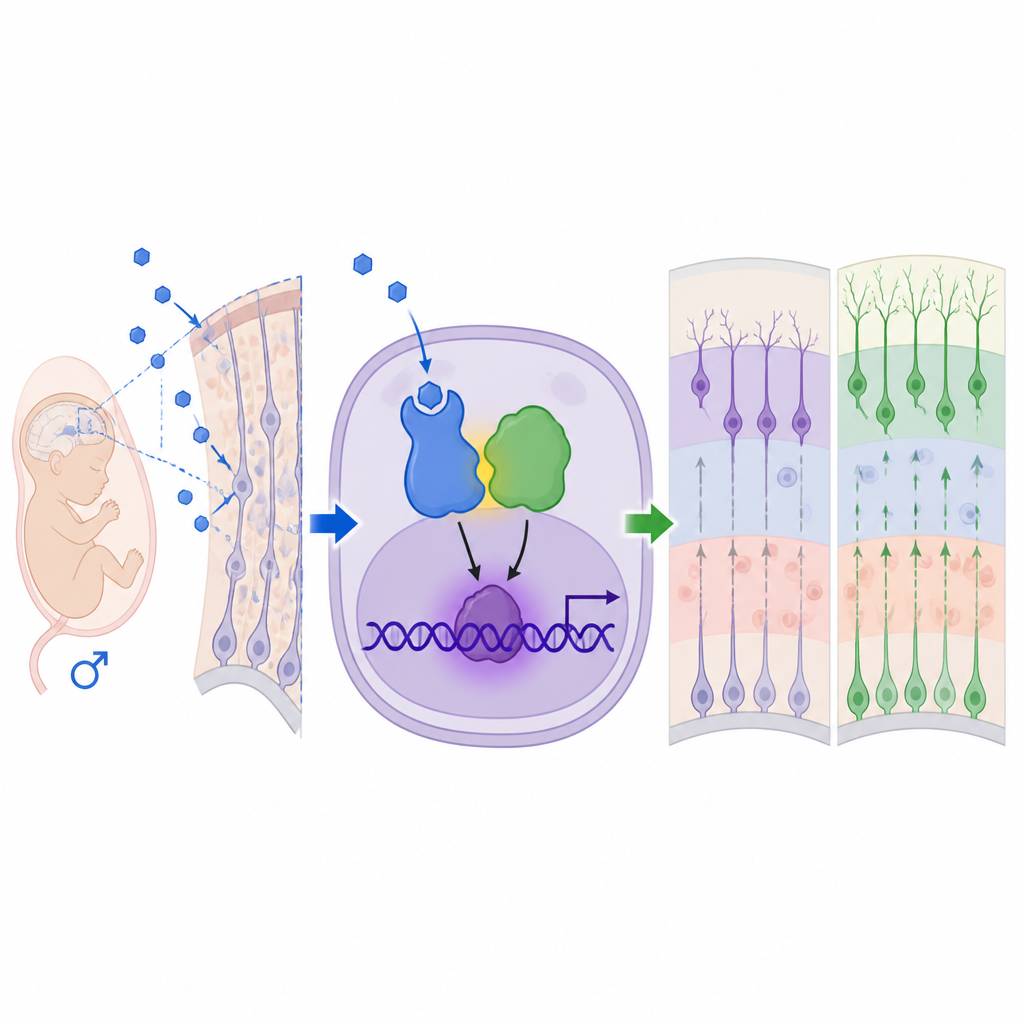
Dalla corteccia alterata al comportamento modificato
Da adulti, i maschi nati da madri iperandrogeniche hanno mostrato differenze comportamentali che rispecchiano diverse caratteristiche osservate spesso nell'autismo. Nei test sociali, questi maschi trascorrevano meno tempo a interagire con altri topi e mostravano meno interesse per nuovi partner sociali, mentre i loro livelli di movimento restavano normali. Presentavano inoltre comportamenti ripetitivi più frequenti, come seppellire più biglie, e segni più forti di ansia nei test dell'open field e dell'elevated plus maze. Le femmine della stessa condizione, allevate nelle stesse circostanze e affiancate a madri di controllo dopo la nascita, hanno mostrato cambiamenti comportamentali molto più lievi o assenti, evidenziando una vulnerabilità con bias maschile.
Una via non standard nelle cellule cerebrali in sviluppo
Per capire come gli androgeni esercitino questi effetti, il team si è focalizzato sui recettori degli androgeni, le proteine che percepiscono questi ormoni. Hanno riscontrato livelli maggiori e localizzazione nucleare del recettore degli androgeni nella corteccia fetale maschile, e il blocco di questo recettore con il farmaco flutamide ha invertito l'eccesso di neurogenesi e la maggior parte dei cambiamenti comportamentali. Le analisi dell'espressione genica hanno indicato MEF2C, un fattore di trascrizione già collegato a disturbi dello sviluppo neurologico, come principale bersaglio a valle. Sorprendentemente, il recettore degli androgeni non agiva da solo né attraverso i suoi consueti siti di legame al DNA. Piuttosto, si è associato fisicamente a MeCP2, una proteina codificata da un gene sul cromosoma X nota per la sindrome di Rett e la sindrome da duplicazione di MeCP2. Insieme, recettore degli androgeni e MeCP2 hanno formato un complesso attivatore che si legava a un sito riconosciuto da MeCP2 nella regione regolatoria di Mef2c, aumentando i livelli di MEF2C e spingendo le cellule staminali neurali verso la destinazione neuronale.
Cosa succede quando MeCP2 è esso stesso aumentato
Gli autori si sono poi rivolti a un modello murino con una copia in più di MeCP2, precedentemente dimostrato mostrare una neurogenesi corticale aumentata e comportamenti simili all'autismo. Hanno scoperto che anche questi maschi con duplicazione di MeCP2 avevano MEF2C elevato e cambiamenti corticali simili, anche in assenza di androgeni prenatali aggiuntivi. Ridurre Mef2c o bloccare i recettori degli androgeni in questi topi ha normalizzato la stratificazione corticale e attenuato molte delle manifestazioni sociali, ripetitive e ansiose. Questo suggerisce che un eccesso di MeCP2 può attivare la stessa via sensibile agli ormoni, amplificando il rischio specifico per i maschi quando sono presenti segnali androgenici.
Come questo lavoro cambia la nostra visione delle differenze fra i sessi
Nel complesso, lo studio rivela una via finora non riconosciuta attraverso la quale l'esposizione materna agli androgeni può plasmare la corteccia fetale maschile e il comportamento successivo. Invece di agire solo tramite i suoi bersagli classici, il recettore degli androgeni può sfruttare MeCP2 per attivare MEF2C, alterando così l'equilibrio dei destini delle cellule staminali neurali e rimodellando sottilmente i circuiti corticali. Poiché MeCP2 è sul cromosoma X ed è già implicato in diverse sindromi neuroevolutive umane, questa partnership sensibile agli ormoni offre una spiegazione molecolare concreta del perché i ragazzi possano essere più soggetti ad alcune condizioni cerebrali, suggerendo al contempo che è necessario considerare insieme fattori genetici e ambienti ormonali prenatali.
Citazione: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
Parole chiave: androgeni prenatali, MeCP2, sviluppo corticale, MEF2C, rischio di autismo