Clear Sky Science · pl
MeCP2 kontroluje kortykalne defekty i zmiany zachowania wywołane matczyną hiperandrogenizacją poprzez niekanoniczną, zależną od AR regulację Mef2c
Dlaczego te badania są istotne dla rodzin
Wiele zaburzeń wpływających na uczenie się, umiejętności społeczne i zachowanie występuje częściej u chłopców niż u dziewcząt, lecz przyczyny tej różnicy płciowej wciąż nie są jasne. To badanie wykorzystuje model myszy, aby zbadać, jak wysokie poziomy męskich hormonów w czasie ciąży mogą subtelnie przekształcać rozwijający się mózg męskiego potomstwa oraz jak znany białkowy regulator mózgu, MeCP2, pomaga przekładać te sygnały hormonalne na trwałe zmiany w strukturze mózgu i zachowaniu.
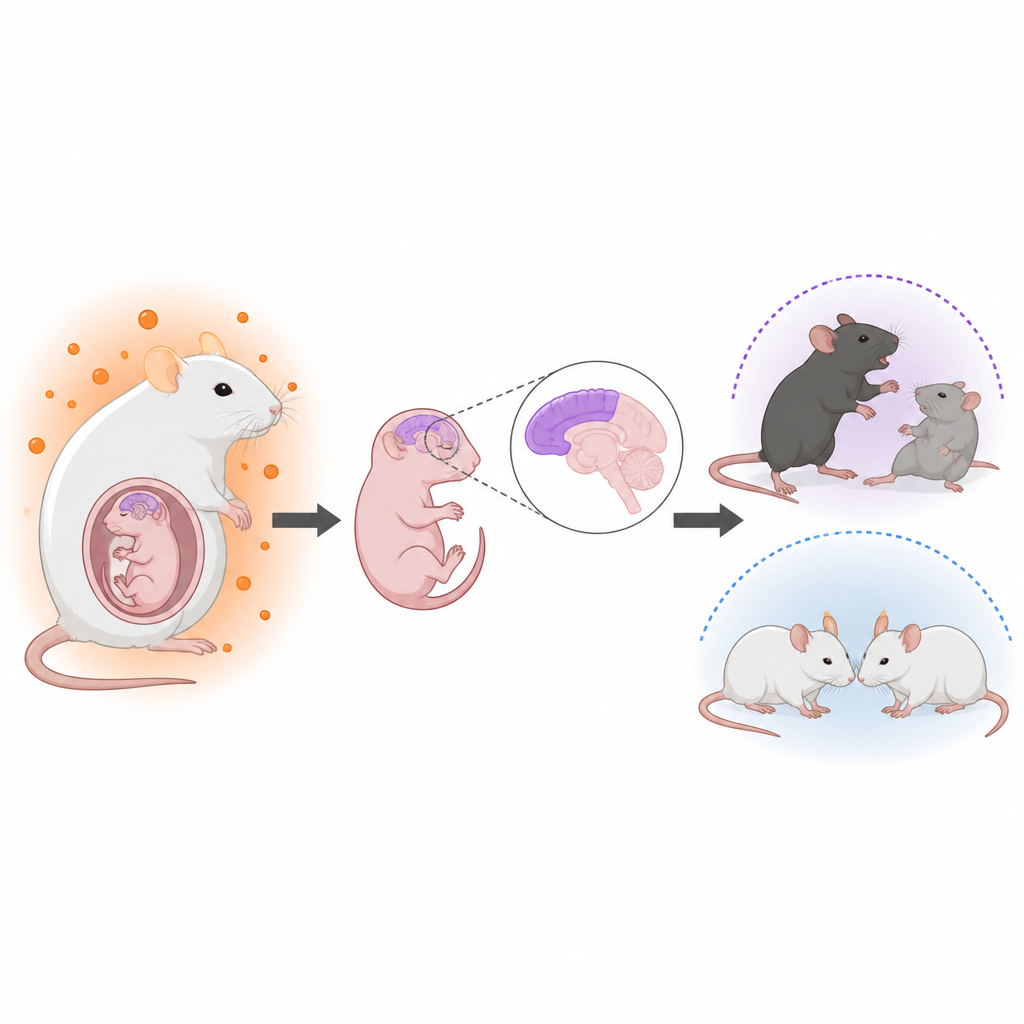
Hormony przed narodzinami a późniejsze zdrowie mózgu
Lekarze od dawna obserwują związki między podwyższonymi męskimi hormonami w łonie matki a wyższym prawdopodobieństwem wystąpienia zaburzeń neurorozwojowych, takich jak autyzm. Na przykład kobiety z zespołem policystycznych jajników mają często wyższe poziomy androgenów, a ich dzieci wykazują nieco zwiększone ryzyko autyzmu. Nie było jednak jasne, jak te hormony działają na mózg płodowy ani dlaczego synowie wydają się bardziej dotknięci niż córki. Autorzy postanowili opracować realistyczny model myszy matczynej hiperandrogenizacji, a następnie śledzić rozwój mózgu i zachowanie potomstwa.
Jak zespół odtworzył ekspozycję hormonalną
Naukowcy lecili ciężarne myszy lekiem blokującym aromatazę — enzym, który normalnie przekształca testosteron w estrogen. Spowodowało to podwyższenie poziomu testosteronu u matek, w płynie owodniowym otaczającym płody oraz w mózgach płodów, bez zmiany ogólnych wyników ciąży czy masy urodzeniowej. Dzięki znakowaniu genetycznemu i mikroskopii skupili się na korze mózgowej, zewnętrznej warstwie mózgu odpowiedzialnej za myślenie i zachowania społeczne. U męskich potomków, a jedynie słabo u samic, zaobserwowano, że komórki macierzyste i progenitorowe były przesunięte w kierunku wcześniejszego i większego wytwarzania neuronów, podczas gdy pula komórek macierzystych i niektóre późniejsze typy komórek, jak astrocyty, została zmniejszona. Normalne, warstwowe ułożenie neuronów kory stało się wyraźnie mniej uporządkowane, mimo że całkowity rozmiar mózgu się nie zmienił.
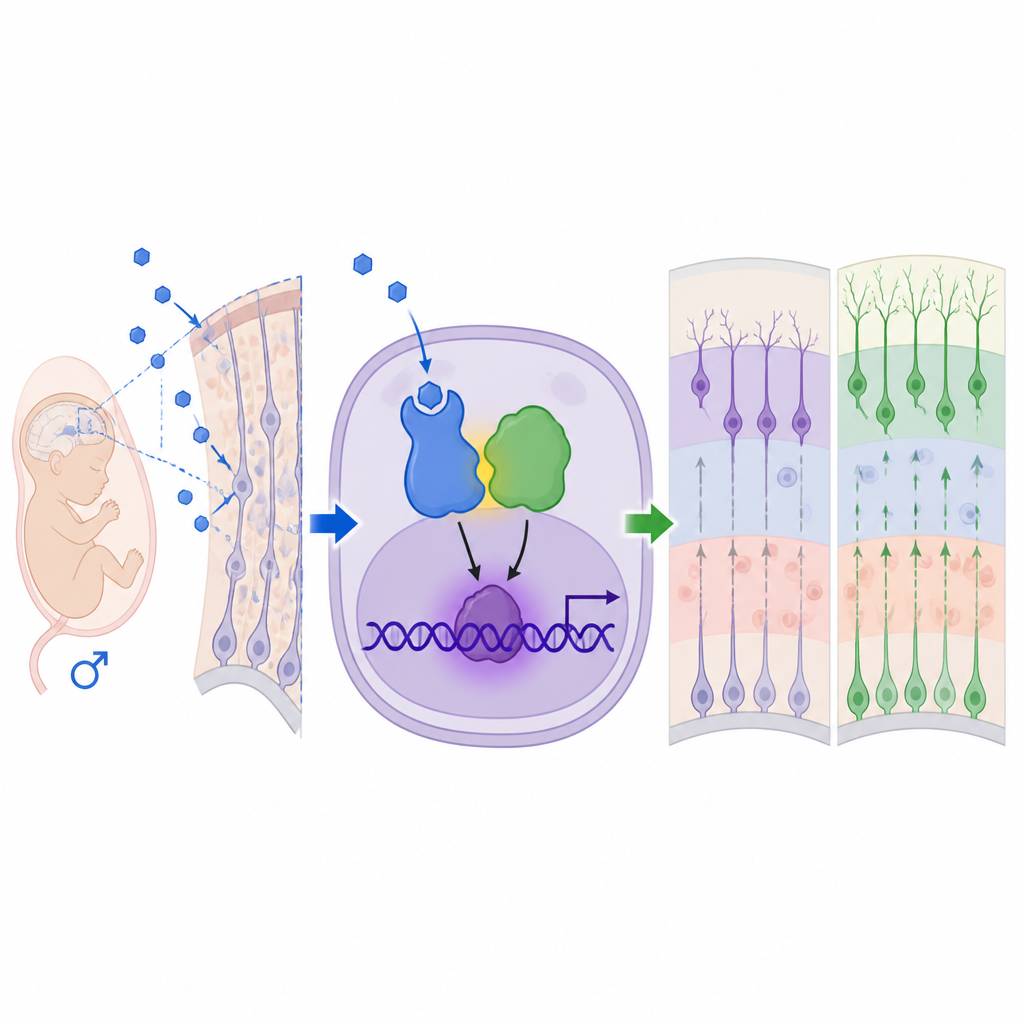
Od zmienionej kory do zmienionego zachowania
Jako dorośli, męscy potomkowie pochodzący od matek z hiperandrogenizmem wykazywali zmiany w zachowaniu przypominające cechy często obserwowane w autyzmie. W testach społecznych ci samcy spędzali mniej czasu na interakcjach z innymi myszami i wykazywali mniejsze zainteresowanie nowymi partnerami społecznymi, podczas gdy poziom ich aktywności ruchowej pozostawał normalny. Wykazywali też więcej powtarzalnych zachowań, takich jak zakopywanie większej liczby kuleczek, oraz silniejsze objawy lęku w testach otwartego pola i wspinaczki z podwyższeniami (elevated plus maze). Samice wychowane w tych samych warunkach i przeszczepione po porodzie do kontrolnych matek wykazywały znacznie łagodniejsze lub brak takich zmian behawioralnych, co podkreśla męską predyspozycję do wrażliwości.
Niekonwencjonalna ścieżka wewnątrz rozwijających się komórek mózgowych
Aby zrozumieć, w jaki sposób androgeny wywołują te efekty, zespół przyjrzał się receptorom androgenowym — białkom wykrywającym te hormony. Stwierdzono wyższe poziomy i jądrową lokalizację receptora androgenowego w męskiej korze płodowej, a zablokowanie tego receptora lekiem flutamidem odwracało nadmierną neurogenezę i większość zmian behawioralnych. Analizy ekspresji genów wskazały na MEF2C, czynnik transkrypcyjny już powiązany z zaburzeniami neurorozwojowymi, jako kluczowy docelowy element. Co zaskakujące, receptor androgenowy nie działał samodzielnie ani przez swoje klasyczne miejsca wiązania z DNA. Zamiast tego fizycznie współdziałał z MeCP2 — białkiem kodowanym przez gen na chromosomie X, najlepiej znanym z zespołu Rett i zespołu duplikacji MeCP2. Razem receptor androgenowy i MeCP2 tworzyły kompleks aktywacyjny, który wiązał się w regionie regulacyjnym Mef2c w miejscu rozpoznawanym przez MeCP2, zwiększając poziomy MEF2C i kierując komórki macierzyste nerwowe w stronę losu neuronalnego.
Co się dzieje, gdy sam MeCP2 jest zwiększony
Autorzy sięgnęli następnie po model myszy niosący dodatkową kopię MeCP2, który wcześniej wykazywał zwiększoną neurogenezę korową i zachowania przypominające autyzm. Odkryli, że samce z duplikacją MeCP2 także miały podwyższone MEF2C i podobne zmiany korowe, nawet bez dodatkowych prenatalnych androgenów. Obniżenie ekspresji Mef2c lub zablokowanie receptorów androgenowych u tych myszy normalizowało warstwowanie kory i łagodziło wiele zachowań społecznych, powtarzalnych i związanych z lękiem. Sugeruje to, że nadmiar MeCP2 może uruchomić tę samą wrażliwą na hormony ścieżkę, wzmacniając męskie ryzyko w obecności sygnałów androgenowych.
Jak ta praca zmienia nasze spojrzenie na różnice płciowe
Podsumowując, badanie ujawnia wcześniej nieznaną drogę, dzięki której matczyna ekspozycja na androgeny może kształtować męską korę płodową i późniejsze zachowanie. Zamiast działać jedynie przez klasyczne cele, receptor androgenowy potrafi wykorzystać MeCP2 do uruchomienia MEF2C, przesuwając równowagę losów komórek macierzystych nerwowych i subtelnie przebudowując obwody korowe. Ponieważ MeCP2 znajduje się na chromosomie X i jest już powiązane z kilkoma ludzkimi zespołami neurorozwojowymi, ta wrażliwa na hormony współpraca daje konkretną molekularną podstawę wyjaśniającą, dlaczego chłopcy mogą być bardziej podatni na pewne zaburzenia o podłożu mózgowym, jednocześnie sugerując, że zarówno geny, jak i prenatalne środowisko hormonalne należy rozważać razem.
Cytowanie: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
Słowa kluczowe: prenatalne androgeny, MeCP2, rozwój kory, MEF2C, ryzyko autyzmu