Clear Sky Science · ja
MeCP2は非標準的なAR依存的Mef2c制御を介して母体高アンドロゲン症による大脳皮質欠損と行動変化を支配する
この研究が家族にとって重要な理由
学習や社会性、行動に関わる多くの状態は男子に多く見られますが、この性差の理由はまだ明確ではありません。本研究はマウスを用い、妊娠中の高い男性ホルモンが雄の子の発達中の脳をどのように微妙に再構築するか、そしてよく知られた脳タンパク質MeCP2がこれらのホルモン信号を長期的な脳の構造と行動の変化にどのように翻訳するかを探ります。
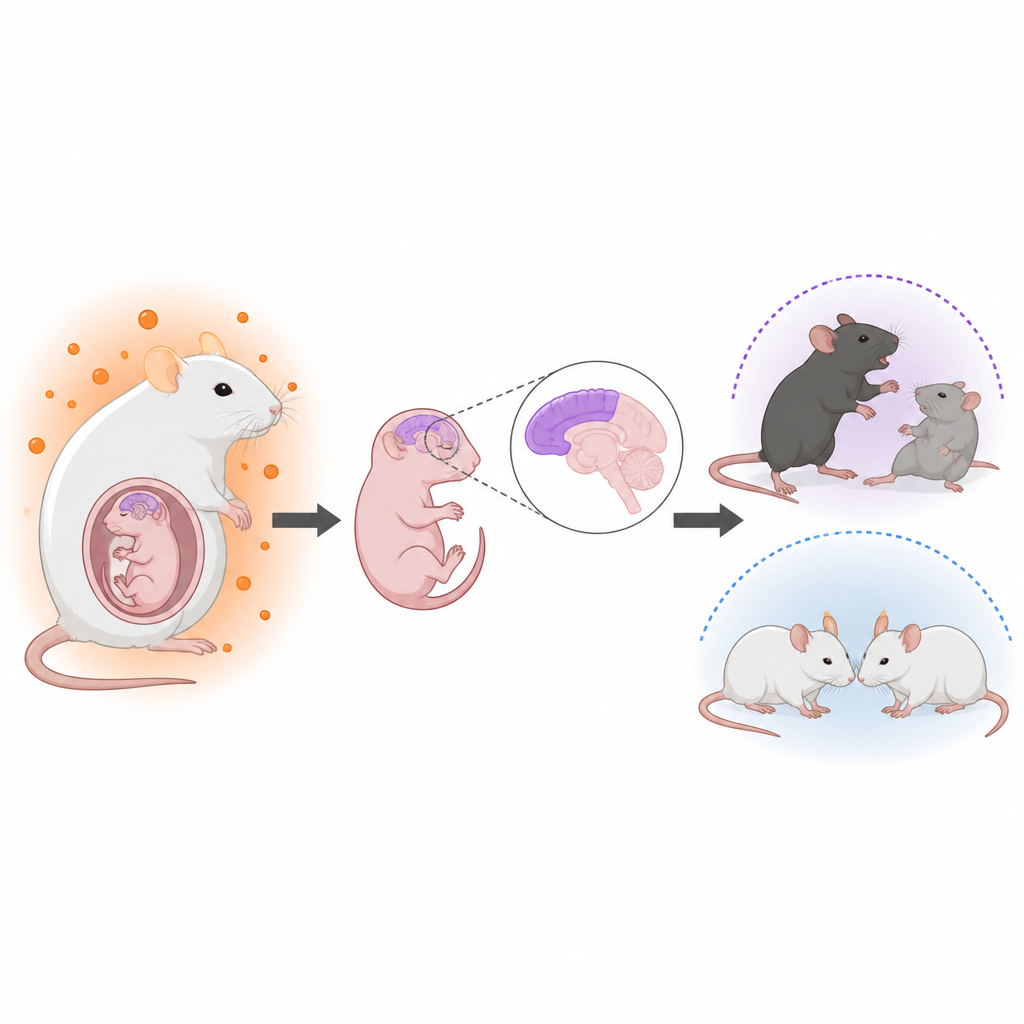
出生前のホルモンとその後の脳の健康
医師たちは以前から、胎内での高い男性ホルモンと自閉症などの神経発達障害の発症率上昇との関連を注目してきました。例えば、多嚢胞性卵巣症候群の女性はしばしばアンドロゲンが高く、その子どもに自閉症リスクがやや高いことが示されています。しかし、これらのホルモンが胎児脳でどのように作用するのか、なぜ息子が娘より影響を受けやすいのかは不明でした。著者らは現実的な母体高アンドロゲン症のマウスモデルを構築し、子孫の脳発達と行動を追跡することを目指しました。
研究チームのホルモン曝露モデル
研究者らは妊娠マウスに、通常テストステロンをエストロゲンに変換する酵素であるアロマターゼを阻害する薬剤を投与しました。これにより母体、羊水、および胎児脳内のテストステロン濃度が上昇しましたが、妊娠の全体的な結果や出生体重は変わりませんでした。遺伝子マーキングと顕微鏡観察を用いて、思考や社会的行動を支える脳の外層である大脳皮質に焦点を当てました。雄の子では(雌では軽度のみ)、神経幹/前駆細胞がより早期に、かつ多くのニューロンを作る方向へ傾き、幹細胞のプールや後期細胞型(例えばアストロサイト)が減少していました。総脳サイズは変わらない一方で、皮質ニューロンの通常の層状配列は目に見えて乱れていました。
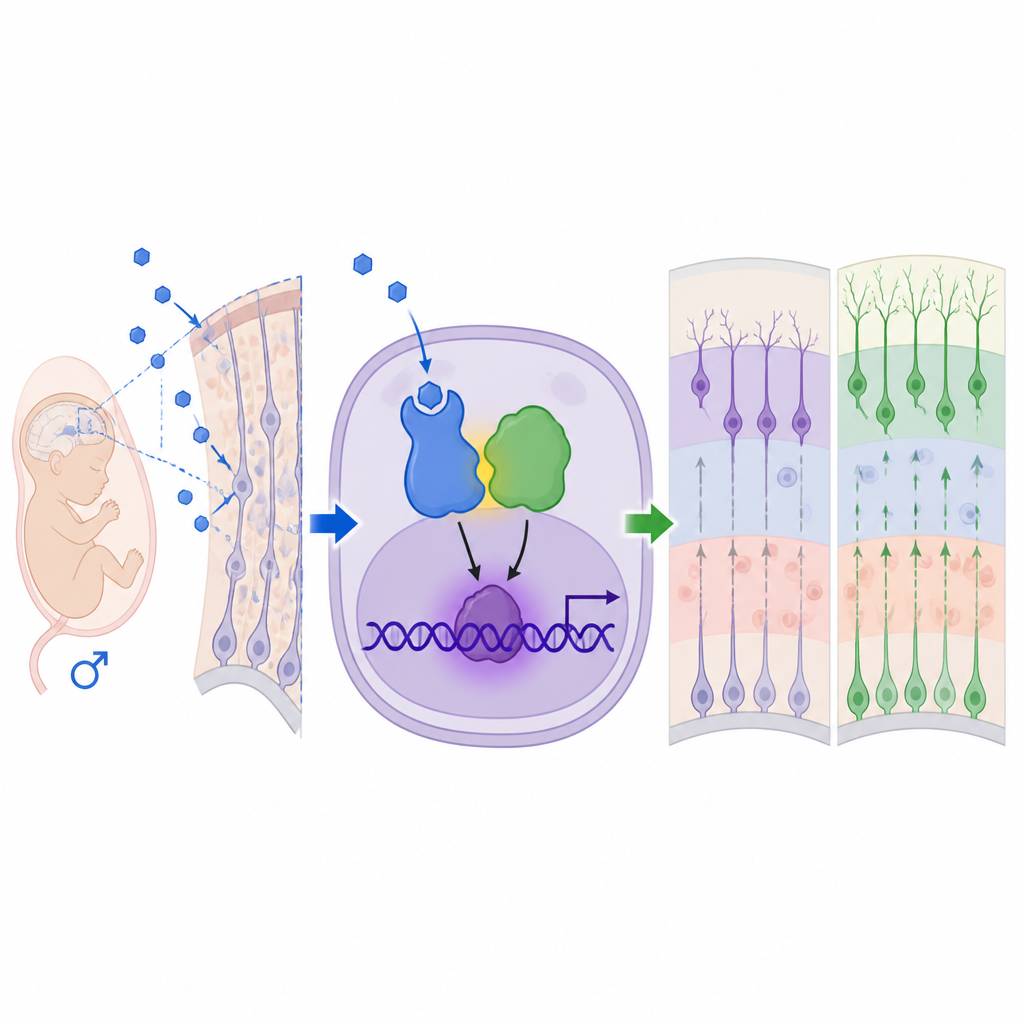
変化した皮質から行動変化へ
成人期において、母体が高アンドロゲン状態であった雄子は、自閉症でしばしば見られる特徴を反映する行動の違いを示しました。社会性テストでは、これらの雄は他のマウスとの交流に費やす時間が短く、新しい社会的相手への興味が低下しましたが、運動レベルは正常でした。また、より多くのマーブルを埋めるなど反復的行動が増え、開放場や高架臂迷路テストでは不安様の兆候が強まりました。同じ条件下で育てられ、生後にコントロール母に交差養育された雌子は、はるかに軽度か無変化であり、脆弱性が雄に偏ることを強調しています。
発達中の脳細胞内の非標準的経路
アンドロゲンがどのようにこれらの影響を及ぼすかを理解するため、チームはこれらのホルモンを感知するタンパク質であるアンドロゲン受容体に注目しました。雄胎児皮質ではアンドロゲン受容体の発現と核内局在が増加しており、フルタミドでこの受容体を遮断すると過剰な神経新生と大部分の行動変化が逆転しました。遺伝子発現解析は、神経発達障害と関連する転写因子MEF2Cを主要な下流標的として示しました。驚くべきことに、アンドロゲン受容体は単独で、または通常のDNA結合部位を介して作用しているわけではありませんでした。代わりに、X染色体上の遺伝子でコードされ、レット症候群やMeCP2重複症で知られるタンパク質MeCP2と物理的に結合しました。アンドロゲン受容体とMeCP2は共に活性化複合体を形成し、Mef2cの制御領域にあるMeCP2が認識する部位に結合してMEF2Cを増強し、神経幹細胞をニューロンへと駆り立てました。
MeCP2自体が増加した場合に起きること
著者らは次に、MeCP2のコピーが余分にあるマウスモデルに着目しました。これらのマウスは以前、皮質神経新生の増加と自閉症様行動を示すことが報告されていました。MeCP2重複の雄でも、出生前の追加アンドロゲンがなくてもMEF2Cが上昇し、類似の皮質変化が見られました。これらのマウスでMef2cを抑えるかアンドロゲン受容体を阻害すると、皮質の層配列が正常化し、社会性、反復行動、不安様行動の多くが改善しました。これは、過剰なMeCP2が同じホルモン感受性経路を関与させ得ること、そしてアンドロゲン信号が存在する際に雄特有のリスクを増幅し得ることを示唆しています。
この研究が性差の見方をどう変えるか
総じて、本研究は母体のアンドロゲン曝露が雄胎児の皮質とその後の行動を形作る、これまで認識されていなかった経路を明らかにしました。アンドロゲン受容体は古典的な標的のみを通じて作用するのではなく、MeCP2を取り込みMEF2Cをスイッチオンすることで、神経幹細胞の運命のバランスを傾け、皮質回路を微妙に再配線します。MeCP2はX染色体上に位置し、いくつかのヒトの神経発達症候群に既に関与しているため、このホルモン依存的な連携は、なぜ男子がある種の脳に基づく状態にかかりやすいのかという具体的な分子説明を提供すると同時に、遺伝子と出生前のホルモン環境の両方を併せて考慮する必要があることを示唆します。
引用: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
キーワード: 出生前アンドロゲン, MeCP2, 皮質発達, MEF2C, 自閉症リスク