Clear Sky Science · es
MeCP2 gobierna los defectos corticales y las alteraciones conductuales inducidos por la hiperandrogenemia materna mediante una regulación no canónica dependiente de AR de Mef2c
Por qué esta investigación importa a las familias
Muchas condiciones que afectan el aprendizaje, las habilidades sociales y el comportamiento son más frecuentes en niños que en niñas, pero las razones de esta diferencia sexual siguen sin aclararse. Este estudio usa ratones para explorar cómo niveles elevados de hormonas masculinas durante el embarazo pueden remodelar de forma sutil el cerebro en desarrollo de la descendencia masculina, y cómo una proteína cerebral bien conocida, MeCP2, ayuda a traducir esas señales hormonales en cambios duraderos en la estructura cerebral y el comportamiento.
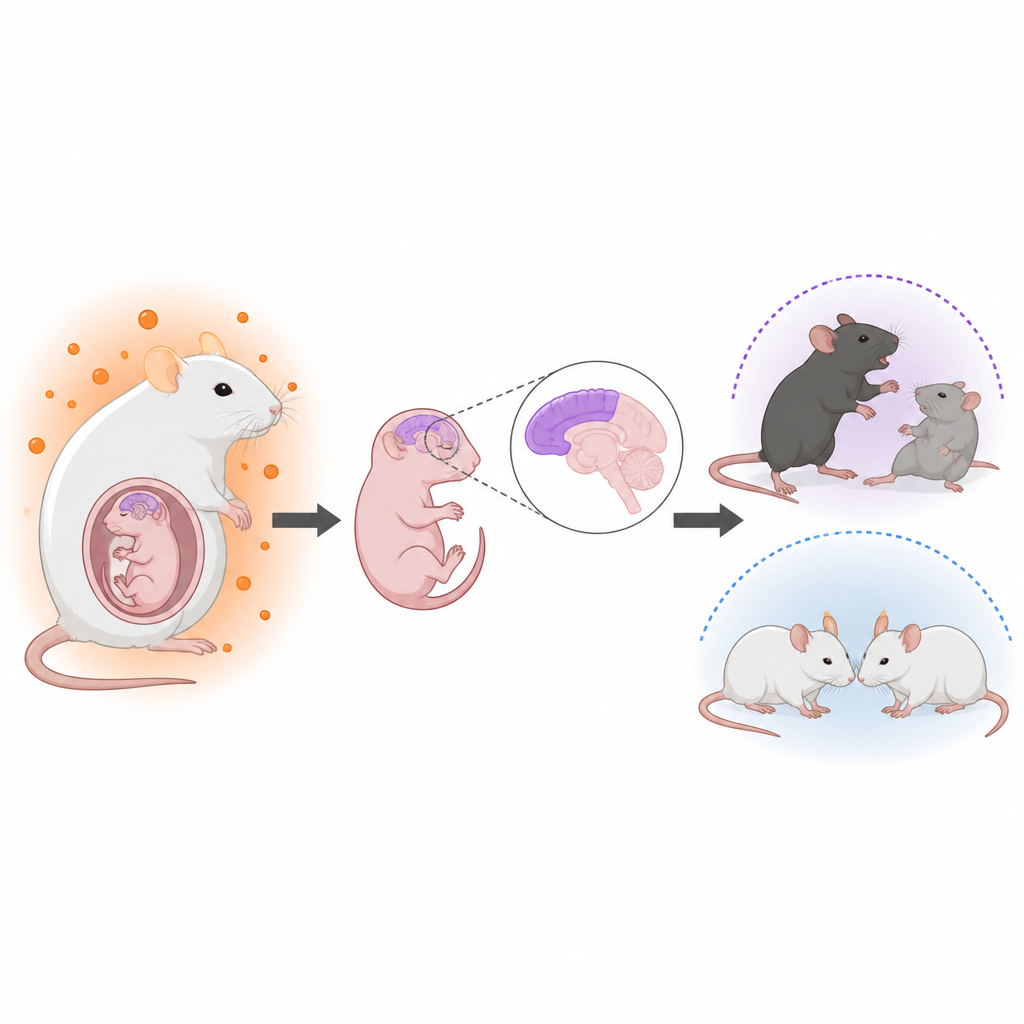
Hormonas antes del nacimiento y salud cerebral posterior
Los médicos han observado durante mucho tiempo vínculos entre niveles elevados de hormonas masculinas en el útero y una mayor probabilidad de trastornos del neurodesarrollo como el autismo. Por ejemplo, las mujeres con síndrome de ovario poliquístico suelen presentar niveles más altos de andrógenos y sus hijos muestran un riesgo de autismo ligeramente aumentado. Sin embargo, no estaba claro cómo actúan estas hormonas sobre el cerebro fetal ni por qué los hijos parecen más afectados que las hijas. Los autores se propusieron construir un modelo de ratón realista de hiperandrogenemia materna y luego seguir tanto el desarrollo cerebral como el comportamiento de la descendencia.
Cómo el equipo modeló la exposición hormonal
Los investigadores trataron a ratonas embarazadas con un fármaco que bloquea la aromatasa, la enzima que normalmente convierte la testosterona en estrógeno. Esto elevó los niveles de testosterona en las madres, en el líquido amniótico que rodea a los fetos y en los cerebros fetales, sin cambiar los resultados generales del embarazo ni los pesos al nacer. Mediante marcaje genético y microscopía, se centraron en la corteza cerebral, la capa externa del cerebro que sostiene el pensamiento y el comportamiento social. En la descendencia masculina, pero solo de forma leve en las hembras, observaron que las células madre y progenitoras neurales fueron empujadas a crear neuronas antes y en mayor número, mientras que el reservorio de células madre y algunos tipos celulares tardíos, como los astrocitos, se redujeron. La disposición normal por capas de las neuronas corticales se volvió notablemente menos ordenada, pese a que el tamaño cerebral total no cambió.
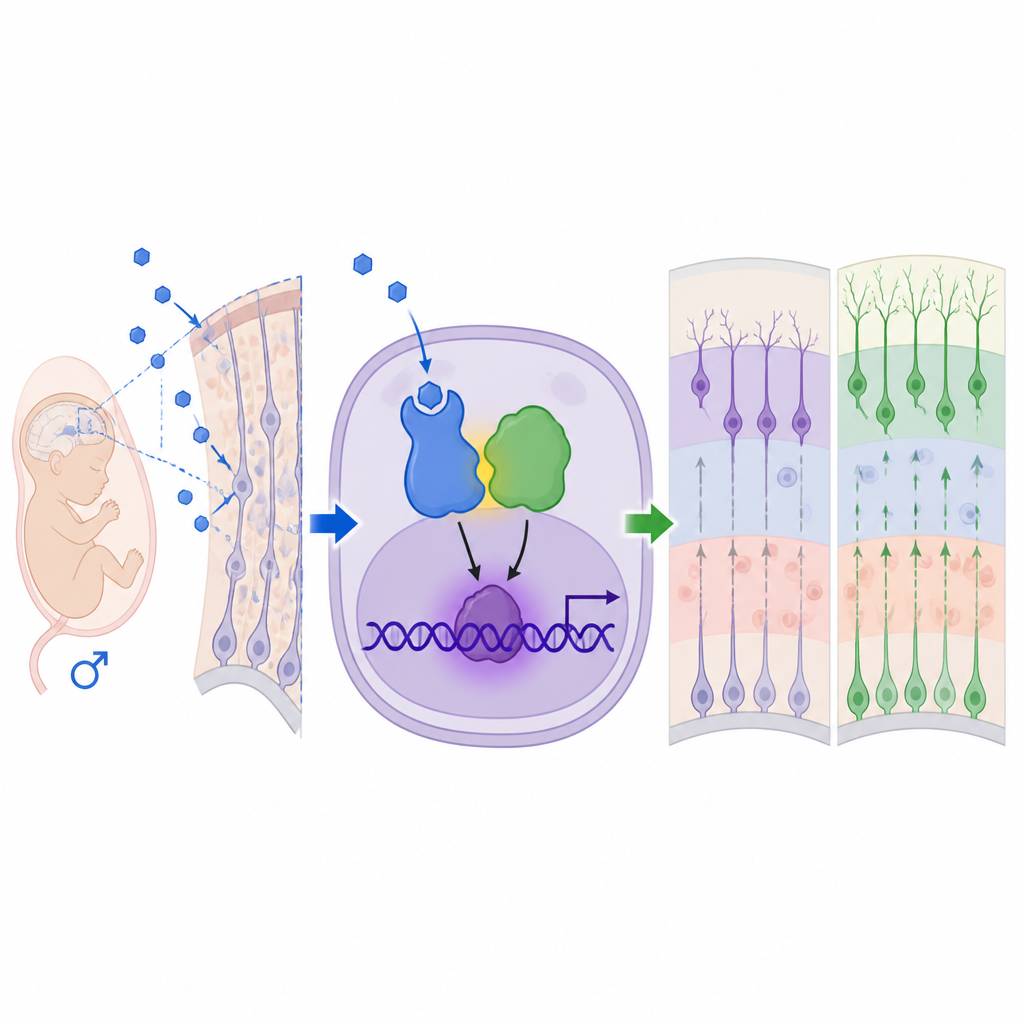
De una corteza alterada a un comportamiento modificado
En la edad adulta, los machos procedentes de madres hiperandrogénicas mostraron diferencias conductuales que reflejan varios rasgos frecuentemente observados en el autismo. En pruebas sociales, estos machos pasaron menos tiempo interactuando con otros ratones y mostraron menor interés por nuevas parejas sociales, mientras que sus niveles de movimiento se mantuvieron normales. También exhibieron comportamientos repetitivos más frecuentes, como enterrar más canicas, y signos más intensos de ansiedad en pruebas de campo abierto y en el laberinto elevado en cruz. Las hembras de la descendencia, criadas en las mismas condiciones y posteriormente acogidas por madres de control tras el nacimiento, mostraron cambios conductuales mucho más leves o nulos, lo que pone de relieve una mayor vulnerabilidad en los machos.
Una vía no estándar dentro de las células cerebrales en desarrollo
Para entender cómo los andrógenos ejercen estos efectos, el equipo se centró en los receptores de andrógenos, las proteínas que detectan estas hormonas. Encontraron niveles y localización nuclear aumentados del receptor de andrógenos en la corteza fetal masculina, y bloquear este receptor con el fármaco flutamida revirtió la neurogénesis excesiva y la mayoría de los cambios conductuales. Los análisis de expresión génica apuntaron a MEF2C, un factor de transcripción ya vinculado a trastornos del neurodesarrollo, como un objetivo descendente clave. Sorprendentemente, el receptor de andrógenos no actuó solo ni a través de sus sitios habituales de unión al ADN. En cambio, se asoció físicamente con MeCP2, una proteína codificada por un gen en el cromosoma X conocida por el síndrome de Rett y el síndrome de duplicación de MeCP2. Juntos, el receptor de andrógenos y MeCP2 formaron un complejo activador que se unió en un sitio reconocido por MeCP2 en la región reguladora de Mef2c, aumentando los niveles de MEF2C e impulsando a las células madre neurales hacia destino neuronal.
Qué ocurre cuando MeCP2 está aumentado
Los autores recurrieron entonces a un modelo de ratón que porta una copia extra de MeCP2, que previamente había mostrado aumento de la neurogénesis cortical y conductas similares al autismo. Descubrieron que estos machos con duplicación de MeCP2 también presentaban MEF2C elevado y cambios corticales similares, incluso sin andrógenos prenatales adicionales. Reducir Mef2c o bloquear los receptores de andrógenos en estos ratones normalizó el apilamiento cortical y alivió muchas de las conductas sociales, repetitivas y de tipo ansioso. Esto sugiere que un exceso de MeCP2 puede activar la misma vía sensible a hormonas, amplificando el riesgo específico de los machos cuando están presentes señales de andrógenos.
Cómo cambia esto nuestra visión de las diferencias sexuales
En conjunto, el estudio revela una ruta hasta ahora no reconocida mediante la cual la exposición materna a andrógenos puede moldear la corteza fetal masculina y el comportamiento posterior. En lugar de actuar solo a través de sus dianas clásicas, el receptor de andrógenos puede secuestrar a MeCP2 para activar MEF2C, desplazando así el equilibrio de destinos de las células madre neurales y reconectando de forma sutil los circuitos corticales. Dado que MeCP2 se localiza en el cromosoma X y ya está implicado en varios síndromes humanos del neurodesarrollo, esta asociación sensible a hormonas ofrece una explicación molecular concreta de por qué los niños pueden ser más propensos a ciertas condiciones cerebrales, al tiempo que sugiere que tanto los genes como el ambiente hormonal prenatal deben considerarse conjuntamente.
Cita: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
Palabras clave: andrógenos prenatales, MeCP2, desarrollo cortical, MEF2C, riesgo de autismo