Clear Sky Science · pt
MeCP2 governa defeitos corticais e alterações comportamentais induzidos por hiperandrogenismo materno via regulação não canônica dependente de AR de Mef2c
Por que esta pesquisa importa para as famílias
Muitas condições que afetam aprendizado, habilidades sociais e comportamento são mais comuns em meninos do que em meninas, mas as razões dessa diferença entre os sexos ainda não são claras. Este estudo utiliza camundongos para investigar como níveis elevados de hormônios masculinos durante a gravidez podem remodelar de forma sutil o cérebro em desenvolvimento dos filhotes machos, e como uma proteína cerebral bem conhecida, MeCP2, ajuda a traduzir esses sinais hormonais em alterações duradouras na estrutura cerebral e no comportamento.
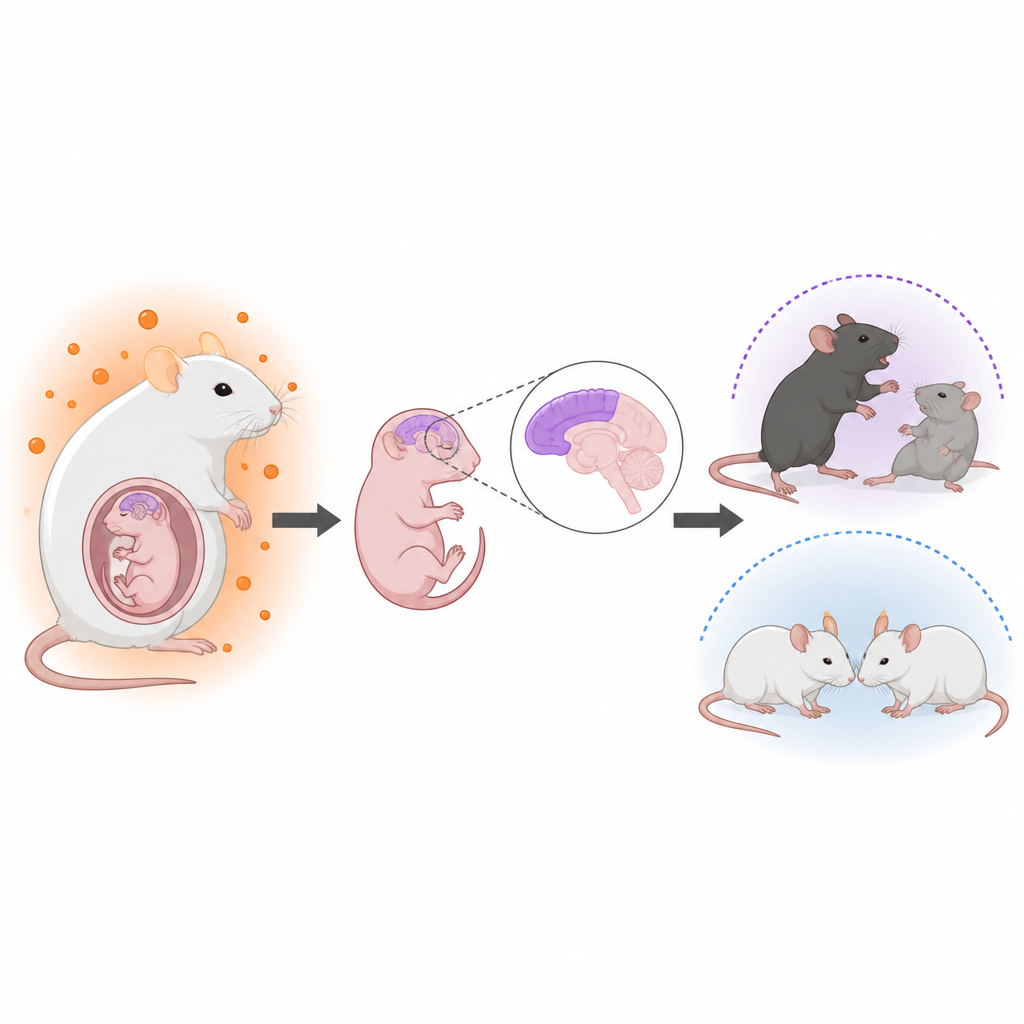
Hormônios antes do nascimento e saúde cerebral posterior
Médicos vêm observando há muito tempo ligações entre níveis elevados de hormônios masculinos no útero e maior probabilidade de condições do neurodesenvolvimento, como o autismo. Por exemplo, mulheres com síndrome dos ovários policísticos frequentemente apresentam níveis mais altos de andrógenos e seus filhos mostram um risco ligeiramente aumentado de autismo. No entanto, não estava claro como esses hormônios atuam no cérebro fetal ou por que os filhos parecem ser mais afetados do que as filhas. Os autores procuraram construir um modelo realista de hiperandrogenismo materno em camundongos e então acompanhar tanto o desenvolvimento cerebral quanto o comportamento dos filhotes.
Como a equipe modelou a exposição hormonal
Os pesquisadores trataram camundongas grávidas com um fármaco que bloqueia a aromatase, a enzima que normalmente converte testosterona em estrogênio. Isso elevou os níveis de testosterona nas mães, no líquido amniótico ao redor dos fetos e nos cérebros fetais, sem alterar os desfechos gerais da gravidez ou os pesos ao nascer. Usando marcação genética e microscopia, eles focaram no córtex cerebral, a camada externa do cérebro que sustenta o raciocínio e o comportamento social. Nos filhotes machos, mas apenas de forma leve nas fêmeas, constataram que células-tronco neurais e progenitoras foram direcionadas a gerar neurônios mais cedo e em maior número, enquanto o reservatório de células-tronco e alguns tipos celulares tardios, como astrócitos, foi reduzido. O arranjo em camadas normal dos neurônios corticais tornou-se visivelmente menos ordenado, embora o tamanho total do cérebro não tenha mudado.
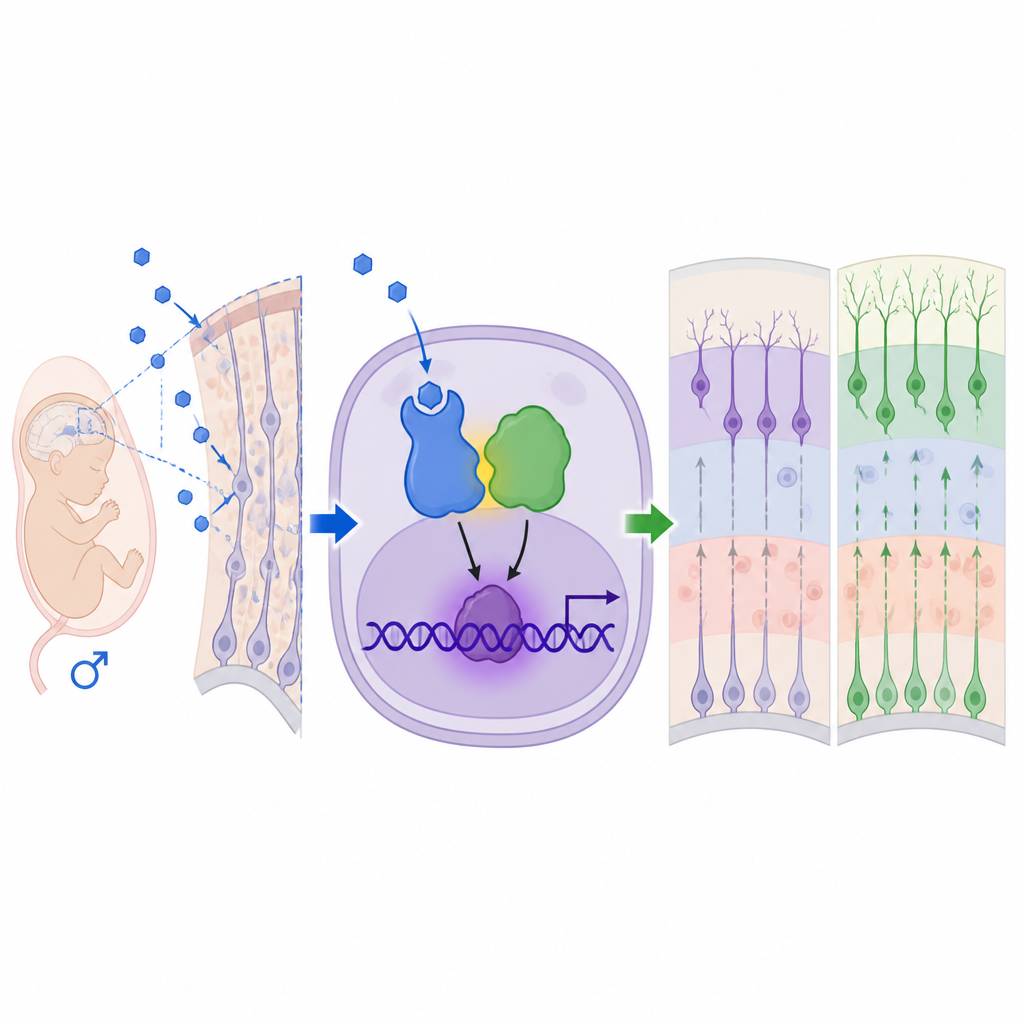
Do córtex alterado ao comportamento modificado
Na vida adulta, os filhotes machos de mães hiperandrogênicas exibiram diferenças comportamentais que espelham várias características frequentemente observadas no autismo. Em testes sociais, esses machos passaram menos tempo interagindo com outros camundongos e mostraram menos interesse por novos parceiros sociais, enquanto seus níveis de movimento permaneceram normais. Também exibiram comportamentos mais repetitivos, como enterrar mais bolinhas, e sinais mais intensos de ansiedade em testes de campo aberto e labirinto elevado em “+”. As fêmeas, criadas nas mesmas condições e adotadas por mães controle após o nascimento, apresentaram alterações comportamentais bem mais leves ou ausentes, ressaltando uma vulnerabilidade com viés masculino.
Uma via não convencional dentro de células cerebrais em desenvolvimento
Para entender como os andrógenos exercem esses efeitos, a equipe investigou os receptores de andrógeno, as proteínas que detectam esses hormônios. Encontraram níveis mais altos e localização nuclear do receptor de andrógeno no córtex fetal masculino, e bloquear esse receptor com o fármaco flutamida reverteu a neurogênese excessiva e a maioria das alterações comportamentais. Análises de expressão gênica apontaram MEF2C, um fator de transcrição já ligado a transtornos do neurodesenvolvimento, como um alvo chave a jusante. Surpreendentemente, o receptor de andrógeno não atuou sozinho nem através de seus locais habituais de ancoragem no DNA. Em vez disso, associou-se fisicamente ao MeCP2, uma proteína codificada por um gene no cromossomo X, conhecida por sua relação com a síndrome de Rett e com a síndrome de duplicação de MeCP2. Juntos, receptor de andrógeno e MeCP2 formaram um complexo ativador que se ligou a um sítio reconhecido por MeCP2 na região regulatória de Mef2c, elevando os níveis de MEF2C e conduzindo células-tronco neurais em direção a neurônios.
O que acontece quando o próprio MeCP2 está aumentado
Os autores então utilizaram um modelo de camundongo que carrega uma cópia extra de MeCP2, o qual já havia mostrado neurogênese cortical aumentada e comportamentos semelhantes ao autismo. Descobriram que esses machos com duplicação de MeCP2 também apresentavam MEF2C elevado e alterações corticais semelhantes, mesmo sem andrógenos pré-natais extras. Reduzir Mef2c ou bloquear receptores de andrógeno nesses camundongos normalizou a laminação cortical e aliviou muitos dos comportamentos sociais, repetitivos e semelhantes à ansiedade. Isso sugere que excesso de MeCP2 pode ativar a mesma via sensível a hormônios, amplificando o risco específico em machos quando sinais androgênicos estão presentes.
Como este trabalho muda nossa visão sobre diferenças entre os sexos
No conjunto, o estudo revela uma via antes não reconhecida pela qual a exposição materna a andrógenos pode moldar o córtex fetal masculino e o comportamento posterior. Em vez de agir apenas por meio de seus alvos clássicos, o receptor de andrógeno pode sequestrar MeCP2 para ativar MEF2C, desequilibrando destinos de células-tronco neurais e reconfigurando sutilmente circuitos corticais. Como MeCP2 está no cromossomo X e já está implicado em várias síndromes humanas do neurodesenvolvimento, essa parceria sensível a hormônios oferece uma explicação molecular concreta para por que meninos podem ser mais propensos a certas condições cerebrais, ao mesmo tempo em que sugere que tanto genes quanto o ambiente hormonal pré-natal devem ser considerados em conjunto.
Citação: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
Palavras-chave: andrógenos pré-natais, MeCP2, desenvolvimento cortical, MEF2C, risco de autismo