Clear Sky Science · fr
MeCP2 gouverne les défauts corticaux et les altérations comportementales induits par l’hyperandrogénie maternelle via une régulation non canonique dépendante du récepteur aux androgènes de Mef2c
Pourquoi cette recherche compte pour les familles
De nombreux troubles affectant l’apprentissage, les compétences sociales et le comportement sont plus fréquents chez les garçons que chez les filles, mais les raisons de cette différence sexuelle restent floues. Cette étude utilise la souris pour explorer comment des taux élevés d’hormones mâles pendant la grossesse peuvent remodeler subtilement le cerveau en développement des descendants mâles, et comment une protéine cérébrale bien connue, MeCP2, traduit ces signaux hormonaux en changements durables de la structure cérébrale et du comportement.
Les hormones avant la naissance et la santé cérébrale ultérieure
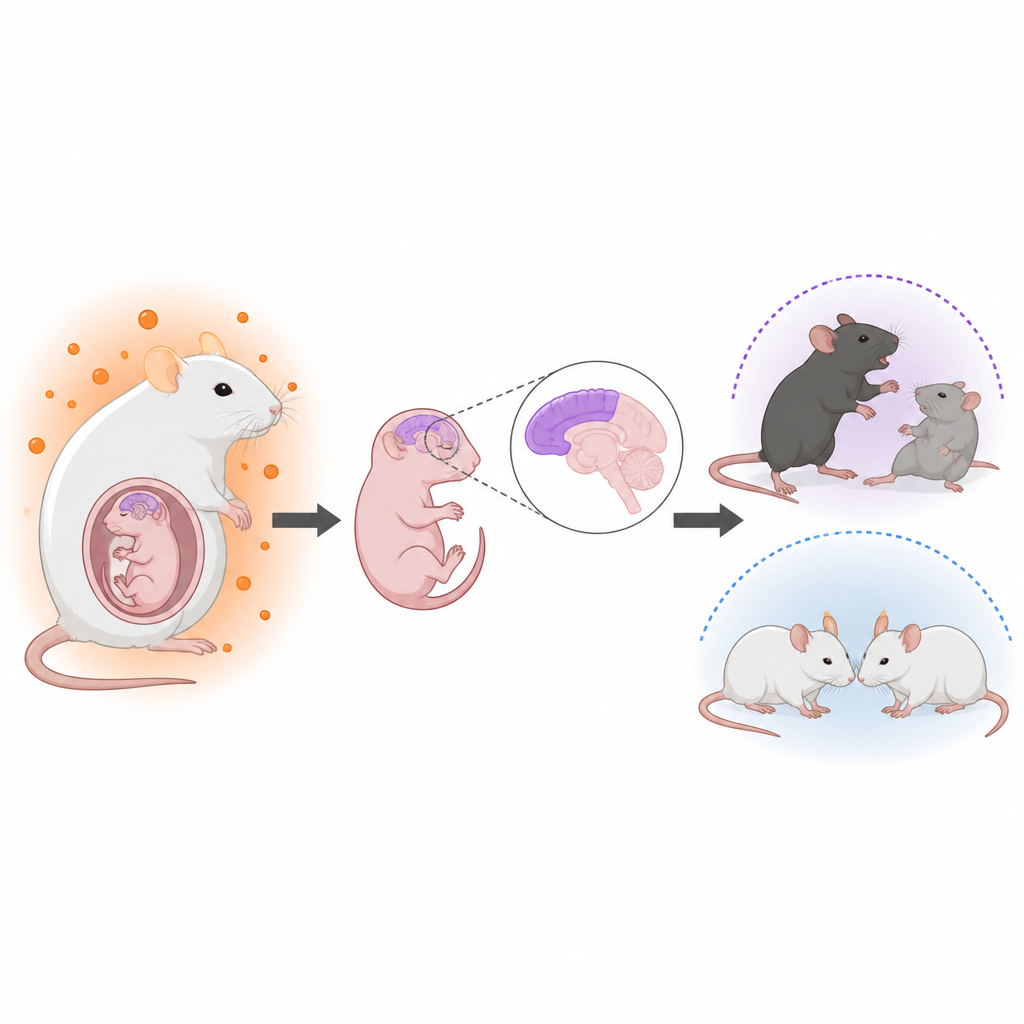
Les cliniciens ont depuis longtemps relevé des liens entre des androgènes élevés in utero et un risque accru de troubles du neurodéveloppement, comme l’autisme. Par exemple, les femmes atteintes du syndrome des ovaires polykystiques présentent souvent des taux d’androgènes plus élevés et leurs enfants présentent un risque légèrement augmenté d’autisme. Cependant, on ignorait comment ces hormones agissent sur le cerveau fœtal et pourquoi les fils semblent plus touchés que les filles. Les auteurs ont donc mis au point un modèle murin réaliste d’hyperandrogénie maternelle pour suivre ensuite le développement cérébral et le comportement des descendants.
Comment l’équipe a modélisé l’exposition hormonale
Les chercheurs ont traité des souris gravides avec un médicament qui bloque l’aromatase, l’enzyme qui convertit normalement la testostérone en œstrogènes. Cela a augmenté les taux de testostérone chez les mères, dans le liquide amniotique entourant les fœtus et dans les cerveaux fœtaux, sans modifier les issues globales de la grossesse ni les poids à la naissance. Grâce au marquage génétique et à la microscopie, ils se sont concentrés sur le cortex cérébral, la couche externe du cerveau qui soutient la pensée et le comportement social. Chez les descendants mâles, et de façon beaucoup plus modeste chez les femelles, ils ont constaté que les cellules souches neurales et progénitrices étaient poussées à produire des neurones plus tôt et en plus grand nombre, tandis que le réservoir de cellules souches et certaines cellules tardives comme les astrocytes diminuaient. L’organisation en couches normales des neurones corticaux est devenue visiblement moins ordonnée, bien que la taille cérébrale totale n’ait pas changé.
Du cortex modifié au comportement altéré
A l’âge adulte, les descendants mâles issus de mères hyperandrogéniques présentaient des différences comportementales qui rappellent plusieurs traits souvent observés dans l’autisme. Lors de tests sociaux, ces mâles passaient moins de temps à interagir avec d’autres souris et montraient moins d’intérêt pour de nouveaux partenaires sociaux, alors que leur niveau de locomotion restait normal. Ils présentaient également davantage de comportements répétitifs, comme enterrer plus de billes, et des signes plus marqués d’anxiété dans les épreuves en champ ouvert et en labyrinthe en croix surélevé. Les femelles issues des mêmes conditions et élevées par des mères témoins après la naissance montraient des changements comportementaux bien plus légers, voire inexistants, soulignant une vulnérabilité biaisée vers les mâles.
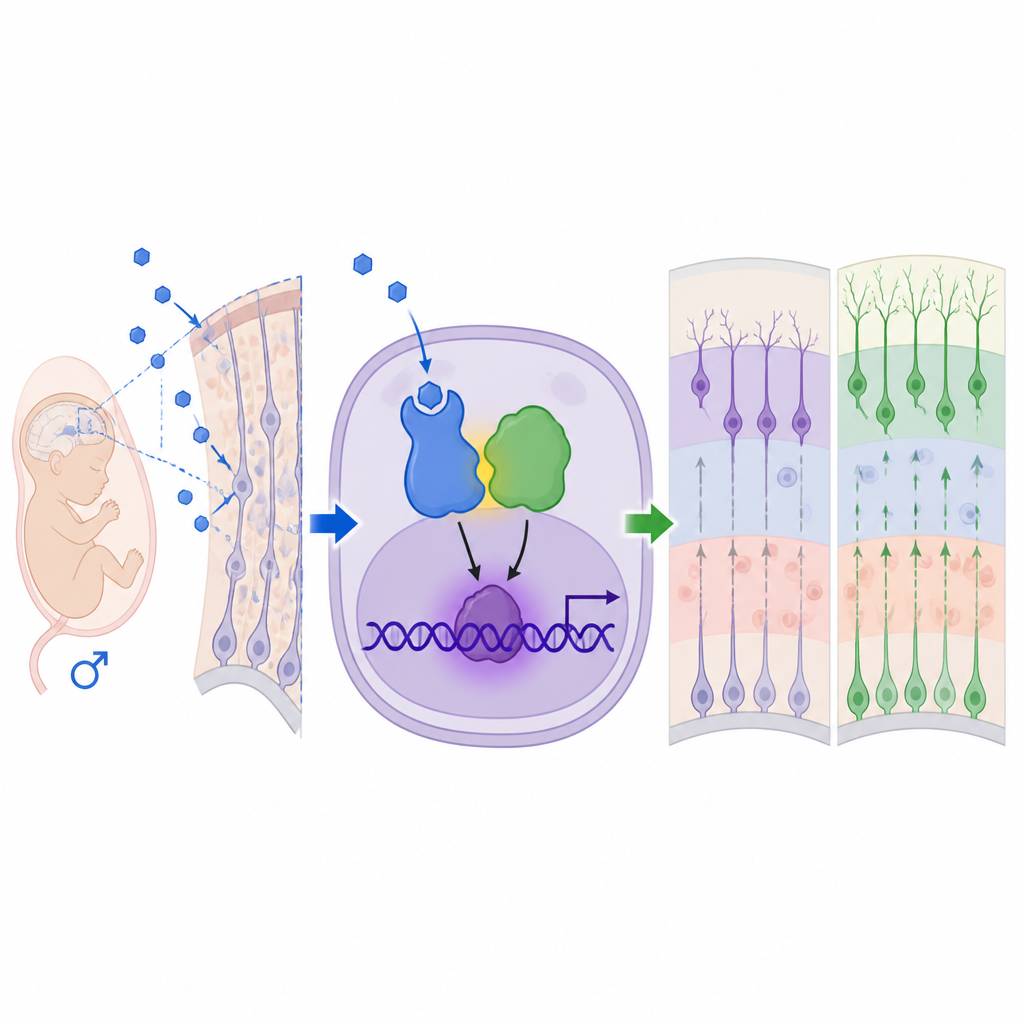
Une voie non standard à l’intérieur des cellules cérébrales en développement
Pour comprendre comment les androgènes produisent ces effets, l’équipe s’est penchée sur les récepteurs aux androgènes, les protéines qui détectent ces hormones. Ils ont observé des niveaux plus élevés et une localisation nucléaire accrue du récepteur aux androgènes dans le cortex fœtal mâle, et le blocage de ce récepteur par la flutamide a inversé la neurogenèse excessive et la plupart des changements comportementaux. Les analyses d’expression génique ont identifié MEF2C, un facteur de transcription déjà associé aux troubles du neurodéveloppement, comme une cible en aval clé. De façon surprenante, le récepteur aux androgènes n’agissait pas seul ni via ses sites d’ancrage classiques sur l’ADN. Il s’est physiquement associé à MeCP2, une protéine codée par un gène porté par le chromosome X, connue notamment à partir du syndrome de Rett et du syndrome de duplication de MeCP2. Ensemble, le récepteur aux androgènes et MeCP2 ont formé un complexe activateur qui se liait à un site reconnu par MeCP2 dans la région régulatrice de Mef2c, augmentant les niveaux de MEF2C et orientant les cellules souches neurales vers des destinées neuronales.
Que se passe-t-il lorsque MeCP2 est lui-même augmenté
Les auteurs se sont ensuite intéressés à un modèle murin portant une copie supplémentaire de MeCP2, qui avait déjà montré une neurogenèse corticale accrue et des comportements proches de l’autisme. Ils ont découvert que ces mâles avec duplication de MeCP2 présentaient eux aussi une élévation de MEF2C et des changements corticaux similaires, même sans androgènes prénataux supplémentaires. Réduire l’expression de Mef2c ou bloquer les récepteurs aux androgènes chez ces souris normalisait la stratification corticale et atténuait nombre des comportements sociaux, répétitifs et anxieux. Cela suggère qu’un excès de MeCP2 peut mobiliser la même voie sensible aux hormones, amplifiant le risque spécifique aux mâles lorsque des signaux androgéniques sont présents.
Comment ce travail modifie notre regard sur les différences entre les sexes
Globalement, l’étude révèle une voie jusque-là méconnue par laquelle l’exposition maternelle aux androgènes peut façonner le cortex fœtal masculin et le comportement ultérieur. Plutôt que d’agir uniquement via ses cibles classiques, le récepteur aux androgènes peut détourner MeCP2 pour activer MEF2C, basculant l’équilibre des destinées des cellules souches neurales et reconfigurant subtilement les circuits corticaux. Parce que MeCP2 se trouve sur le chromosome X et est déjà impliqué dans plusieurs syndromes humains du neurodéveloppement, ce partenariat sensible aux hormones offre une explication moléculaire concrète du pourquoi les garçons peuvent être plus susceptibles de certains troubles cérébraux, tout en suggérant que gènes et environnement hormonal prénatal doivent être considérés ensemble.
Citation: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
Mots-clés: androgènes prénataux, MeCP2, développement cortical, MEF2C, risque d’autisme