Clear Sky Science · ar
يُسيطر MeCP2 على العيوب القشرية والتغيرات السلوكية الناتجة عن فرط الأندروجينات الأمومي عبر تنظيم غير كلاسيكي معتمد على مستقبلات الأندروجين للمورث Mef2c
لماذا تهم هذه الدراسة العائلات
العديد من الحالات التي تؤثر على التعلم والمهارات الاجتماعية والسلوك أكثر شيوعًا لدى الأولاد مقارنة بالبنات، لكن أسباب هذا الاختلاف بين الجنسين ما زالت غير واضحة. تستخدم هذه الدراسة الفئران لاستكشاف الكيفية التي يمكن أن تعيد بها المستويات العالية من الهرمونات الذكرية أثناء الحمل تشكيل الدماغ النامي للأجنة الذكور بشكل دقيق، وكيف يساعد بروتين دماغي معروف وهو MeCP2 في تحويل تلك الإشارات الهرمونية إلى تغييرات مستمرة في بنية الدماغ والسلوك.
الهرمونات قبل الولادة وصحة الدماغ لاحقًا
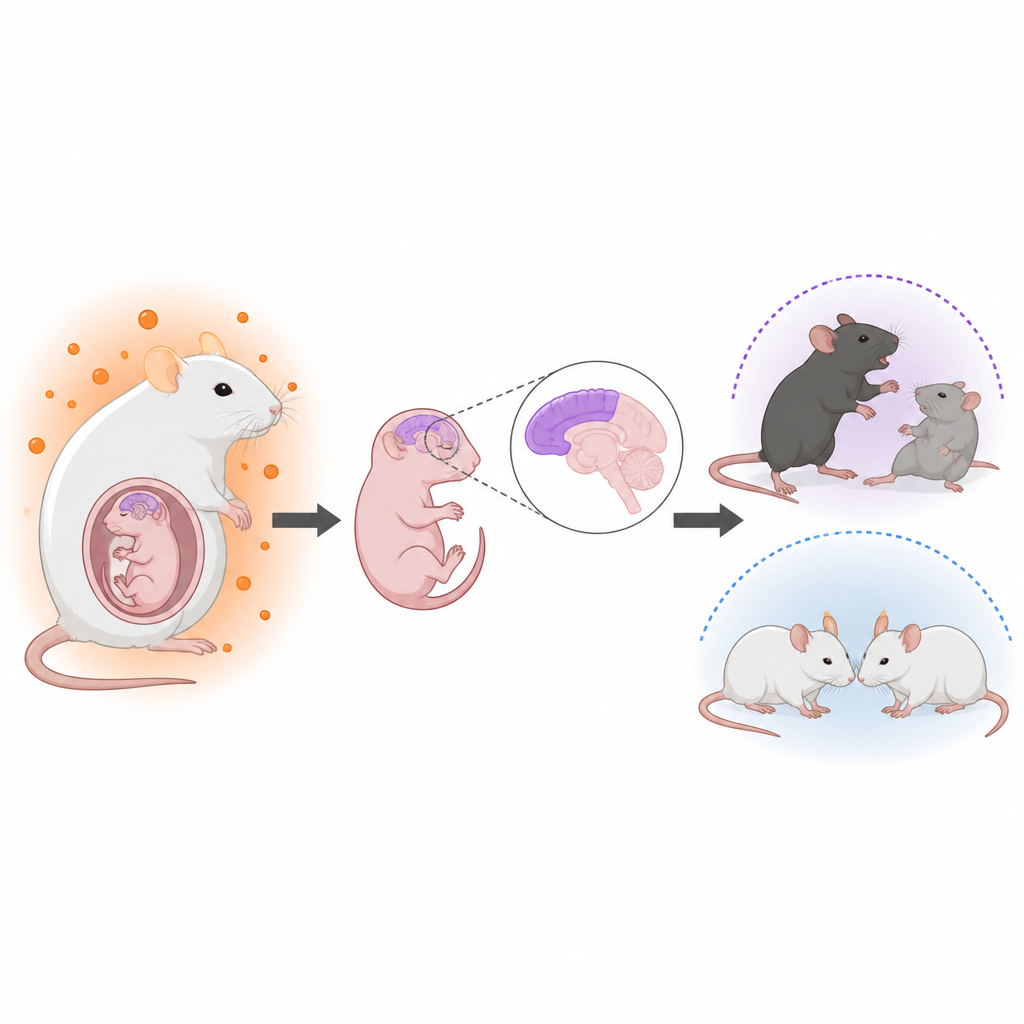
لاحظ الأطباء منذ زمن وجود روابط بين ارتفاع الهرمونات المذكرة في الرحم وزيادة احتمال حدوث اضطرابات النمو العصبي مثل التوحد. على سبيل المثال، النساء المصابات بمتلازمة تكيس المبايض غالبًا ما يكنّ مستويات أعلى من الأندروجينات وأطفالهن يظهرون خطرًا طفيفًا متزايدًا للتوحد. ومع ذلك، لم يكن واضحًا كيف تؤثر هذه الهرمونات على دماغ الجنين أو لماذا يبدو أن الأولاد يتأثرون أكثر من البنات. سعى الباحثون لبناء نموذج فأري واقعي لفرط الأندروجينات الأمومي ثم تتبّع كل من تطور الدماغ والسلوك لدى النسل.
كيف نمذَج الفريق التعرض الهرموني
عالج الباحثون فئرانًا حوامل بدواء يثبط الأروماتاز، وهو الإنزيم الذي يحول عادة التستوستيرون إلى إستروجين. رفع ذلك مستويات التستوستيرون لدى الأمهات وفي السائل الأمينوسي المحيط بالأجنة وفي أدمغة الأجنة، دون تغيير مخرجات الحمل أو أوزان الولادة بصورة عامة. باستخدام الوسم الجيني والمجهر، ركزوا على القشرة المخية، الطبقة الخارجية من الدماغ المسؤولة عن التفكير والسلوك الاجتماعي. في النسل الذكر، لكن بدرجة طفيفة لدى الإناث فقط، وجدوا أن الخلايا الجذعية والعصبية المحللة دُفعت لإنتاج خلايا عصبية مبكرًا وبأعداد أكبر، بينما تقلصت مخزونات الخلايا الجذعية وبعض الخلايا اللاحقة مثل الخلايا النجمية. صار الترتيب الطبقي الطبيعي للخلايا القشرية أقل انتظامًا بشكل ملحوظ، رغم أن الحجم الكلي للدماغ لم يتغير.
من القشرة المتغيرة إلى السلوك المعدل
كب بالغين، أظهر النسل الذكر من الأمهات ذات فرط الأندروجينات فروقًا في السلوك تشبه عدة ملامح تُرى غالبًا في التوحد. في اختبارات اجتماعية، قضى هؤلاء الذكور وقتًا أقل في التفاعل مع فئران أخرى وأبدوا اهتمامًا أقل بشركاء اجتماعيين جدد، بينما بقيت مستويات حركتهم طبيعية. كما أظهروا سلوكيات نمطية متكررة أكثر، مثل دفن عدد أكبر من الخرز، وملامح قلق أقوى في اختبارات الساحة المفتوحة والمميز المرتفع. أما الإناث اللاتي تربين تحت نفس الظروف ونُقلن بعد الولادة إلى أمهات ضابطة، فظهرن تغيرات سلوكية أخف بكثير أو معدومة، مما يبرز تحيزًا في القابلية لدى الذكور.
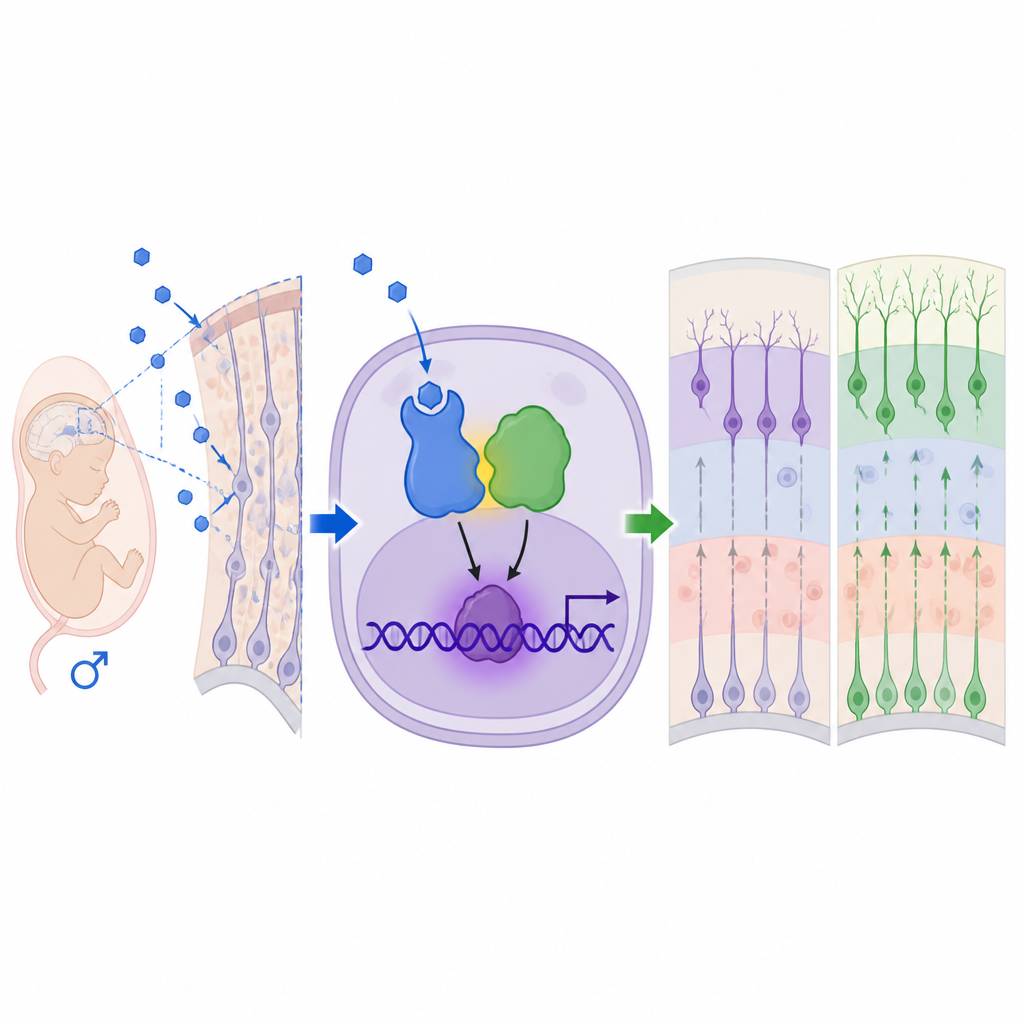
ممر غير نمطي داخل خلايا الدماغ النامية
لفهم كيف تمارس الأندروجينات هذه التأثيرات، قام الفريق بالتدقيق في مستقبلات الأندروجين، البروتينات التي تلتقط هذه الهرمونات. وجدوا مستويات أعلى وتوضعًا نوويًا لمستقبل الأندروجين في قشرة الجنين الذكرية، وإيقاف هذا المستقبل بالدواء فلوتاميد عكس فرط تكون الخلايا العصبية ومعظم التغيرات السلوكية. أشارت تحليلات التعبير الجيني إلى MEF2C، عامل نسخي مرتبط بالفعل باضطرابات النمو العصبي، كهدف أساسي لاحق. بشكل مفاجئ، لم يعمل مستقبل الأندروجين بمفرده أو عبر مواقع ارتباطه الكلاسيكية على الحمض النووي. بل تعاون جسديًا مع MeCP2، وهو بروتين مشفَّر بواسطة جين على الكروموسوم X ويشتهر بمتلازمة ريت ومضاعفة MeCP2. معًا شكل مستقبل الأندروجين وMeCP2 مركبًا منشطًا يلتصق بموقع يتعرف عليه MeCP2 في المنطقة التنظيمية لـ Mef2c، معززًا مستويات MEF2C ودافعًا خلايا الجذع العصبية نحو مصير خلوي عصبي.
ماذا يحدث عند زيادة MeCP2 بنفسه
انتقل المؤلفون بعد ذلك إلى نموذج فأري يحمل نسخة إضافية من MeCP2، والذي ثبت سابقًا أنه يظهر زيادة في تكون الخلايا القشرية العصبية وسلوكيات شبيهة بالتوحد. اكتشفوا أن هؤلاء الذكور الحاملين مضاعفة MeCP2 لديهم أيضًا مستويات مرتفعة من MEF2C وتغييرات قشرية مماثلة، حتى دون زيادة في الأندروجينات قبل الولادة. خفض نشاط Mef2c أو حجب مستقبلات الأندروجين في هذه الفئران أعاد ترتيب طبقات القشرة إلى وضع أكثر طبيعية وخفف العديد من السلوكيات الاجتماعية والنمطية ومظاهر القلق. يشير هذا إلى أن فرط MeCP2 يمكن أن يشغّل نفس المسار الحساس للهرمون، مضخمًا الخطر الخاص بالذكور عندما تتوفر إشارات الأندروجين.
كيف يغير هذا العمل نظرتنا للفروق بين الجنسين
بشكل عام، تكشف الدراسة عن طريق لم يسبق التعرف عليها سابقًا يمكن من خلالها أن تشكل الأندروجينات الأمومية قشرة الجنين الذكرية والسلوك اللاحق. بدلًا من العمل فقط عبر أهدافه الكلاسيكية، يمكن لمستقبل الأندروجين أن يستغل MeCP2 لتشغيل MEF2C، وبذلك يقلب توازن مصائر الخلايا الجذعية العصبية ويعيد توصيل دوائر قشرية بدقة. ونظرًا لأن MeCP2 يقع على الكروموسوم X ومرتبط بالفعل بعدة متلازمات بشرية في التطور العصبي، فإن هذه الشراكة الحساسة للهرمونات تقدم تفسيرًا جزيئيًا ملموسًا لماذا قد يكون الأولاد أكثر عرضة لبعض الحالات المعتمدة على الدماغ، كما تقترح أن كلا من الجينات وبيئة الهرمونات قبل الولادة يجب أن يُؤخذَا بعين الاعتبار معًا.
الاستشهاد: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
الكلمات المفتاحية: الأندروجينات قبل الولادة, MeCP2, تطور القشرة الدماغية, MEF2C, خطر التوحد