Clear Sky Science · de
MeCP2 steuert durch nichtkanonische, AR‑abhängige Regulation von Mef2c kortikale Defekte und Verhaltensänderungen, die durch mütterliche Hyperandrogenämie ausgelöst werden
Warum diese Forschung für Familien wichtig ist
Viele Störungen, die Lernen, soziale Fähigkeiten und Verhalten betreffen, kommen bei Jungen häufiger vor als bei Mädchen, doch die Gründe für diesen Geschlechtsunterschied sind noch unklar. Diese Studie nutzt ein Mausmodell, um zu untersuchen, wie hohe Androgenspiegel während der Schwangerschaft das sich entwickelnde Gehirn männlicher Nachkommen subtil umgestalten können und wie das bekannte Hirnprotein MeCP2 diese hormonellen Signale in bleibende Veränderungen von Struktur und Verhalten übersetzt.
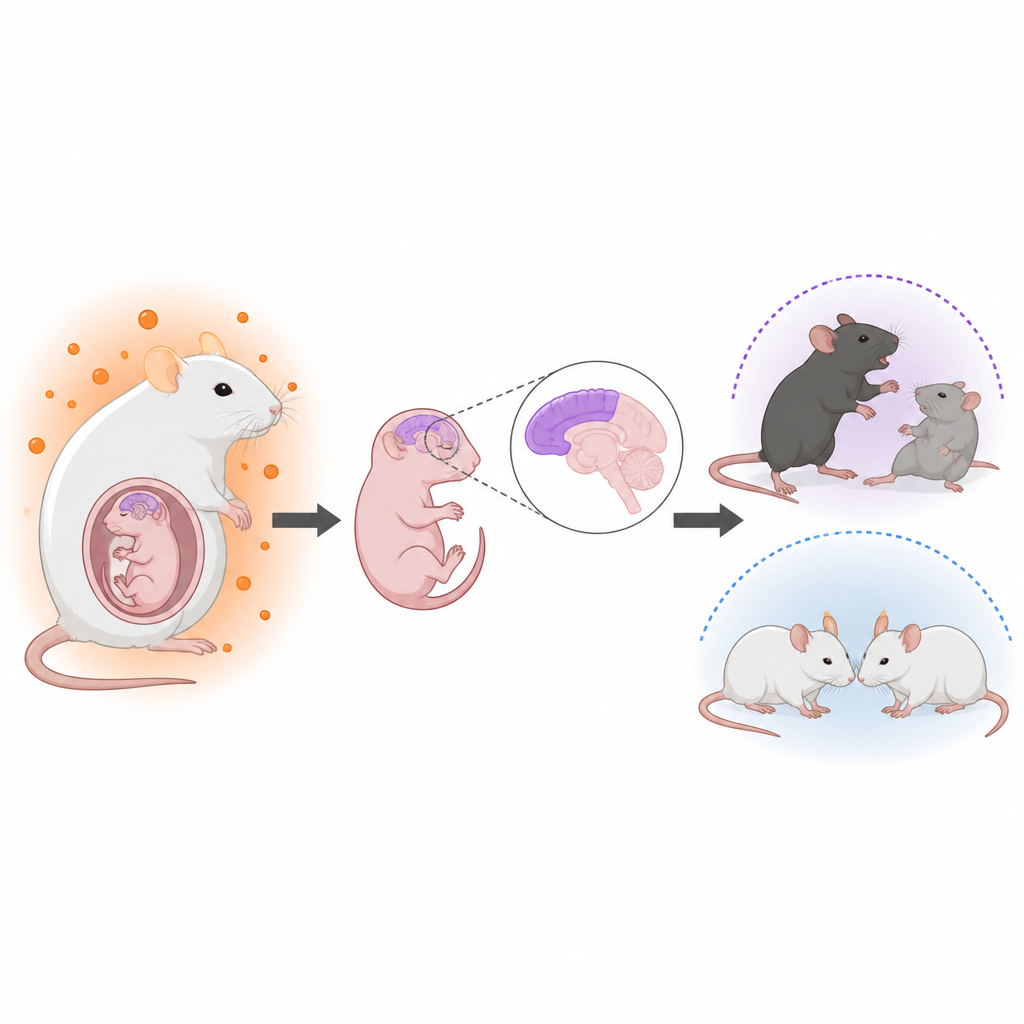
Hormone vor der Geburt und spätere Gehirngesundheit
Ärztinnen und Ärzte beobachten seit langem Zusammenhänge zwischen erhöhten Androgenen im Mutterleib und einer höheren Wahrscheinlichkeit für neuroentwicklungsbedingte Erkrankungen wie Autismus. Beispielsweise haben Frauen mit polyzystischem Ovarialsyndrom häufig erhöhte Androgenspiegel, und ihre Kinder zeigen ein leicht erhöhtes Autismusrisiko. Es war jedoch unklar, wie diese Hormone im fetalen Gehirn wirken oder warum Söhne stärker betroffen zu sein scheinen als Töchter. Die Autorinnen und Autoren entwickelten ein realistisches Mausmodell mütterlicher Hyperandrogenämie und verfolgten damit sowohl die Gehirnentwicklung als auch das Verhalten der Nachkommen.
Wie das Team die Hormonexposition modellierte
Die Forschenden behandelten trächtige Mäuse mit einem Arzneistoff, der Aromatase blockiert, das Enzym, das Testosteron normalerweise in Östrogen umwandelt. Dadurch stiegen die Testosteronspiegel bei den Müttern, in der Fruchtwässerschicht um die Föten und in den fetalen Gehirnen, ohne die Schwangerschaftsausgänge oder Geburtsgewichte insgesamt zu verändern. Mit genetischer Markierung und Mikroskopie konzentrierten sie sich auf den zerebralen Kortex, die äußere Hirnschicht, die Denken und soziales Verhalten trägt. Bei männlichen Nachkommen, bei weiblichen nur schwächer ausgeprägt, beobachteten sie, dass neuronale Stamm‑ und Vorläuferzellen verstärkt und früher Neuronen bildeten, während der Stammzellpool und einige spätere Zelltypen wie Astrozyten reduziert waren. Die normale geschichtete Anordnung kortikaler Neuronen wurde merklich weniger geordnet, obwohl die Gesamtgröße des Gehirns unverändert blieb.
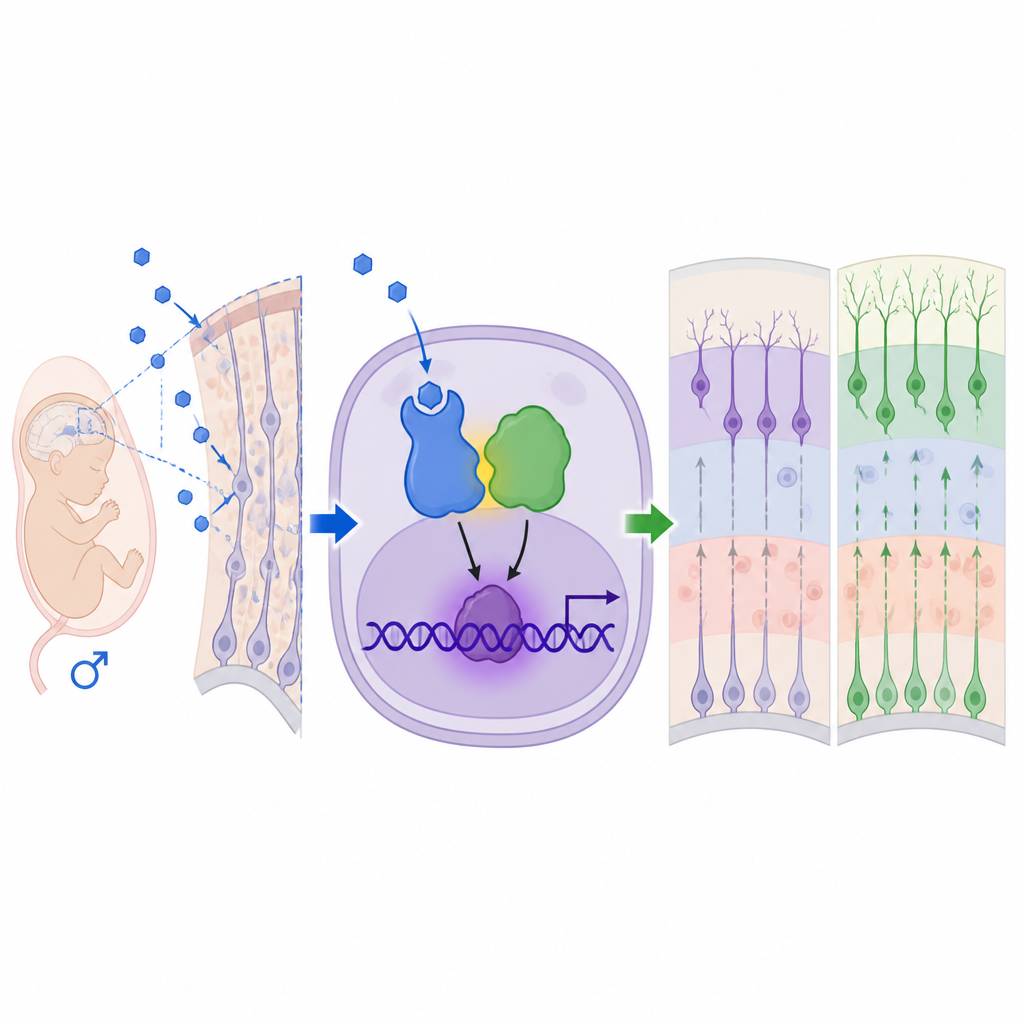
Vom veränderten Kortex zum veränderten Verhalten
Als Erwachsene zeigten männliche Nachkommen hyperandrogenischer Mütter Verhaltensunterschiede, die mehrere Merkmale widerspiegeln, die häufig bei Autismus beobachtet werden. In Sozialtests verbrachten diese Männchen weniger Zeit mit Interaktion mit anderen Mäusen und zeigten weniger Interesse an neuen Sozialpartnern, während ihre Aktivitätsniveaus normal blieben. Sie zeigten außerdem mehr repetitive Verhaltensweisen, etwa indem sie mehr Murmeln vergruben, und stärkere Angstzeichen in Open‑Field‑ und Elevated‑Plus‑Maze‑Tests. Weibliche Nachkommen, die denselben Bedingungen ausgesetzt und nach der Geburt zu Kontrollmüttern übergeben wurden, zeigten deutlich mildere oder gar keine solchen Verhaltensänderungen, was eine männliche Verwundbarkeit hervorhebt.
Ein unkonventioneller Weg innerhalb sich entwickelnder Gehirnzellen
Um zu verstehen, wie Androgene diese Effekte ausüben, betrachtete das Team die Androgenrezeptoren, die diese Hormone erkennen. Sie fanden höhere Spiegel und nukleäre Lokalisation des Androgenrezeptors im männlichen fetalen Kortex, und die Blockade dieses Rezeptors mit dem Arzneistoff Flutamid kehrte die überschießende Neurogenese und die meisten Verhaltensänderungen um. Genexpressionsanalysen wiesen auf MEF2C hin, einen Transkriptionsfaktor, der bereits mit neuroentwicklungsbedingten Störungen in Verbindung gebracht wurde, als wichtigen nachgeschalteten Zielpunkt. Überraschenderweise agierte der Androgenrezeptor nicht allein oder über seine üblichen DNA‑Andockstellen. Stattdessen bildete er physisch einen Komplex mit MeCP2, einem Protein, das von einem Gen auf dem X‑Chromosom kodiert wird und vor allem aus dem Rett‑Syndrom und dem MeCP2‑Duplikationssyndrom bekannt ist. Gemeinsam bildeten Androgenrezeptor und MeCP2 einen Aktivator‑Komplex, der an einer von MeCP2 erkannten Stelle in der Mef2c‑Regulationsregion band, MEF2C erhöhte und neuronale Stammzellen in Richtung Neuronen lenkte.
Was passiert, wenn MeCP2 selbst erhöht ist
Die Autorinnen und Autoren untersuchten anschließend ein Mausmodell mit einer zusätzlichen Kopie von MeCP2, das bereits zuvor erhöhte kortikale Neurogenese und autismusähnliche Verhaltensweisen gezeigt hatte. Sie stellten fest, dass diese MeCP2‑duplizierten Männchen ebenfalls erhöhtes MEF2C und ähnliche kortikale Veränderungen aufwiesen, selbst ohne zusätzliche pränatale Androgene. Eine Herunterregulierung von Mef2c oder die Blockade von Androgenrezeptoren in diesen Mäusen normalisierte die kortikale Schichtung und linderte viele der sozialen, repetitiven und angstähnlichen Verhaltensweisen. Das deutet darauf hin, dass ein Übermaß an MeCP2 denselben hormonempfindlichen Weg aktivieren kann und das männliche Risiko erhöht, wenn androgenetische Signale vorhanden sind.
Wie diese Arbeit unseren Blick auf Geschlechtsunterschiede verändert
Insgesamt zeigt die Studie einen bisher unerkannte n Weg, über den mütterliche Androgenexposition den männlichen fetalen Kortex und das spätere Verhalten formen kann. Anstatt nur über klassische Zielgene zu wirken, kann der Androgenrezeptor MeCP2 kapern, um MEF2C einzuschalten, wodurch das Gleichgewicht der Zellschicksale neuronaler Stammzellen verschoben und kortikale Schaltkreise subtil umverdrahtet werden. Da MeCP2 auf dem X‑Chromosom liegt und bereits in mehreren menschlichen neuroentwicklungsbedingten Syndromen eine Rolle spielt, bietet diese hormonempfindliche Partnerschaft eine greifbare molekulare Erklärung dafür, warum Jungen für bestimmte gehirnbasierte Erkrankungen anfälliger sein könnten. Zugleich legt sie nahe, dass sowohl genetische Faktoren als auch pränatale Hormonumgebungen gemeinsam betrachtet werden müssen.
Zitation: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
Schlüsselwörter: pränatale Androgene, MeCP2, kortikale Entwicklung, MEF2C, Autismusrisiko