Clear Sky Science · nl
MeCP2 bestuurt door maternale hyperandrogenisme veroorzaakte corticale afwijkingen en gedragsveranderingen via niet‑canonische AR‑afhankelijke regulatie van Mef2c
Waarom dit onderzoek van belang is voor gezinnen
Veel aandoeningen die leren, sociale vaardigheden en gedrag beïnvloeden komen vaker voor bij jongens dan bij meisjes, maar de redenen voor dit sekseverschil zijn nog onduidelijk. Deze studie gebruikt muizen om te onderzoeken hoe hoge niveaus van mannelijke hormonen tijdens de zwangerschap het zich ontwikkelende brein van mannelijke nakomelingen subtiel kunnen hervormen, en hoe een bekend herseneiwit, MeCP2, die hormonale signalen omzet in blijvende veranderingen in hersenstructuur en gedrag.
Hormonen vóór de geboorte en latere hersengezondheid
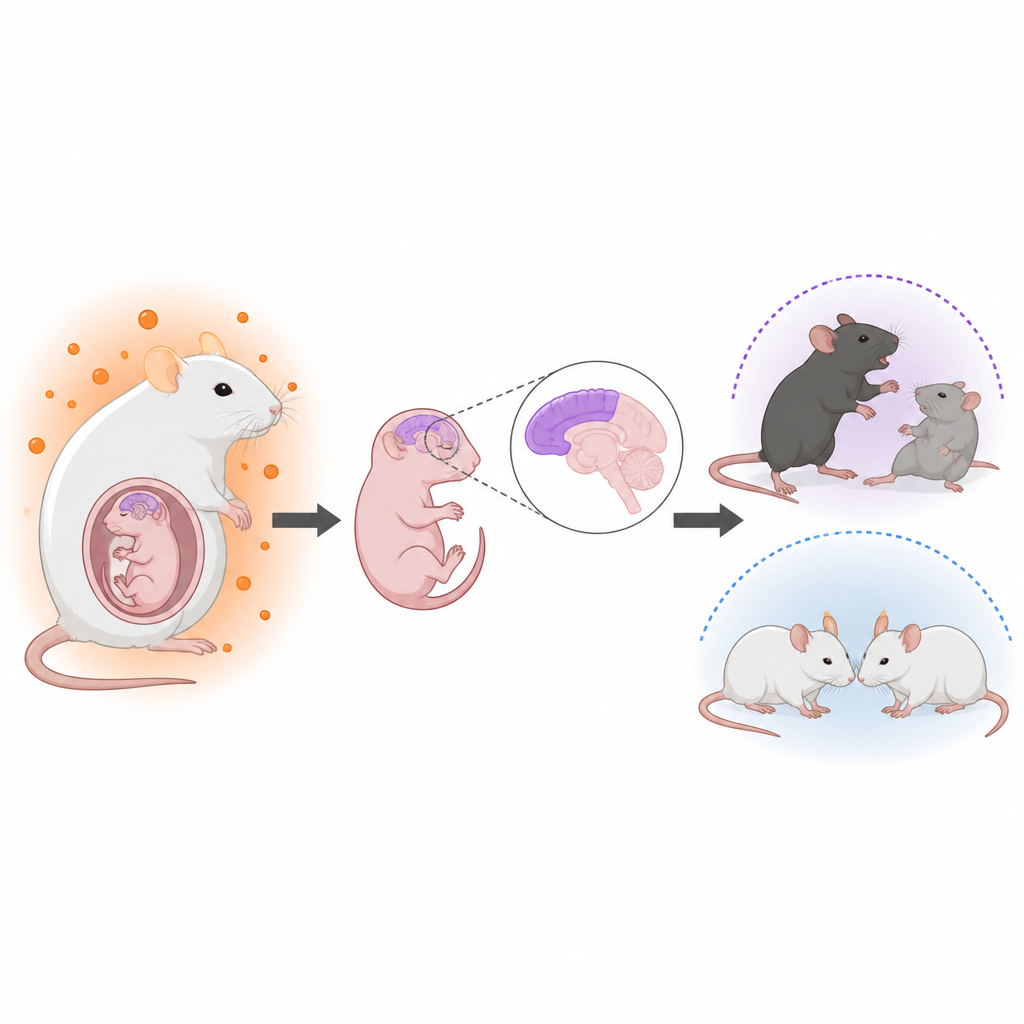
Artsen hebben al lang verbanden opgemerkt tussen verhoogde mannelijke hormonen in de baarmoeder en een hogere kans op neuroontwikkelingsstoornissen zoals autisme. Vrouwen met polycysteus-ovariumsyndroom hebben bijvoorbeeld vaak hogere androgenenwaarden en hun kinderen vertonen een licht verhoogd autisme‑risico. Het was echter onduidelijk hoe deze hormonen op het foetale brein inwerken of waarom zonen meer lijken te worden getroffen dan dochters. De auteurs maakten daarom een realistisch muismodel van maternale hyperandrogenie en volgden zowel hersenontwikkeling als gedrag bij de nakomelingen.
Hoe het team hormonale blootstelling nabootste
De onderzoekers behandelden drachtige muizen met een middel dat aromatase blokkeert, het enzym dat normaal testosteron omzet in oestrogeen. Dit verhoogde de testosteronspiegels bij de moeders, in het vruchtwater rond de foetussen en in de foetale hersenen, zonder de algemene zwangerschapsuitkomsten of geboortegesprekken te veranderen. Met genetische labeling en microscopie richtten zij zich op de cerebrale cortex, de buitenste laag van de hersenen die denken en sociaal gedrag ondersteunt. Bij mannelijke nakomelingen, en in mindere mate bij vrouwelijke, zagen ze dat neurale stam‑ en progenitorcellen eerder en in grotere aantallen neuronen produceerden, terwijl de voorraad stamcellen en sommige latere celtypen zoals astrocyten afnam. De normale gelaagde ordening van corticale neuronen raakte merkbaar minder ordelijk, hoewel de totale hersengrootte niet veranderde.
Van veranderde cortex naar afwijkend gedrag
Als volwassenen vertoonden mannelijke nakomelingen van hyperandrogene moeders gedragsverschillen die meerdere kenmerken weerspiegelen die vaak bij autisme worden gezien. In sociale tests brachten deze mannetjes minder tijd door met interactie met andere muizen en toonden ze minder interesse in nieuwe sociale partners, terwijl hun beweeglijkheid normaal bleef. Ze vertoonden ook meer repetitief gedrag, zoals het ingraven van meer knikkers, en sterkere aanwijzingen voor angst in open‑veld‑ en verhoogde plus‑mattests. Vrouwelijke nakomelingen, opgevoed onder dezelfde omstandigheden en na de geboorte overgeplaatst naar controlemoeders, lieten veel mildere of geen dergelijke gedragsveranderingen zien, wat de mannelijke kwetsbaarheid benadrukt.
Een niet‑standaard route binnen ontwikkelende hersencellen
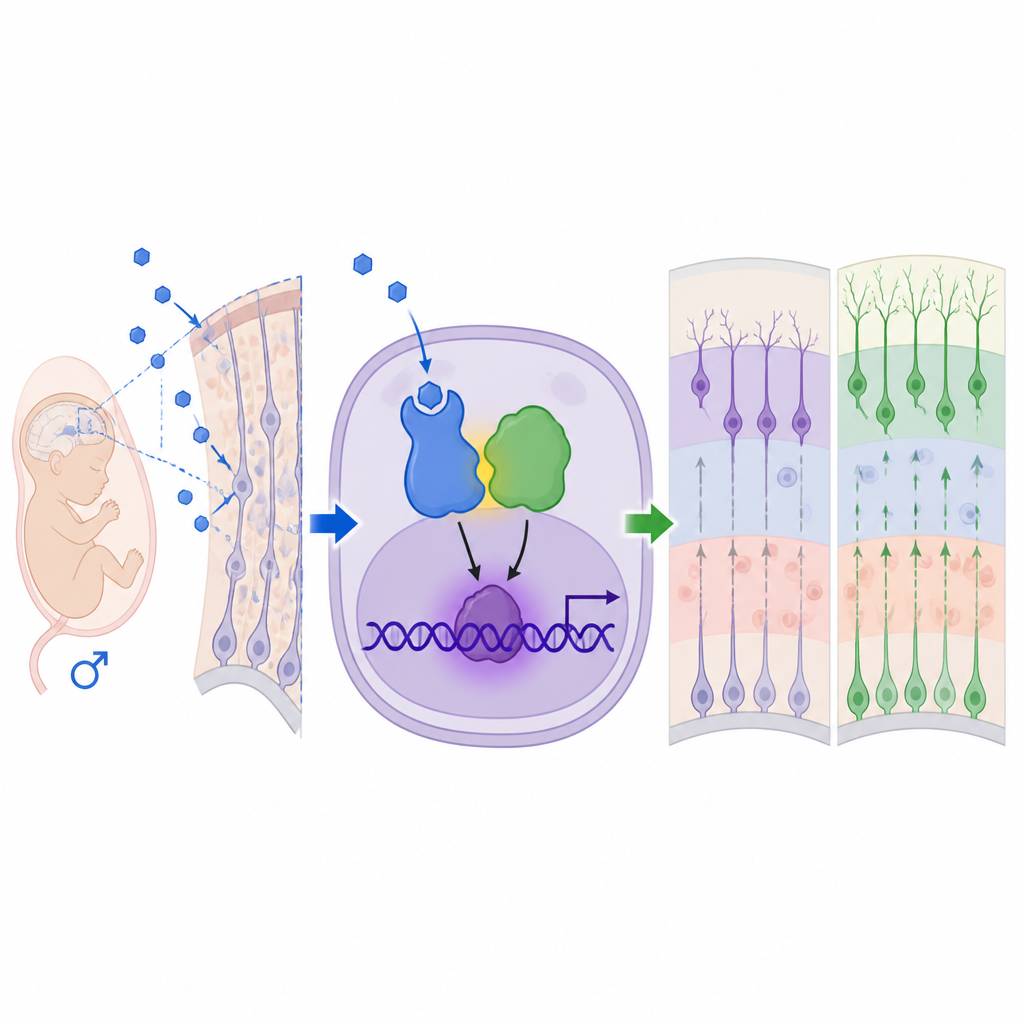
Om te begrijpen hoe androgenen deze effecten uitoefenen, zoomde het team in op androgenenreceptoren, de eiwitten die deze hormonen waarnemen. Ze vonden hogere niveaus en nucleaire lokalisatie van de androgenenreceptor in de mannelijke foetale cortex, en het blokkeren van deze receptor met het middel flutamide keerde de overmatige neurogenese en de meeste gedragsveranderingen om. Genexpressieanalyses wezen op MEF2C, een transcriptiefactor die al gekoppeld is aan neuro‑ontwikkelingsstoornissen, als een belangrijk downstream‑doel. Verrassend genoeg werkte de androgenenreceptor niet alleen of via zijn gebruikelijke DNA‑bindingsplaatsen. In plaats daarvan ging hij fysiek samen met MeCP2, een eiwit gecodeerd door een gen op het X‑chromosoom dat vooral bekend is van Rett‑syndroom en MeCP2‑duplicatiesyndroom. Samen vormden androgenenreceptor en MeCP2 een activatorcomplex dat bond op een door MeCP2 herkend element in het regulatorische gebied van Mef2c, waardoor MEF2C‑niveaus toenamen en neurale stamcellen naar neuronen werden gedreven.
Wat gebeurt er wanneer MeCP2 zelf verhoogd is
De auteurs gebruikten vervolgens een muismodel met een extra kopie van MeCP2, waarvan eerder was aangetoond dat het verhoogde corticale neurogenese en autisme‑achtige gedragingen veroorzaakt. Ze ontdekten dat deze MeCP2‑verdubbelde mannetjes ook verhoogde MEF2C‑waarden en vergelijkbare corticale veranderingen hadden, zelfs zonder extra prenatale androgenen. Het verlagen van Mef2c of het blokkeren van androgenenreceptoren in deze muizen normaliseerde de corticallayering en verzachtte veel van de sociale, repetitieve en angstachtige gedragingen. Dit suggereert dat te veel MeCP2 dezelfde hormoon‑gevoelige route kan inschakelen en het mannelijke risico versterkt wanneer androgenensignalen aanwezig zijn.
Hoe dit werk onze kijk op sekseverschillen verandert
Samengevat onthult de studie een voorheen ongekende route waarlangs maternale androgenenblootstelling de mannelijke foetale cortex en later gedrag kan vormen. In plaats van alleen via de klassieke doelwitten te werken, kan de androgenenreceptor MeCP2 kapen om MEF2C aan te zetten, waardoor het evenwicht van neurale stamcelmijlpaden verschuift en corticale circuits subtiel worden hervormd. Omdat MeCP2 op het X‑chromosoom ligt en al betrokken is bij verschillende menselijke neuro‑ontwikkelingssyndromen, biedt deze hormoongevoelige samenwerking een concrete moleculaire verklaring waarom jongens vatbaarder kunnen zijn voor bepaalde hersengerelateerde aandoeningen, en suggereert ze dat zowel genen als prenatale hormonale omgevingen samen moeten worden bekeken.
Bronvermelding: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
Trefwoorden: prenatale androgenen, MeCP2, corticale ontwikkeling, MEF2C, autisme risico