Clear Sky Science · he
MeCP2 שולט בפגמי קורטקס ושינויים התנהגותיים שנגרמים על ידי יתר אנדרוגנים אימהיים דרך ויסות לא-קנוני של Mef2c התלוי ב-AR
מדוע המחקר הזה חשוב למשפחות
מצבים רבים שמשפיעים על למידה, יכולות חברתיות והתנהגות שכיחים יותר בבנים מאשר בבנות, אך הסיבות להבדל המגדרי הזה עדיין לא ברורות. מחקר זה משתמש בעכברים כדי לחקור כיצד רמות גבוהות של הורמונים זכריים במהלך ההריון יכולות לעצב בעדינות את המוח המתפתח של צאצאים זכרים, וכיצד חלבון מוח ידוע, MeCP2, מסייע לתרגם אותות הורמונליים אלה לשינויים מתמשכים במבנה המוח ובהתנהגות.
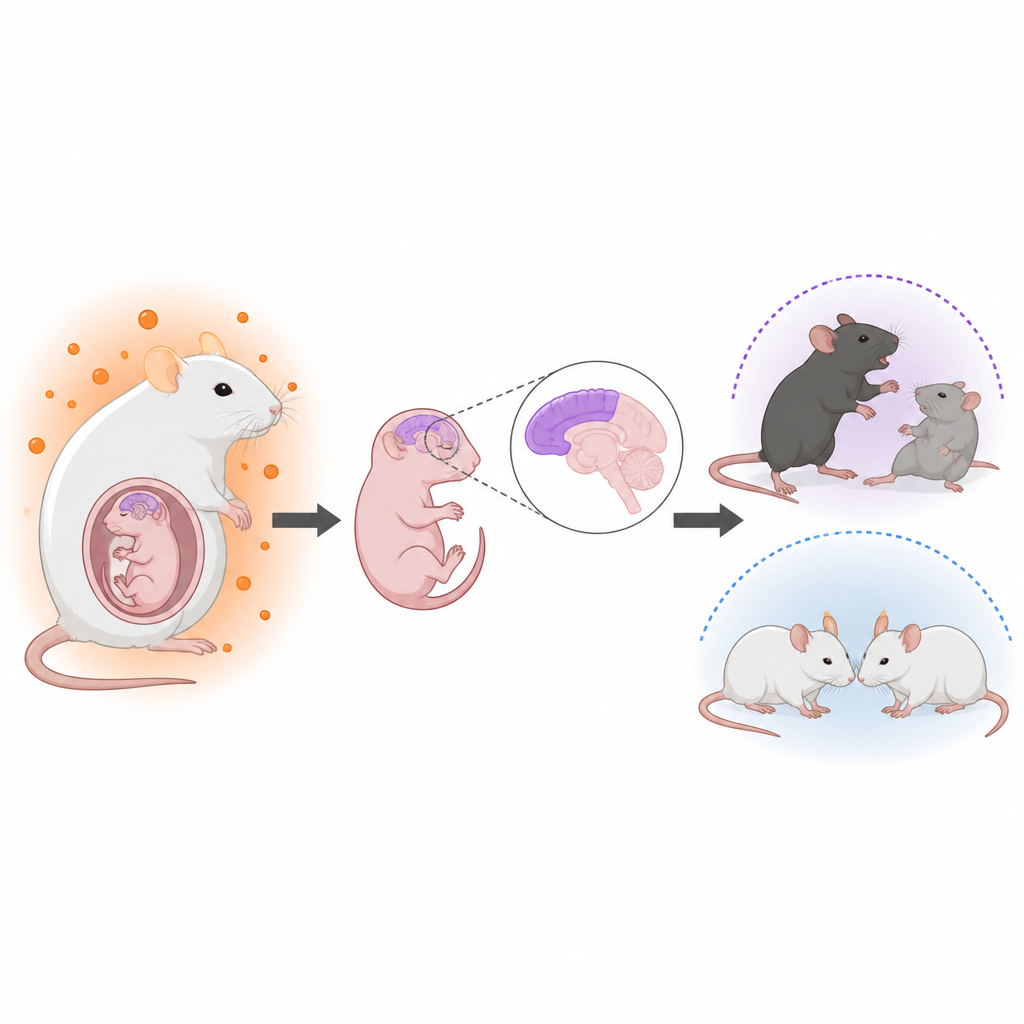
הורמונים לפני הלידה ובריאות המוח מאוחר יותר
רופאים כבר זמן רב שמים לב לקישורים בין רמות אנדרוגנים גבוהות ברחם לבין סבירות גבוהה יותר למצבים נוירו-התפתחותיים כגון אוטיזם. למשל, נשים עם תסמונת השחלות הפוליציסטית נוטות להיות עם רמות אנדרוגנים גבוהות יותר ובניהן נצפה סיכון מעט מוגבר לאוטיזם. עם זאת, לא היה ברור כיצד הורמונים אלה פועלים על מוח העובר או מדוע בני הם כאילו מושפעים יותר מבנות. החוקרים יצרו מודל עכבר ריאלי של היפראנדרוגניות אימהית ומעקבו אחר התפתחות המוח וההתנהגות בצאצאים.
כיצד הקבוצה סימלה חשיפה הורמונלית
החוקרים טיפלו בעכברות הרות בתרופה שחוסמת ארומטאז, האנזים שממיר בדרך כלל טסטוסטרון לאסטרוגן. כך עלו רמות הטסטוסטרון אצל האימהות, בנוזל העוברי ובמוחות העובריים, ללא שינוי בתוצאות ההריון או במשקל הלידה. באמצעות תיוג גנטי ומיקרוסקופיה הם התמקדו בקורטקס המוחי, השכבה החיצונית של המוח התומכת בחשיבה ובהתנהגות חברתית. אצל צאצאים זכרים, אך במידה קלה בלבד אצל נקבות, הם מצאו שתאי גזע נוירונליים ותאים פרוגניטוריים נדחפו ליצור נוירונים מוקדם יותר ובכמות גדולה יותר, בעוד מאגר תאי הגזע וכמה סוגי תאים מאוחרים יותר כגון אסטרוציטים פחתו. הסידור השכבתי הרגיל של הנוירונים הקורטיקליים הפך לפחות מסודר, אף על פי שלא נצפו שינויים בגודל המוח הכולל.
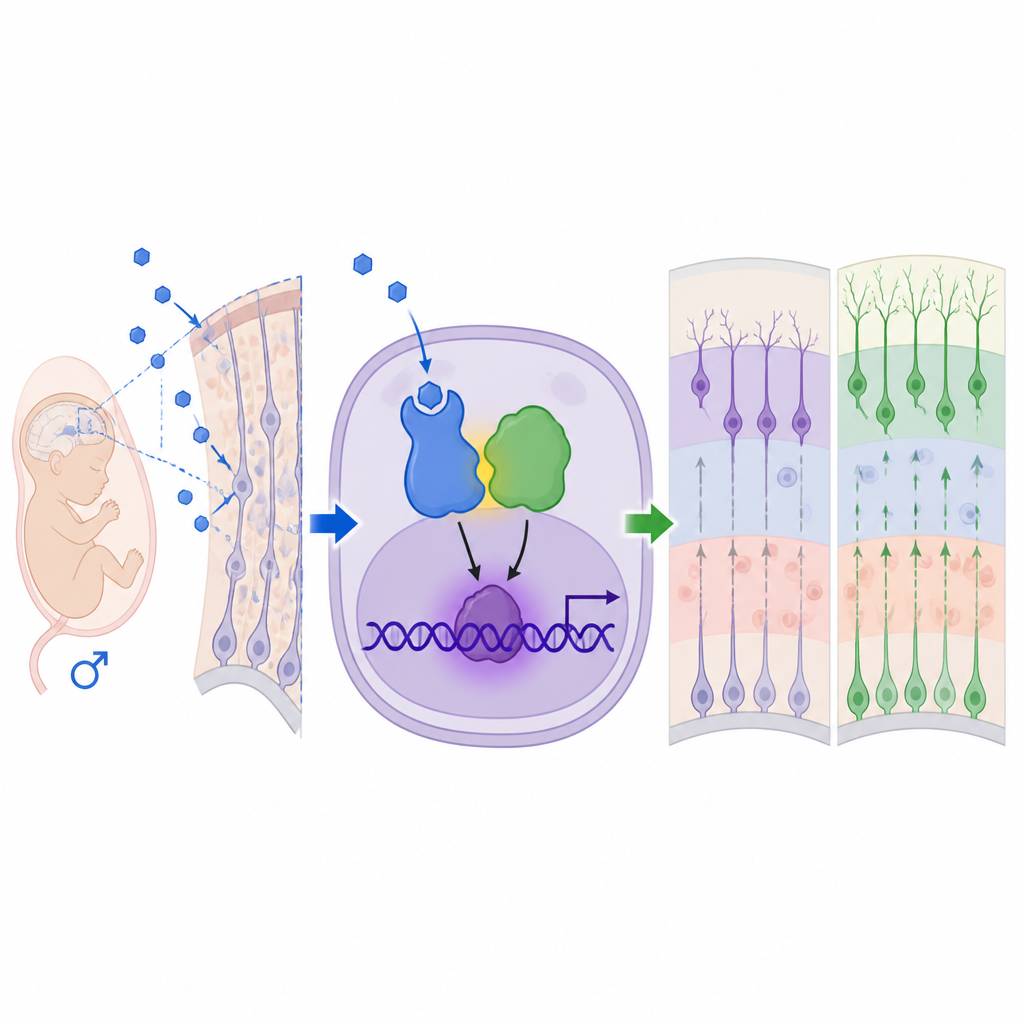
מקורטקס משתנה להתנהגות משתנה
בגיל בגרות, צאצאים זכרים מאימהות היפראנדרוגניות הראו הבדלים בהתנהגות המשקפים כמה תכונות שנצפות לעתים באוטיזם. בבדיקות חברתיות, זכרים אלה בילו פחות זמן באינטראקציה עם עכברים אחרים והציגו פחות עניין בדרך כלל בחברות חברתיות חדשות, בעוד שרמות התנועה שלהם נותרו תקינות. הם גם הראו יותר התנהגויות חזרתיות, כגון קבורת מספר גדול יותר של אבנים, וסימני חרדה חזקים יותר בבדיקות שדה פתוח ומבט גבוה. צאצאים נקבות, שנחשפו לאותן תנאים וגודלו אצל אימהות בקרה אחרי הלידה, הראו שינויים התנהגותיים קלים הרבה יותר או כלל לא, מה שמצביע על פגיעות מובהקת אצל זכרים.
נתיב לא סטנדרטי בתוך תאי מוח מתפתחים
כדי להבין כיצד אנדרוגנים מפעילים את ההשפעות הללו, הצוות התרכז בקולטני האנדרוגן, החלבונים החשים הורמונים אלה. הם מצאו רמות גבוהות יותר ומיקום גרעיני של קולטני האנדרוגן בקורטקס העוברי הזכרי, וחסימה של קולטנים אלה באמצעות התרופה פלוטמיד היפוכה את הנוירוגנזיס המוגבר ואת רוב השינויים ההתנהגותיים. ניתוחי ביטוי גנים הצביעו על MEF2C, פקטור שעתוק שכבר נקשר להפרעות נוירו-התפתחותיות, כמטרה מרכזית בדצנדנטה. בהפתעה, קולטני האנדרוגן לא פעלו לבדם או דרך את אתרי העיגון ה-DNA הרגילים שלהם. במקום זאת הם שקמו פיזית עם MeCP2, חלבון המקודד על כרומוזום X הידוע מתסמונת רט ומהכפלת MeCP2. יחד, קולטני האנדרוגן ו-MeCP2 בנו קומפלקס מפעיל שקשר באתר שמוכר על ידי MeCP2 באזור הבקרה של Mef2c, הגבירה את רמות MEF2C ודחפה תאי גזע נוירונליים לכיוון יצירת נוירונים.
מה קורה כאשר MeCP2 עצמו מוגבר
החוקרים עברו לאחר מכן למודל עכבר הנושא עותק נוסף של MeCP2, אשר קודם לכן הוצג כבעל נוירוגנזיס קורטיקלי מוגבר והתנהגויות דמויות אוטיזם. הם גילו שגם זכרים עם הכפלת MeCP2 הציגו רמות מוגברות של MEF2C ושינויים קורטיקליים דומים, גם ללא אנדרוגנים פרנאטליים נוספים. הפחתת Mef2c או חסימת קולטני אנדרוגן בעכברים אלה נורמלזה את השיכוב הקורטיקלי והקל על רבות מהתנהגויות חברתיות, חזרתיות וחרדתיות. ממצא זה מרמז שעודף MeCP2 יכול להפעיל את אותו נתיב הרגיש להורמונים, ולהגביר את הסיכון הייחודי לזכרים בזמן שנוכחים אותות אנדרוגניים.
כיצד עבודה זו משנה את השקפתנו על הבדלי המינים
בסך הכל, המחקר חושף מסלול שלא היה מוכר קודם לכן שבאמצעותו חשיפה אימהית לאנדרוגנים יכולה לעצב את הקורטקס העוברי הזכרי ואת ההתנהגות לאחר מכן. במקום לפעול רק דרך המטרות הקלאסיות שלו, קולטני האנדרוגן יכולים לחבור ל-MeCP2 כדי להפעיל את MEF2C, ובכך להטות את מאזן גורלות תאי הגזע הנוירונליים ולשנות בעדינות מעגלים קורטיקליים. מכיוון ש-MeCP2 נמצא על כרומוזום X וכבר מעורב במספר תסמונות נוירו-התפתחותיות בבני אדם, שותפות רגישת-הורמונים זו מציעה הסבר מולקולרי קונקרטי מדוע בנים עשויים להיות פגיעים יותר למצבים מוחיים מסוימים, ובו בזמן מרמזת כי גם גנים וגם סביבות הורמונליות פרה-נאטליות צריכים להילקח בחשבון יחד.
ציטוט: Wang, YM., Jia, Y., Wu, Y. et al. MeCP2 Governs maternal hyperandrogenism-induced cortical defects and behavioral alterations via noncanonical AR-dependent regulation of Mef2c. Nat Commun 17, 4225 (2026). https://doi.org/10.1038/s41467-026-72942-3
מילות מפתח: אנדרוגנים פרה-נאטליים, MeCP2, התפתחות קורטיקלית, MEF2C, סיכון לאוטיזם