Clear Sky Science · zh
技术与生物噪声源混淆了多路增强子 AAV 筛选
寻找合适的遗传钥匙
科学家越来越依赖将基因递送到特定脑细胞类型的病毒,以期用于基础研究和未来治疗。但要让这些工具精确工作,研究者必须附加合适的“开关”,即增强子,使每种病毒仅在目标细胞类型中被激活。本研究表明,当许多携带增强子的病毒在同一实验中一起测试时,隐藏的技术性和生物学噪声会严重模糊结果,使有前景的工具看起来远不如实际精确。
为什么细胞特异性基因控制很重要
增强子是帮助在特定细胞类型或脑区开启基因的短 DNA 片段。通过将这些增强子与腺相关病毒(AAV)耦合,科学家可以将荧光标记或治疗基因有针对性地递送到特定类型的神经元或支持性胶质细胞。传统上,每种增强子–AAV 组合在动物身上逐一测试——过程缓慢、费用高且难以扩展。多路复用方法承诺提供捷径:将许多不同条形码的增强子–AAV 混合,注入小鼠,然后使用单细胞 RNA 测序读取哪个增强子在何种细胞中被激活。理论上,这应当在一次实验中揭示数十种增强子的行为。
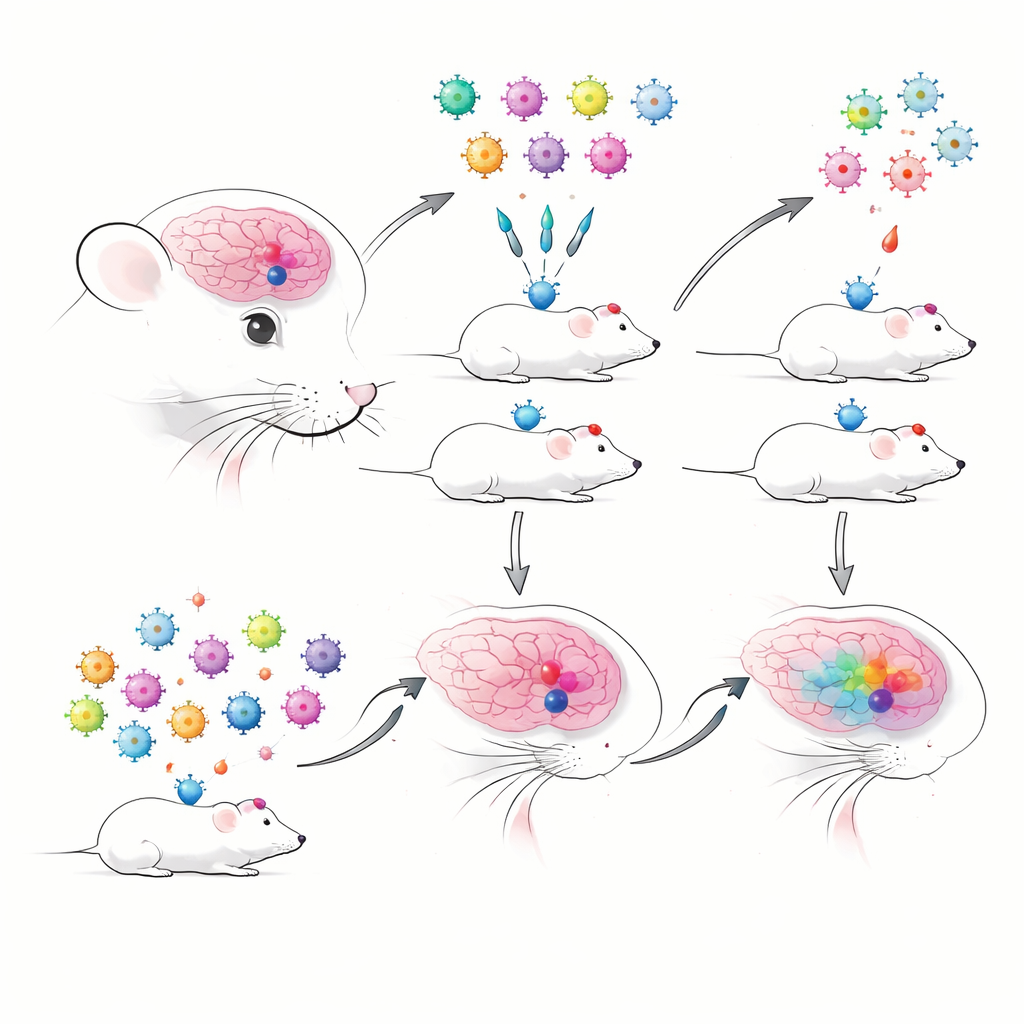
当许多试验共享一只小鼠时
作者首先构建了带条形码的 AAV,携带先前经良好表征且已知能高度标记特定脑细胞类型的增强子。每个增强子驱动一种荧光蛋白和一段短的 RNA 条形码标签,便于通过测序追踪。他们将传统的逐一注射与“多路复用”池注射进行比较,后者将许多增强子–AAV 一次性混合递送,并用基于微滴的单细胞 RNA 测序读取结果。很快,他们遇到一个实际难题:在基于细胞核的制备中——对冷冻或脆弱组织有用——病毒条形码检测得非常差,而全细胞制备能够更可靠地捕获病毒转录本。这迫使他们偏向使用全细胞制备,但全细胞更易碎,可能导致某些细胞类型代表性不足。
病毒基因组中的隐性混淆
即便改善了转录本捕获,多路复用筛选仍未重现逐一测试中那种清晰的细胞特异性模式。许多增强子在池内表现出远低于单独测试的选择性,尤其是那些本来较弱或靶向罕见细胞类型的增强子。为探究原因,团队比较了先单独包装再混合的病毒与从单一质粒池共同包装的病毒。使用长读长测序,他们发现共同包装产生了高比例的“嵌合”基因组——即增强子与条形码被打乱匹配的病毒粒子。这些嵌合粒子引入误导性条形码信号,降低了表观特异性。作者还探索了一种双条形码系统(“scQers”),每个病毒同时携带与表达相关的条形码和一个独立的构成性条形码。匹配这两种条形码对可以过滤掉部分错误读数并提高特异性,但仍不足以恢复逐一验证时的性能。
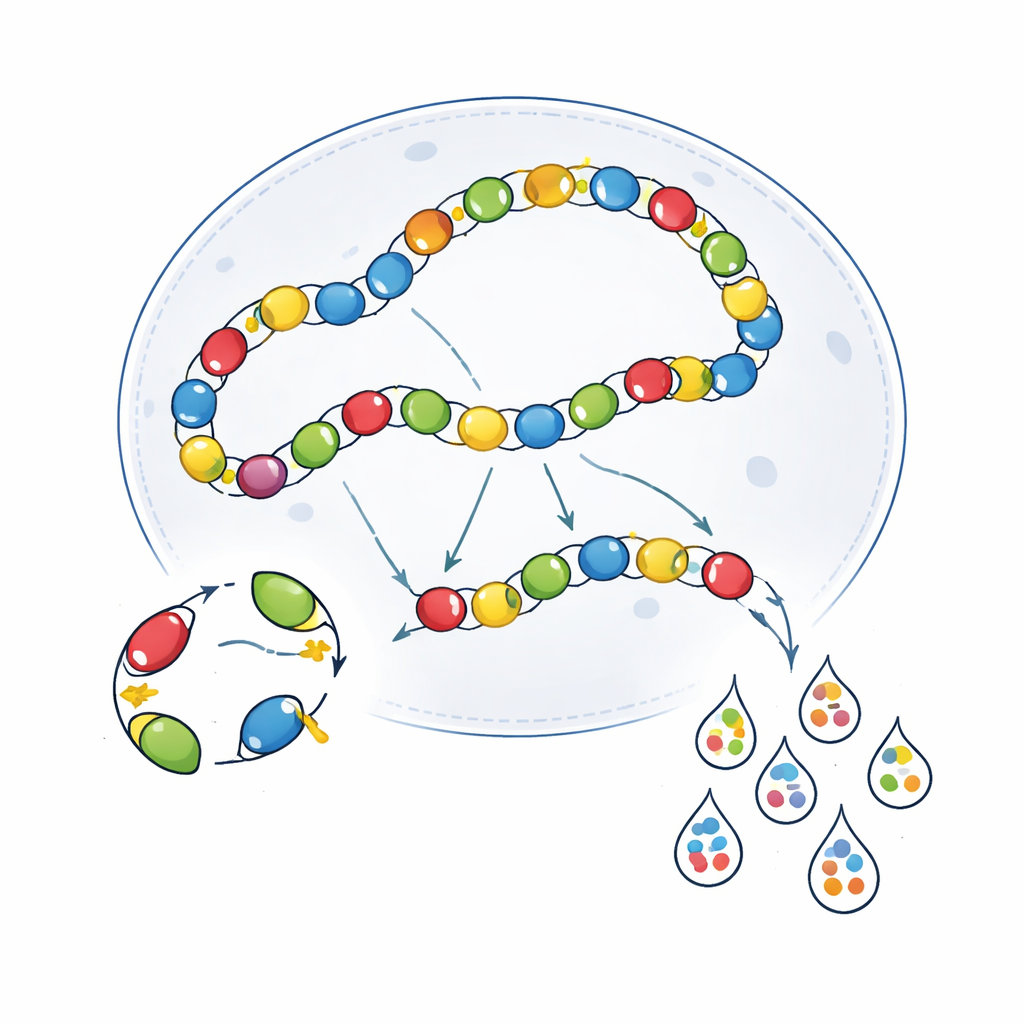
细胞内的生物学串扰
技术性伪影只是问题的一部分。病毒在细胞内的相互作用也会模糊结果。进入细胞核后,AAV 基因组常常首尾相接形成长链。在这种排列中,一个病毒基因组上的活性增强子可能无意间驱动相邻基因组的表达——这一现象称为转录性串扰。作者证明,当两种不同的增强子–AAV 共注入时,它们可能在单独存在时通常沉默的细胞类型中相互诱导活性。使用免疫缺陷的 SCID 小鼠(其 AAV 连接减少)在某些增强子上部分降低了这种重叠,但也削弱了整体表达,并未在各方面一致地提高特异性。试图用屏障 DNA 元件隔离病毒基因组也仅在特定背景下有益,在某些脑区有效而在其他区域无显著帮助。
为什么噪声对某些增强子影响更大
通过并排比较大量增强子,研究发现那些靶向丰富细胞类型并产生强荧光信号的增强子在多路复用条件下表现更好。弱增强子或在稀有细胞群中活跃的增强子更容易被嵌合基因组、串扰和杂散条形码产生的背景噪声淹没。重要的是,多路复用筛选中条形码转录本的计数与每个增强子单独测试时测得的蛋白水平相关性不佳,这表明池化实验中的大量条形码信号并不能忠实反映真实的增强子驱动活性。
这对未来脑部工具意味着什么
对非专业读者来说,结论是:将许多携带增强子的病毒合并到一只测试动物中比看上去更复杂。病毒在生产过程中可能重排,它们在细胞内会相互影响,并产生误导性的条形码信号,使精确的增强子显得不可靠。作者得出结论:目前的多路复用增强子 AAV 筛选还无法替代谨慎的逐一验证,尤其是在广泛搜索新的、精细靶向工具时。然而,规模较小且设计周密的池仍可用于对相似增强子进行排序或在投入全面验证之前优化设计。在大规模、无偏池化筛选能够可靠识别针对特定脑细胞类型的最佳遗传“钥匙”之前,还需要实质性的技术和生物学改进。
引用: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
关键词: 增强子 AAV, 基因递送, 单细胞 RNA 测序, 病毒条形码, 脑细胞类型