Clear Sky Science · de
Technische und biologische Rauschquellen verfälschen multiplexe Enhancer-AAV-Screenings
Die richtigen genetischen Schlüssel finden
Wissenschaftler verlassen sich zunehmend auf gentechnisch übertragende Viren, um bestimmte Gehirnzelltypen ein- oder auszuschalten, mit Blick sowohl auf Grundlagenforschung als auch mögliche Therapien. Damit diese Werkzeuge präzise wirken, müssen Forscher die passenden „Anschalter“ — sogenannte Enhancer — anfügen, damit jedes Virus nur in seinem Zielzelltyp aktiv wird. Diese Studie zeigt, dass bei gleichzeitiger Prüfung vieler solcher enhancer-ausgestatteten Viren in einem Experiment verborgene technische und biologische Störgeräusche die Ergebnisse stark verwischen können, sodass vielversprechende Werkzeuge deutlich ungenauer erscheinen, als sie tatsächlich sind.
Warum zell-spezifische Genkontrolle wichtig ist
Enhancer sind kurze DNA-Abschnitte, die helfen, Gene in bestimmten Zelltypen oder Hirnregionen einzuschalten. Durch die Kombination dieser Enhancer mit Adeno-assoziierten Viren (AAVs) können Forscher fluoreszente Marker oder therapeutische Gene gezielt in etwa einen bestimmten Neuronentyp oder unterstützende Gliazellen liefern. Üblicherweise wird jede Enhancer–AAV-Kombination einzeln in Tieren getestet — langsam, teuer und schwer zu skalieren. Multiplex-Verfahren versprechen eine Abkürzung: viele unterschiedlich barcodierte Enhancer-AAVs mischen, in eine Maus injizieren und dann mit Einzelzell-RNA-Sequenzierung ablesen, welcher Enhancer in welcher Zelle aktiv war. Theoretisch sollte so ein Experiment Dutzende Enhancer-Verhalten auf einmal zeigen.
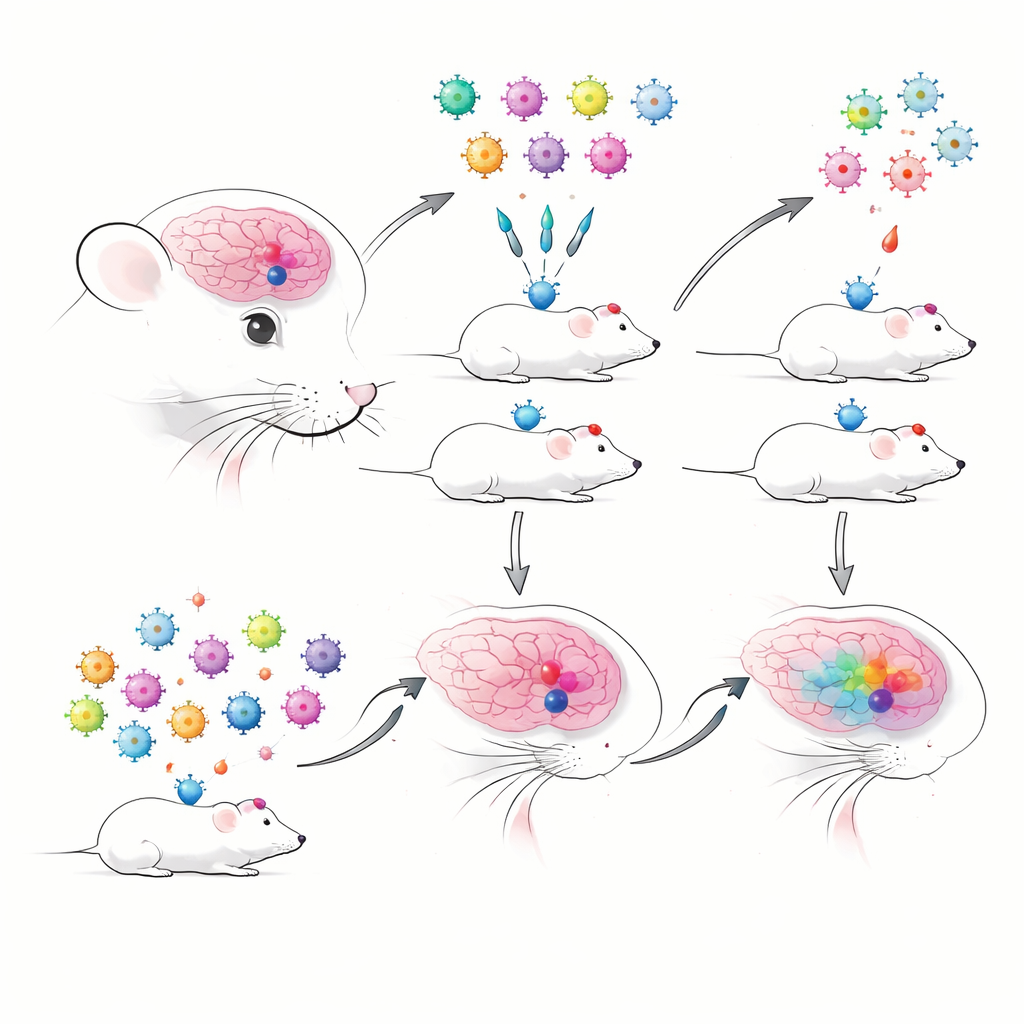
Wenn viele Experimente sich eine Maus teilen
Die Autoren begannen damit, barcodierte AAVs zu bauen, die zuvor gut charakterisierte Enhancer enthielten, von denen bekannt ist, dass sie bestimmte Gehirnzelltypen mit hoher Genauigkeit markieren. Jeder Enhancer trieb ein fluoreszierendes Protein und ein kurzes RNA-Barcode-Tag, was eine Verfolgung per Sequenzierung erlaubte. Sie verglichen traditionelle Einzelinjektionen mit gepoolten „Multiplex“-Injektionen, bei denen viele Enhancer-AAVs gleichzeitig verabreicht und mit droplet-basierter Einzelzell-RNA-Sequenzierung ausgelesen wurden. Gleich zu Beginn stießen sie auf ein praktisches Problem: in nuclei-basierten Präparationen — nützlich für gefrorene oder empfindliche Gewebe — wurden die viralen Barcodes sehr schlecht detektiert, während Ganzzell-Präparationen virale Transkripte deutlich zuverlässiger erfassten. Das zwang sie, Ganzzellen zu bevorzugen, die jedoch fragiler sein können und einige Zelltypen unterrepräsentieren könnten.
Versteckte Vertauschungen in viralen Genomen
Selbst mit besserer Transkript-Erfassung reproduzierten Multiplex-Screenings nicht die klaren, zell-spezifischen Muster, die in Einzeltests beobachtet wurden. Viele Enhancer erschienen deutlich weniger selektiv, besonders jene, die von Natur aus schwächer sind oder seltene Zelltypen anvisieren. Um das zu untersuchen, verglich das Team Viren, die einzeln verpackt und dann gemischt wurden, mit Viren, die gemeinsam aus einer einzigen Plasmid-Pool verpackt wurden. Mithilfe von Langread-Sequenzierung entdeckten sie, dass die gepoolte Verpackung eine hohe Rate an „chimerischen“ Genomen erzeugte — virale Partikel, in denen Enhancer und Barcode durcheinandergeraten und falsch zugeordnet wurden. Diese chimären Partikel fügen irreführende Barcode-Signale hinzu und senken die scheinbare Spezifität. Die Autoren untersuchten auch ein Dual-Barcoding-System („scQers“), bei dem jedes Virus sowohl einen expressions-gekoppelten Barcode als auch einen separaten konstitutiven Barcode trägt. Das Abgleichen dieser Paare erlaubte es, einige fehlerhafte Reads herauszufiltern und die Spezifität zu verbessern, jedoch nicht genug, um die Leistung der Einzelvalidierung wiederherzustellen.
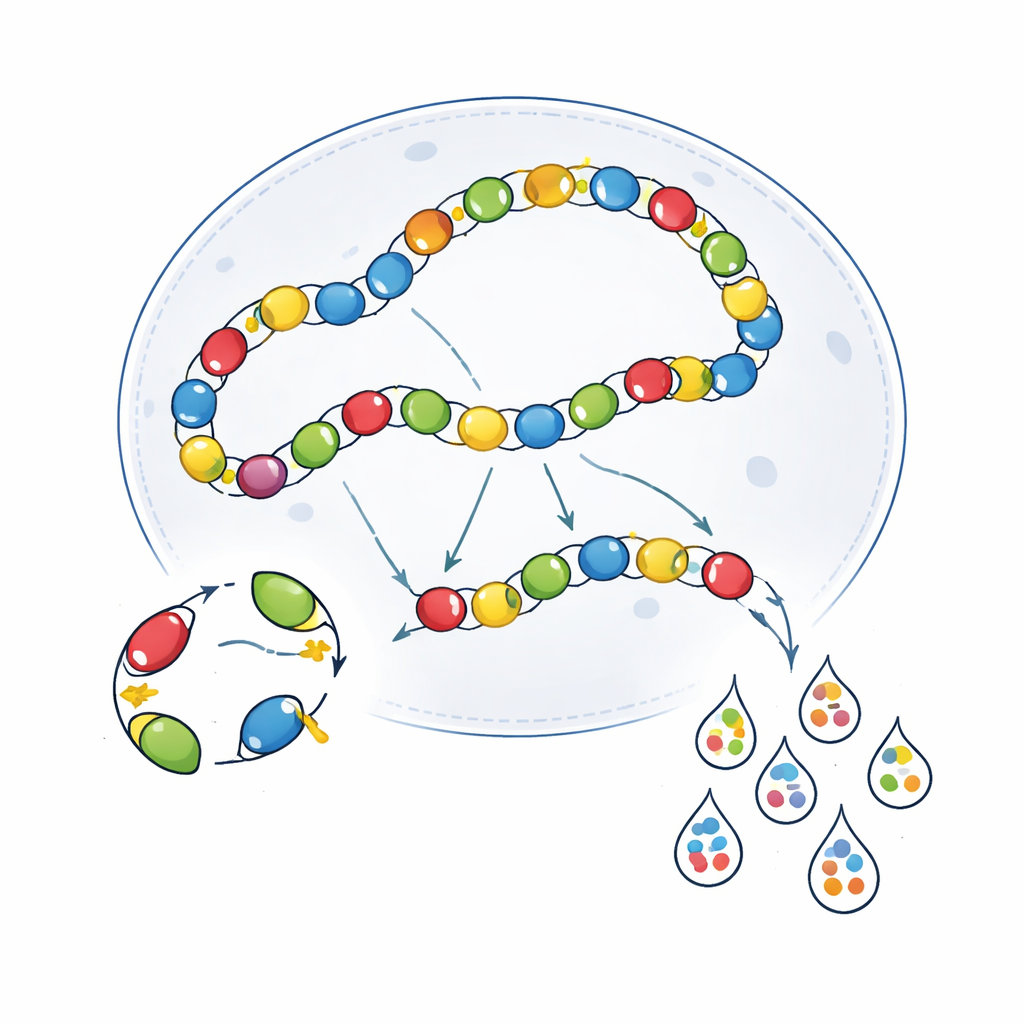
Biologisches Crosstalk innerhalb von Zellen
Technische Artefakte waren nur ein Teil des Problems. Die Viren interagieren auch innerhalb von Zellen auf Weisen, die das Bild verwischen. Einmal im Zellkern, verknüpfen sich AAV-Genome häufig ende-zu-ende und bilden lange Ketten. In dieser Anordnung kann ein aktiver Enhancer auf einem viralen Genom unbeabsichtigt die Expression eines benachbarten Genoms antreiben — ein Phänomen, das als transkriptionales Crosstalk bezeichnet wird. Die Autoren zeigten, dass, wenn zwei verschiedene Enhancer-AAVs ko-injiziert wurden, sie sich gegenseitig in Zelltypen aktivieren konnten, in denen einer allein normalerweise still wäre. Die Verwendung immundefizienter SCID-Mäuse, die eine reduzierte AAV-Konkatenation aufweisen, verringerte diese Überlappung für einige Enhancer teilweise, schwächte aber auch die Gesamtexpression und verbesserte die Spezifität nicht konsequent. Versuche, virale Genome mit Barrieredna-Elementen zu isolieren, zeigten ebenfalls nur kontextabhängige Vorteile — hilfreich in manchen Hirnregionen, nicht aber in allen.
Warum Rauschen einige Enhancer stärker trifft
Durch den direkten Vergleich vieler Enhancer nebeneinander fanden die Autoren, dass solche, die auf häufige Zelltypen zielen und starke Fluoreszenzsignale erzeugen, unter multiplexen Bedingungen besser abschnitten. Schwache Enhancer oder solche, die in seltenen Zellpopulationen aktiv sind, wurden überproportional durch Hintergrundrauschen aus chimären Genomen, Crosstalk und verstreuten Barcodes überdeckt. Wichtig ist, dass die Anzahl der Barcode-Transkripte in Multiplex-Screens nicht gut mit den Proteinmengen korrelierte, die bei Einzeltests gemessen wurden, was darauf hindeutet, dass ein großer Teil des Barcode-Signals in gepoolten Experimenten nicht zuverlässig die tatsächliche enhancer-getriebene Aktivität widerspiegelt.
Was das für künftige Werkzeuge fürs Gehirn bedeutet
Für Nicht-Spezialisten lautet die Quintessenz: Viele enhancer-ausgestattete Viren in einem einzelnen Testtier zu kombinieren, ist komplizierter als es scheint. Die Viren können sich während der Produktion umordnen, innerhalb der Zellen miteinander „kommunizieren“ und irreführende Barcode-Signale erzeugen, die präzise Enhancer unförmig erscheinen lassen. Die Autoren schließen, dass derzeitige multiplexe Enhancer-AAV-Screenings noch nicht die sorgfältige Einzelvalidierung ersetzen können, insbesondere wenn breit nach neuen, fein zielgerichteten Werkzeugen gesucht wird. Kleinere, wohlüberlegte Pools können jedoch weiterhin nützlich sein, um ähnliche Enhancer zu ranken oder Designs zu optimieren, bevor man in vollständige Validierung investiert. Erhebliche technische und biologische Verbesserungen werden erforderlich sein, bevor große, unverzerrte gepoolte Screenings zuverlässig die besten genetischen „Schlüssel“ zur Zielsteuerung spezifischer Gehirnzelltypen aufdecken können.
Zitation: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
Schlüsselwörter: Enhancer AAV, Gentransfer, Einzelzell-RNA-Sequenzierung, virales Barcoding, Gehirnzelltypen