Clear Sky Science · es
Fuentes técnicas y biológicas de ruido confunden el cribado multiplexado de potenciadores en AAV
Encontrar las llaves genéticas adecuadas
Los científicos recurren cada vez más a virus que entregan genes para activar o silenciar tipos celulares específicos del cerebro, con expectativas tanto para la investigación básica como para terapias futuras. Pero para que estas herramientas sean precisas, los investigadores deben acoplar los “interruptores” correctos, llamados potenciadores, de modo que cada virus se active solo en el tipo celular previsto. Este estudio muestra que cuando muchos de estos virus equipados con potenciadores se prueban juntos en un solo experimento, el ruido técnico y biológico oculto puede emborronar gravemente los resultados, haciendo que herramientas prometedoras parezcan mucho menos precisas de lo que realmente son.
Por qué importa el control génico específico por célula
Los potenciadores son fragmentos cortos de ADN que ayudan a activar genes en tipos celulares o regiones cerebrales particulares. Al acoplar estos potenciadores a virus adenoasociados (AAV), los científicos pueden entregar marcadores fluorescentes o genes terapéuticos específicamente a, por ejemplo, cierto tipo de neurona o célula glial de soporte. Tradicionalmente, cada combinación potenciador–AAV se prueba una por una en animales: un proceso lento, costoso y difícil de escalar. Los enfoques multiplexados prometen un atajo: mezclar muchos AAV potenciadores con códigos de barras diferentes, inyectarlos en un ratón y luego usar secuenciación de ARN unicelular para leer qué potenciador estuvo activo en cada célula. En teoría, esto debería revelar docenas de comportamientos de potenciadores en un solo experimento.
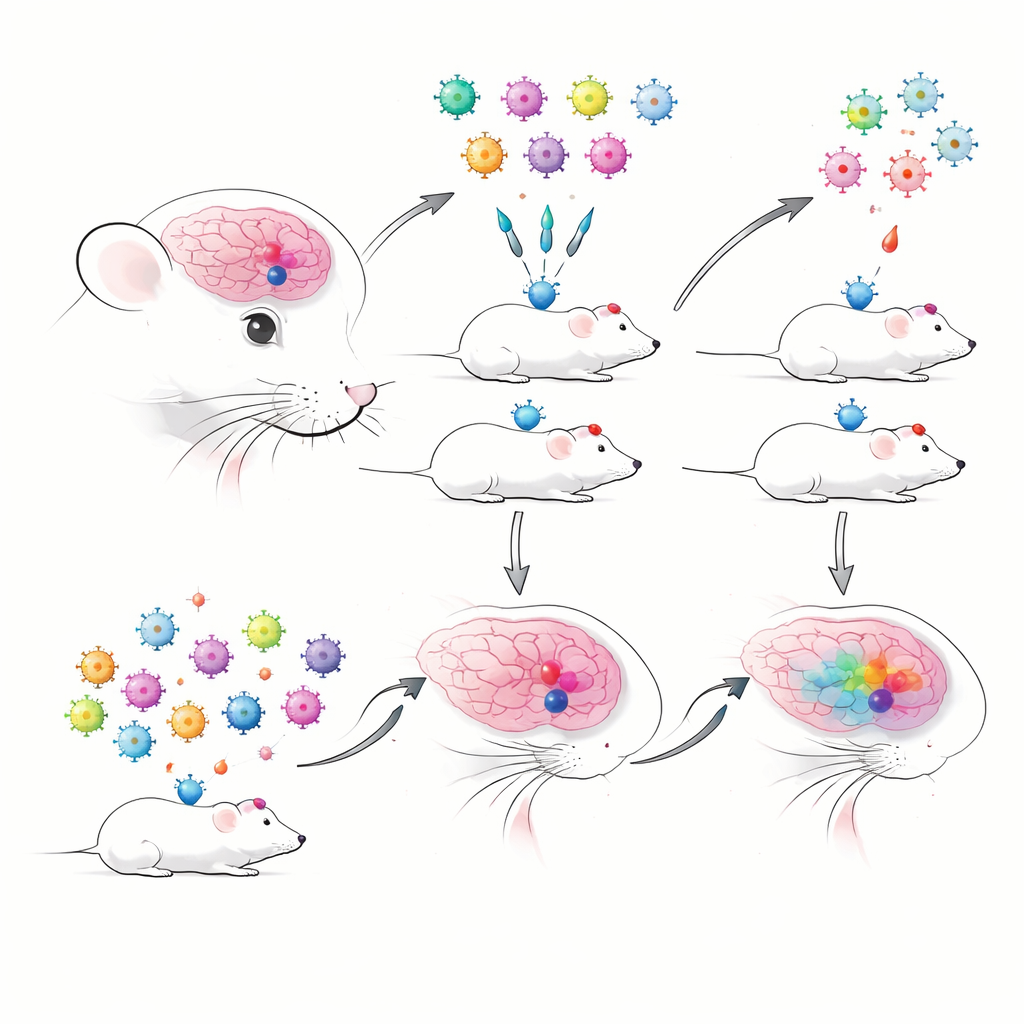
Cuando muchos experimentos comparten un solo ratón
Los autores comenzaron construyendo AAV con códigos de barras que portaban potenciadores previamente bien caracterizados, conocidos por etiquetar tipos celulares cerebrales específicos con alta precisión. Cada potenciador dirigía una proteína fluorescente y una etiqueta de ARN corta con código de barras, lo que permitía su seguimiento por secuenciación. Compararon inyecciones tradicionales una por una con inyecciones “multiplex” agrupadas, donde muchos AAV potenciadores se administraron a la vez y se leyeron mediante secuenciación de ARN unicelular basada en gotas. Desde el principio se toparon con un obstáculo práctico: en preparaciones basadas en núcleos —útiles para tejidos congelados o delicados— las etiquetas virales se detectaron muy mal, mientras que las preparaciones de células enteras capturaron los transcriptos virales con mucha más fiabilidad. Esto les obligó a favorecer células enteras, que pueden ser más frágiles y subrepresentar algunos tipos celulares.
Mezclas ocultas en los genomas virales
Incluso con una mejor captura de transcriptos, las pantallas multiplexadas no reprodujeron los patrones nítidos y específicos por célula observados en las pruebas una por una. Muchos potenciadores parecían mucho menos selectivos, especialmente aquellos que eran naturalmente más débiles o que apuntaban a tipos celulares raros. Para investigar, el equipo comparó virus empaquetados individualmente y luego mezclados, frente a virus empaquetados juntos a partir de una única mezcla de plásmidos. Mediante secuenciación de lectura larga, descubrieron que el empaquetado en pool producía una alta tasa de genomas “quiméricos”: partículas virales en las que potenciador y código de barras se habían mezclado y emparejado mal. Estas partículas quiméricas añaden señales de código de barras engañosas y reducen la especificidad aparente. Los autores también exploraron un sistema de doble codificación (“scQers”), en el que cada virus llevaba tanto un código de barras ligado a la expresión como un código de barras constitutivo separado. Emparejar estas dos marcas permitió filtrar algunas lecturas erróneas y mejoró la especificidad, pero no lo suficiente como para recuperar el rendimiento de la validación individual.
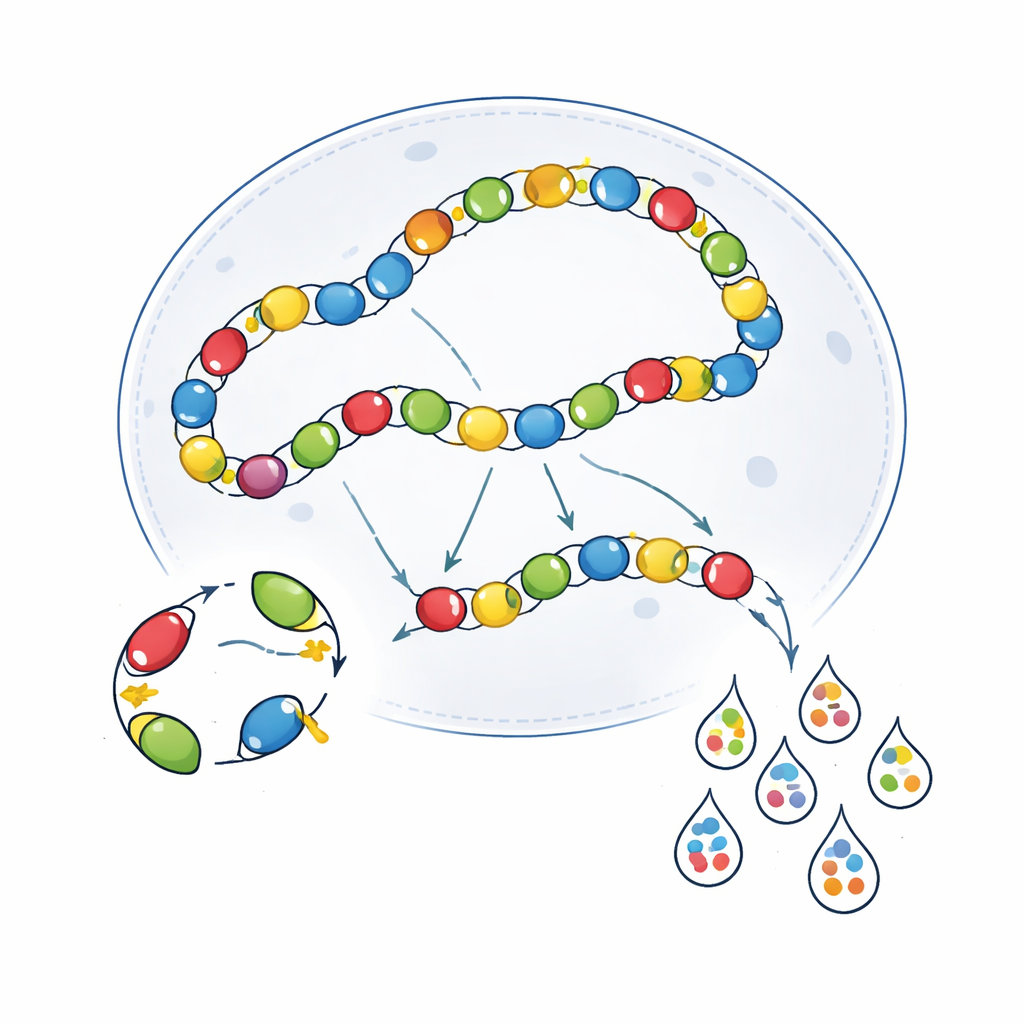
Interferencias biológicas dentro de las células
Los artefactos técnicos fueron solo una parte del problema. Los propios virus interactúan dentro de las células de formas que emborronan el panorama. Una vez en el núcleo, los genomas de AAV con frecuencia se enlazan extremo con extremo, formando largas cadenas. En esta disposición, un potenciador activo en un genoma viral puede, de forma inadvertida, impulsar la expresión de un genoma vecino: un fenómeno llamado interferencia transcripcional. Los autores demostraron que cuando se coinyectaban dos AAV potenciadores diferentes, podían estimular la actividad del otro en tipos celulares donde uno solo normalmente estaría inactivo. El uso de ratones SCID inmunodeficientes, que presentan menor concatenación de AAV, redujo parcialmente esta superposición para algunos potenciadores, pero también debilitó la expresión global y no mejoró de manera consistente la especificidad en todos los casos. Los intentos de aislar los genomas virales con elementos de barrera de ADN mostraron asimismo beneficios dependientes del contexto, ayudando en algunas regiones del cerebro pero no en otras.
Por qué el ruido afecta más a algunos potenciadores
Al comparar muchos potenciadores lado a lado, el estudio encontró que aquellos dirigidos a tipos celulares abundantes y que producían señales fluorescentes fuertes se comportaron mejor en condiciones multiplexadas. Los potenciadores débiles o los activos en poblaciones celulares raras quedaron desproporcionadamente ahogados por el ruido de fondo originado en genomas quiméricos, interferencias y códigos de barras residuales. Es importante destacar que el recuento de transcriptos de código de barras en pantallas multiplexadas no se correlacionó bien con los niveles de proteína medidos cuando cada potenciador se probó por separado, lo que sugiere que gran parte de la señal de código de barras en experimentos agrupados no refleja fielmente la verdadera actividad dirigida por el potenciador.
Qué implica esto para futuras herramientas cerebrales
Para no especialistas, la conclusión es que combinar muchos virus con potenciadores en una sola prueba animal es más complicado de lo que parece. Los virus pueden reorganizarse durante la producción, comunicarse entre sí dentro de las células y generar señales de código de barras engañosas que hacen que potenciadores precisos parezcan imprecisos. Los autores concluyen que el cribado multiplexado actual de potenciadores en AAV aún no puede sustituir a la validación cuidadosa uno por uno, especialmente cuando se busca de forma amplia nuevas herramientas finamente dirigidas. Sin embargo, grupos pequeños y diseñados con criterio pueden seguir siendo útiles para clasificar potenciadores similares u optimizar diseños antes de comprometerse con una validación completa. Serán necesarias mejoras técnicas y biológicas sustanciales antes de que las grandes pantallas agrupadas y no sesgadas puedan revelar de forma fiable las mejores “llaves” genéticas para orientar tipos celulares cerebrales específicos.
Cita: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
Palabras clave: AAV potenciador, entrega de genes, secuenciación de ARN unicelular, codificación viral, tipos de células cerebrales