Clear Sky Science · ru
Технические и биологические источники шума искажают результаты мультиплексного скрининга усиливающих элементов с помощью AAV
Поиск подходящих генетических ключей
Учёные всё чаще используют вирусы для доставки генов, чтобы включать или выключать определённые типы клеток мозга — это важно и для фундаментальных исследований, и для потенциальных терапий. Но чтобы эти инструменты работали точно, к каждому вирусу нужно присоединить подходящий «переключатель» — усилитель — чтобы он активировался только в нужном типе клеток. В этом исследовании показано, что при одновременной проверке многих таких усилителей в одном эксперименте скрытые технические и биологические источники шума могут сильно размывать результаты, из‑за чего перспективные инструменты кажутся гораздо менее специфичными, чем они есть на самом деле.
Почему важно клеточно‑специфичное генетическое управление
Усилители — это короткие участки ДНК, которые помогают включать гены в определённых типах клеток или областях мозга. Комбинируя эти усилители с адено‑ассоциированными вирусами (AAV), исследователи могут доставлять флуоресцентные метки или терапевтические гены именно в, например, определённый тип нейронов или вспомогательных глиальных клеток. Традиционно каждую комбинацию усилитель‑AAV тестируют отдельно в животных — это медленно, дорого и тяжело масштабируется. Мультиплексные подходы обещают ускорение: смешать много по-разному баркодированных усилитель‑AAV, ввести их в мышь и затем с помощью секвенирования РНК отдельных клеток определить, какой усилитель был активен в какой клетке. В теории это должно раскрыть поведение десятков усилителей в одном эксперименте.
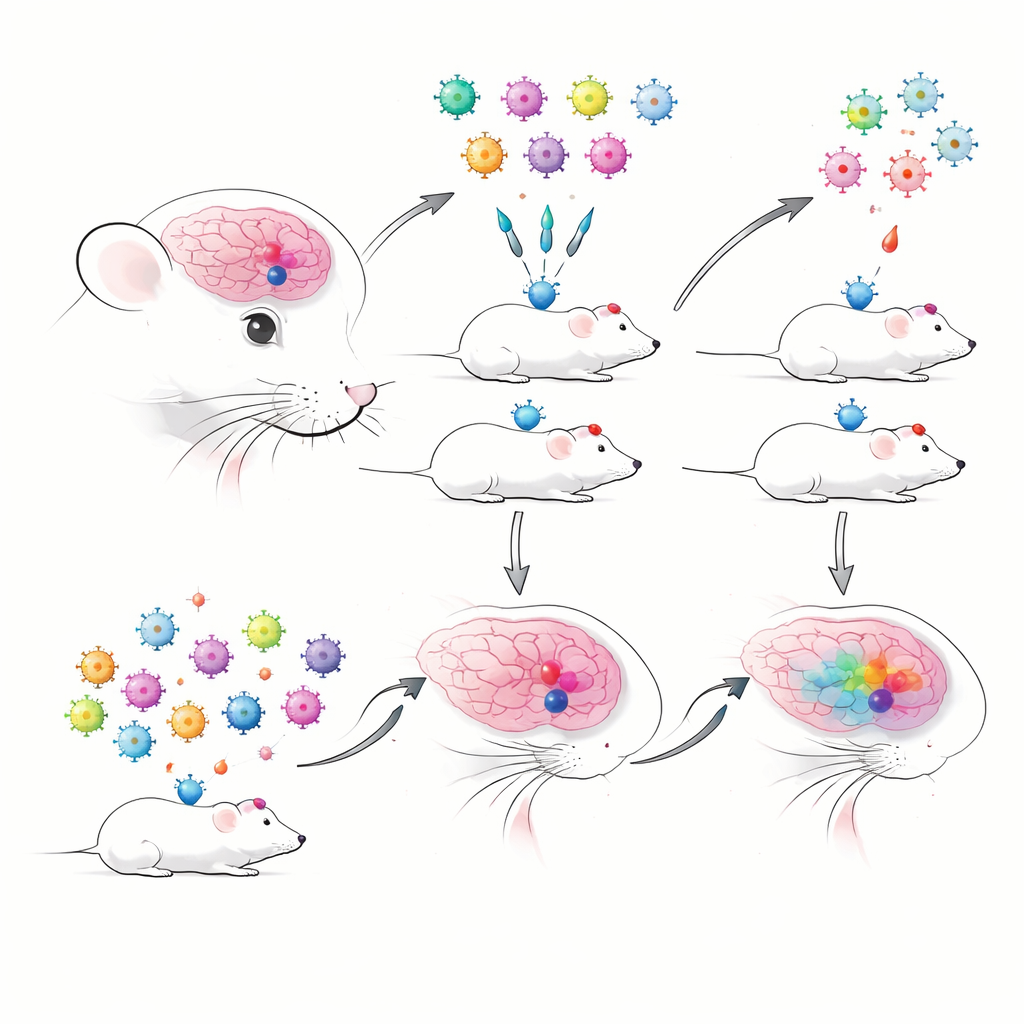
Когда многие эксперименты делят одну мышь
Авторы начали с создания баркодированных AAV, несущих ранее хорошо охарактеризованные усилители, которые надежно маркируют конкретные типы клеток мозга. Каждый усилитель приводил в действие флуоресцентный белок и короткий РНК‑баркод, что позволяло отслеживать их с помощью секвенирования. Они сравнили традиционные отдельные инъекции с пулом «мультиплексных» инъекций, где многие усилитель‑AAV вводились одновременно и читаются с помощью капельно‑основанного секвенирования РНК отдельных клеток. Сразу же возник практический затор: в препаратах на основе ядер — полезных для замороженных или деликатных тканей — вирусные баркоды обнаруживались очень плохо, тогда как в препаратах из цельных клеток вирусные транскрипты улавливались гораздо надёжнее. Это заставило отдать предпочтение целым клеткам, которые более хрупки и могут недопредставлять некоторые типы клеток.
Скрытые путаницы в вирусных геномах
Даже при лучшем захвате транскриптов мультиплексные скрининги не воспроизводили чётких клеточно‑специфичных паттернов, наблюдаемых при по‑отдельности тестах. Многие усилители выглядели гораздо менее селективными, особенно те, которые по природе своей слабее или нацелены на редкие типы клеток. Для выяснения причин команда сравнила вирусы, запакованные по одному и затем смешанные, с вирусами, запакованными вместе из одной пула плазмид. С помощью секвенирования длинных ридов они обнаружили, что совместная упаковка даёт высокий уровень «химерных» геномов — вирусных частиц, в которых усилитель и баркод были перепутаны и несоответствовали друг другу. Такие химерные частицы вносят вводящие в заблуждение сигналы баркодов и понижают кажущуюся специфичность. Авторы также изучали систему двойного баркодирования («scQers»), где каждая вирусная частица несла и экспрессии‑связанный баркод, и отдельный конститутивный баркод. Совпадение этих пар позволило отфильтровывать часть ошибочных считываний и улучшить специфичность, но не настолько, чтобы вернуть производительность, наблюдаемую при по‑отдельности валидации.
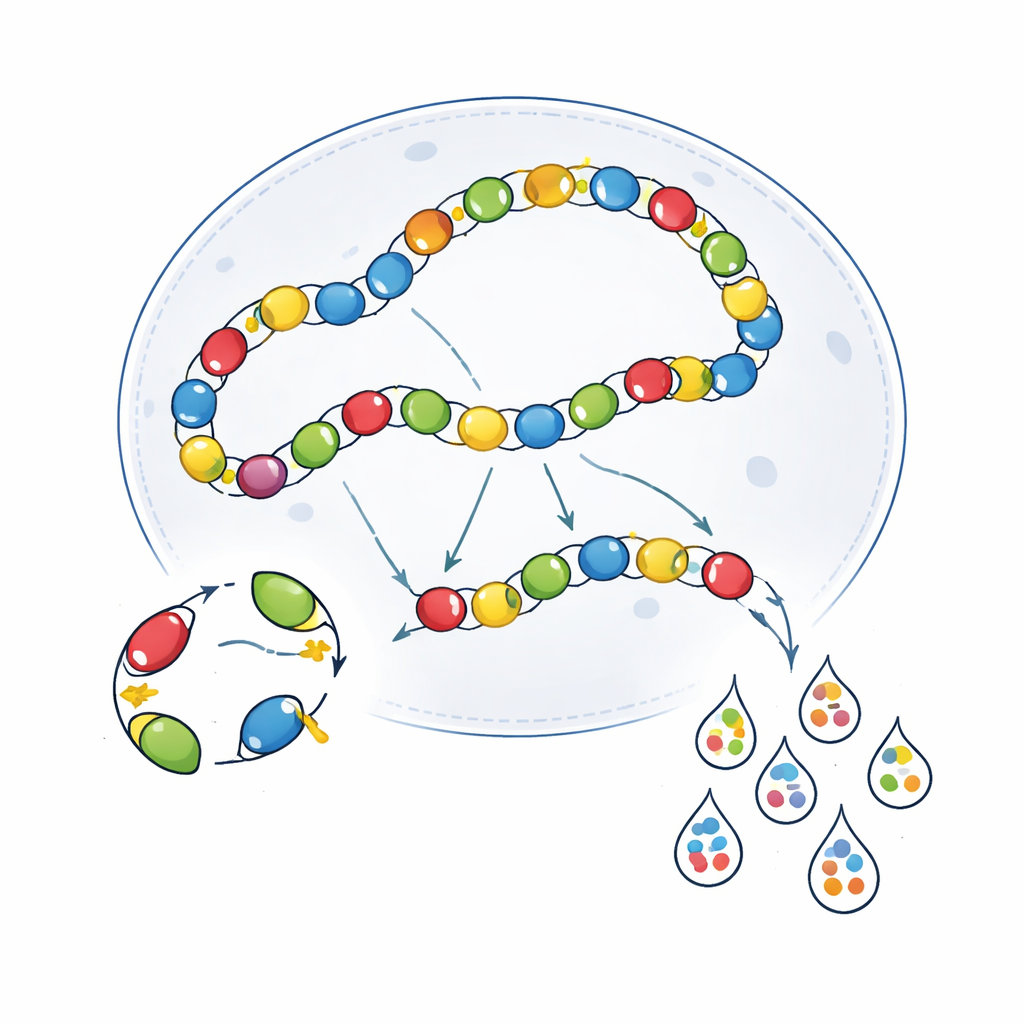
Биологический «перекрёстный разговор» внутри клеток
Технические артефакты — лишь часть проблемы. Сами вирусы во внутри клеток взаимодействуют так, что размывают картину. Оказавшись в ядре, геномы AAV часто соединяются один за другим, образуя длинные цепочки. В такой конфигурации активный усилитель на одном вирусном геноме может случайно приводить к экспрессии с соседнего генома — явление, называемое транскрипционным перекрёстным разговором. Авторы продемонстрировали, что при ко‑инъекции двух разных усилитель‑AAV они могут стимулировать активность друг друга в типах клеток, где один из них по‑одиночке обычно молчит. Использование иммунодефицитных мышей SCID, у которых сокращено конкатенирование AAV, частично уменьшало это перекрытие для некоторых усилителей, но также ослабляло общую экспрессию и не давало последовательного улучшения специфичности во всех случаях. Попытки изолировать вирусные геномы барьерными элементами ДНК также показали лишь контекст‑зависимые преимущества, помогая в некоторых регионах мозга, но не в других.
Почему шум сильнее бьёт по некоторым усилителям
Сравнивая многие усилители одновременно, исследование обнаружило, что те, что нацелены на распространённые типы клеток и дают сильный флуоресцентный сигнал, лучше переносят условия мультиплекса. Слабые усилители или активные в редких популяциях клеток непропорционально теряются на фоне фонового шума от химерных геномов, перекрёстного разговора и случайных баркодов. Важно, что подсчёты транскриптов баркодов в мультиплексных скринингах плохо коррелировали с уровнями белка, измеренными при по‑отдельности тестах, что указывает на то, что большая часть сигналов баркодов в пуловых экспериментах не отражает достоверную усилитель‑зависимую активность.
Что это означает для будущих инструментов для мозга
Для неспециалистов главный вывод таков: объединение многих вирусов с усилителями в одном животном‑испытании сложнее, чем кажется. Вирусы могут перестраиваться во время производства, «переговариваться» друг с другом внутри клеток и создавать вводящие в заблуждение сигналы баркодов, из‑за чего точные усилители выглядят неаккуратными. Авторы делают вывод, что текущие мультиплексные скрининги усилитель‑AAV ещё не могут заменить тщательную по‑отдельности валидацию, особенно при широком поиске новых, тонко нацеленных инструментов. Тем не менее небольшие и продуманно сконструированные пула всё ещё могут быть полезны для ранжирования схожих усилителей или оптимизации дизайна перед окончательной валидацией. Потребуются значительные технические и биологические улучшения, прежде чем крупные, непредвзятые пуловые скрининги смогут надёжно выявлять лучшие генетические «ключи» для нацеливания на конкретные типы клеток мозга.
Цитирование: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
Ключевые слова: усилитель AAV, доставка генов, секвенирование РНК отдельной клетки, вирусное баркодирование, типы клеток мозга