Clear Sky Science · nl
Technische en biologische bronnen van ruis verstoren multiplex AAV-enhancer screening
Het juiste genetische slot vinden
Wetenschappers vertrouwen steeds vaker op virusdeeltjes die genen afleveren om specifieke hersenceltypen in- of uit te schakelen, met zowel basisonderzoek als toekomstige therapieën in het achterhoofd. Om deze instrumenten echter precies te maken, moeten onderzoekers de juiste “aan”-schakelaars toevoegen, zogenaamde enhancers, zodat elk virus alleen in het bedoelde celtype actief wordt. Deze studie laat zien dat wanneer veel van deze met enhancers uitgeruste virussen samen in één experiment worden getest, verborgen technische en biologische ruis de resultaten sterk kunnen vertroebelen, waardoor veelbelovende hulpmiddelen veel minder nauwkeurig lijken dan ze in werkelijkheid zijn.
Waarom celspecifieke genregulatie ertoe doet
Enhancers zijn korte DNA-segmenten die helpen genen in bepaalde celtypen of hersengebieden aan te zetten. Door deze enhancers aan adeno-geassocieerde virussen (AAVs) te koppelen, kunnen onderzoekers fluorescerende merkers of therapeutische genen specifiek afleveren aan bijvoorbeeld een bepaald type neuron of ondersteunende gliacel. Traditioneel wordt elke enhancer–AAV-combinatie één voor één in dieren getest — traag, duur en moeilijk op te schalen. Gemultiplexte benaderingen bieden een kortere route: meng veel verschillend gebarcodeerde enhancer–AAVs, injecteer ze in een muis en gebruik vervolgens single-cell RNA-sequencing om af te lezen welke enhancer in welke cel actief was. In theorie zou dit tientallen enhancer-gedragingen in één experiment aan het licht moeten brengen.
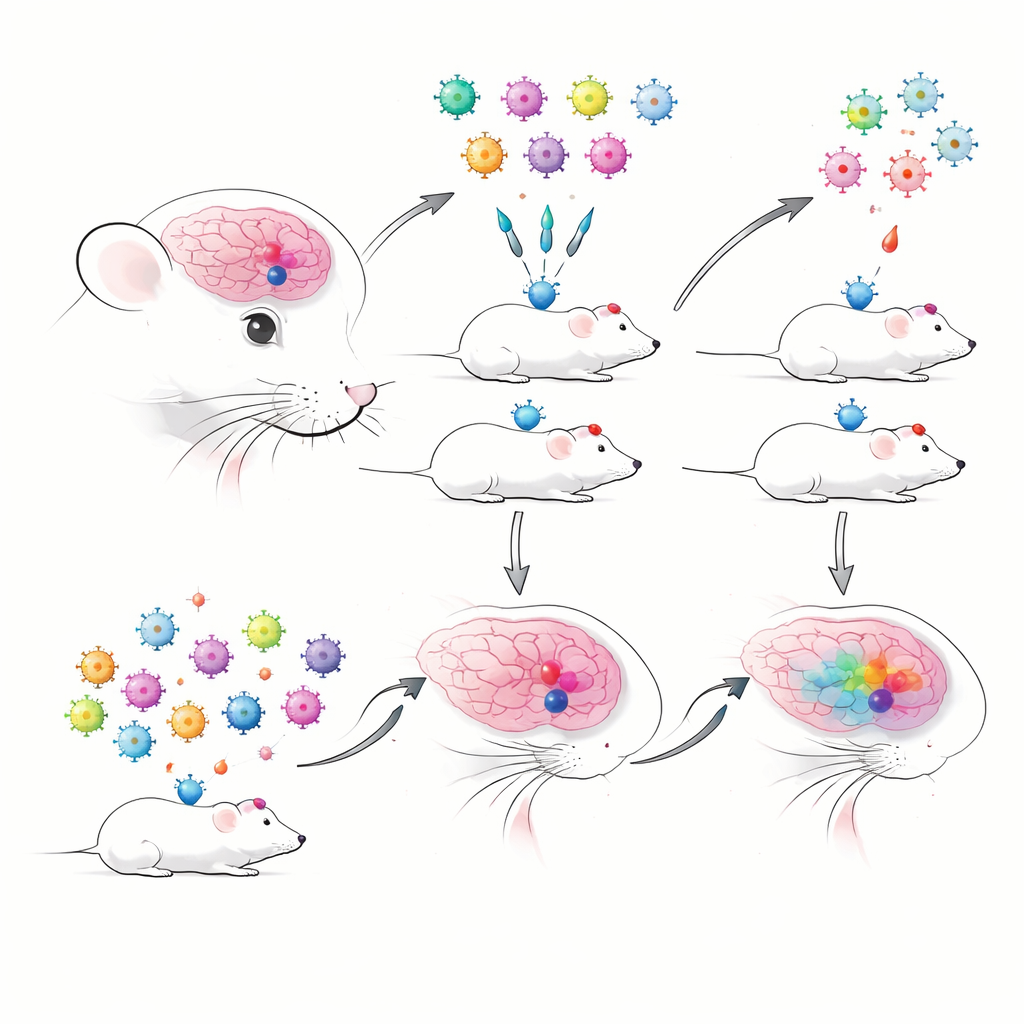
Wanneer veel experimenten één muis delen
De auteurs begonnen met het bouwen van gebarcodeerde AAVs die eerder goed gekarakteriseerde enhancers bevatten, bekend om hun hoge specificiteit voor bepaalde hersenceltypen. Elke enhancer dreef een fluorescerend eiwit en een korte RNA-barcode-tag aan, zodat ze via sequencing gevolgd konden worden. Ze vergeleken traditionele één-voor-één injecties met gepoolde “multiplex” injecties, waarbij veel enhancer–AAVs tegelijk werden afgeleverd en uitgelezen met droplet-gebaseerde single-cell RNA-sequencing. Ze stuitten meteen op een praktisch probleem: bij toeleveringen gebaseerd op geïsoleerde kernen — nuttig voor bevroren of kwetsbaar weefsel — werden de virale barcodes zeer slecht gedetecteerd, terwijl hele cellen de virale transcripties veel betrouwbaarder vastlegden. Dit dwong hen om voor hele cellen te kiezen, die kwetsbaarder kunnen zijn en sommige celtypen mogelijk ondervertegenwoordigen.
Verborgen verwisselingen in virale genomen
Zelfs met betere transcriptopbrengst reproduceerden multiplex-screens niet de heldere, celspecifieke patronen die bij één-voor-één tests werden gezien. Veel enhancers leken veel minder selectief, vooral die natuurlijk zwakker waren of zeldzame celtypen targetten. Om dit te onderzoeken vergeleek het team virussen die afzonderlijk werden verpakt en daarna gemengd, met virussen die samen werden verpakt uit een enkele plasmidepool. Met long-read sequencing ontdekten ze dat gepoolde verpakking een hoge frequentie van “chimerische” genomen produceerde — virale deeltjes waarbij enhancer en barcode waren verstoord en verkeerd gekoppeld. Deze chimerische deeltjes voegen misleidende barcode-signalen toe en verlagen de schijnbare specificiteit. De auteurs onderzochten ook een dubbel-barcoderingssysteem (“scQers”), waarbij elk virus zowel een expressie-gekoppelde barcode als een aparte constitutieve barcode droeg. Het matchen van deze paren maakte het mogelijk enkele foutieve reads eruit te filteren en verbeterde de specificiteit, maar niet genoeg om het prestatieniveau van één-voor-één validatie te herstellen.
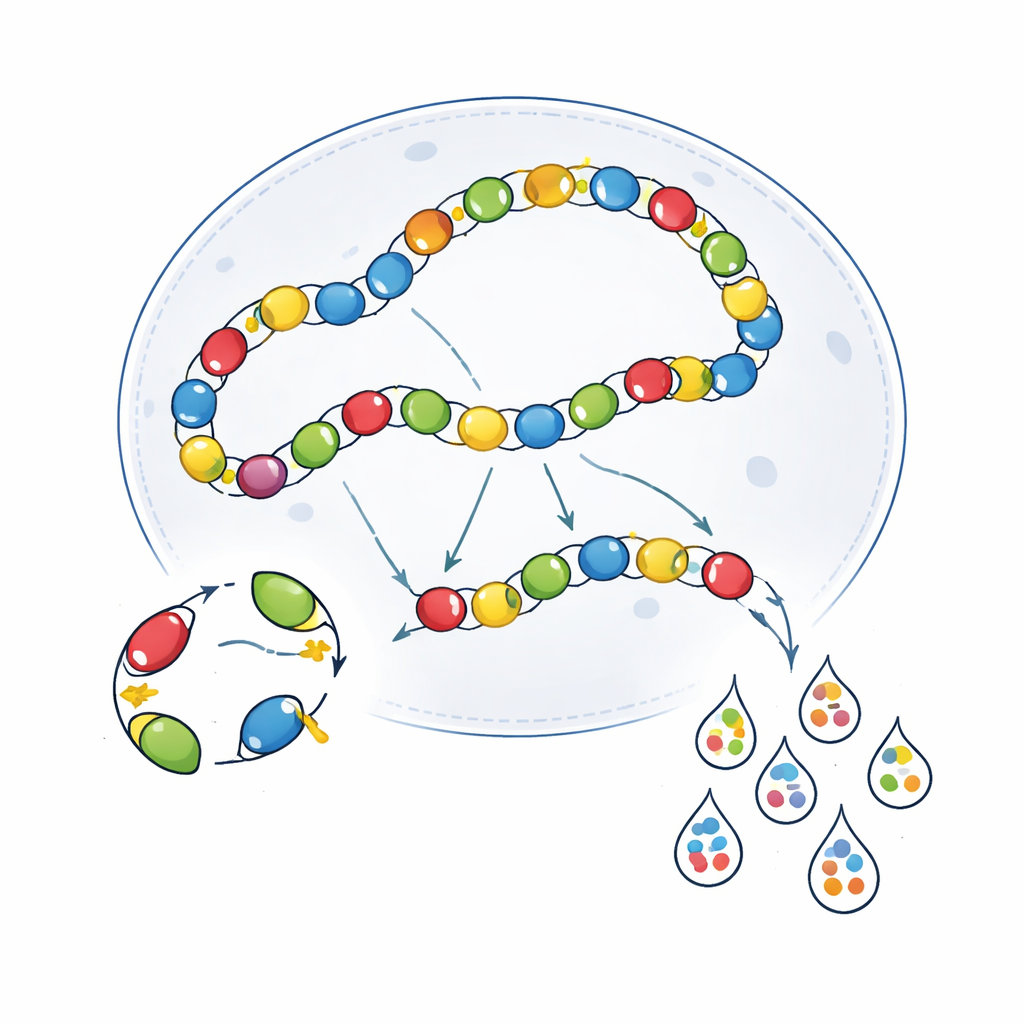
Biologische kruisgesprekken binnen cellen
Technische artefacten waren slechts een deel van het probleem. De virussen zelf interageren binnen cellen op manieren die het beeld vertroebelen. Eenmaal in de kern koppelen AAV-genomen vaak eind-aan-eind en vormen lange ketens. In deze opstelling kan een actieve enhancer op één viraal genoom per ongeluk expressie stimuleren vanaf een aangrenzend genoom — een fenomeen dat transcriptionele crosstalk wordt genoemd. De auteurs toonden aan dat wanneer twee verschillende enhancer–AAVs samen werden geïnjecteerd, ze elkaars activiteit konden aanwakkeren in celtypen waar één alleen normaal gesproken stil zou zijn. Gebruik van immuundeficiënte SCID-muizen, die minder AAV-concatenatie vertonen, verminderde deze overlap gedeeltelijk voor sommige enhancers maar verzwakte ook de algehele expressie en verbeterde de specificiteit niet consistent. Pogingen om virale genomen te isoleren met barrière-DNA-elementen lieten eveneens alleen context-afhankelijke voordelen zien, nuttig in sommige hersengebieden maar niet in andere.
Waarom ruis sommige enhancers harder raakt
Door veel enhancers naast elkaar te vergelijken vond de studie dat diegenen die abundante celtypen targeten en sterke fluorescerende signalen produceren beter presteerden onder gemultiplexte condities. Zwakke enhancers of enhancers actief in zeldzame celpopulaties werden onevenredig overstemd door achtergrondruis van chimerische genomen, crosstalk en losse barcodes. Belangrijk is dat aantallen barcode-transcripts in multiplex-screens niet goed correleerden met de eiwitniveaus gemeten wanneer elke enhancer afzonderlijk werd getest, wat suggereert dat een groot deel van het barcode-signaal in gepoolde experimenten niet trouw de werkelijke enhancer-gedreven activiteit weerspiegelt.
Wat dit betekent voor toekomstige hersengereedschappen
Voor niet-specialisten is de kernboodschap dat het combineren van veel met enhancers uitgeruste virussen in één testdier ingewikkelder is dan het lijkt. De virussen kunnen zich tijdens de productie herschikken, met elkaar ‘praten’ binnen cellen en misleidende barcode-signalen genereren die precieze enhancers slordig doen lijken. De auteurs concluderen dat huidige gemultiplexte enhancer AAV-screens nog niet het zorgvuldige één-voor-één onderzoek kunnen vervangen, vooral niet bij het breed zoeken naar nieuwe, fijn gerichte hulpmiddelen. Kleine en zorgvuldig samengestelde pools kunnen desalniettemin nuttig zijn om vergelijkbare enhancers te rangschikken of ontwerpen te optimaliseren voordat volledige validatie plaatsvindt. Aanzienlijke technische en biologische verbeteringen zijn nodig voordat grote, onbevooroordeelde gepoolde screens betrouwbaar de beste genetische “sleutels” kunnen onthullen om specifieke hersenceltypen te targeten.
Bronvermelding: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
Trefwoorden: enhancer AAV, genafgifte, single-cell RNA sequencing, virale barcodering, hersenceltypen