Clear Sky Science · ar
المصادر التقنية والبيولوجية للضجيج تخلط نتائج فحوصات AAV المعززة متعددة العينات
العثور على المفاتيح الجينية المناسبة
يعتمد العلماء بشكل متزايد على الفيروسات الحاملة للجينات لتشغيل أو إيقاف أنواع خلوية محددة في الدماغ، بغرض البحث الأساسي والمحتمل للعلاجات المستقبلية. ولكي تصبح هذه الأدوات دقيقة، يجب على الباحثين ربط "مفاتيح التشغيل" الصحيحة، المسماة المعززات، بحيث ينشط كل فيروس فقط في نوع الخلية المقصود. تُظهر هذه الدراسة أنه عندما تُختبر العديد من الفيروسات المزودة بالمعززات معًا في تجربة واحدة، يمكن للضجيج التقني والبيولوجي المخفي أن يطمس النتائج بشدة، مما يجعل الأدوات الواعدة تبدو أقل دقة مما هي عليه بالفعل.
لماذا يهم التحكم الجيني النوعي للخلايا
المعززات هي مقاطع قصيرة من الحمض النووي تساعد على تشغيل الجينات في أنواع خلوية أو مناطق دماغية معينة. من خلال ربط هذه المعززات بفيروسات مترافقة مع متعضية (AAV)، يمكن للعلماء توصيل علامات فلورية أو جينات علاجية إلى نوع معين من الخلايا العصبية أو خلايا الدبق الداعمة. تقليديًا، يُختبر كل تركيبة معزز–AAV على حدة في الحيوانات—وهو نهج بطيء ومكلف ويصعب توسيعه. تعد الأساليب متعددة العينات باختصار هذا الطريق: خلط العديد من AAV-المعززات المرمزة بشكل مختلف، حقنها في فأر، ثم استخدام تسلسل RNA أحادي الخلية لقراءة أي معزز كان نشطًا في أي خلية. نظريًا، ينبغي أن يكشف ذلك عن سلوكيات عشرات المعززات في تجربة واحدة.
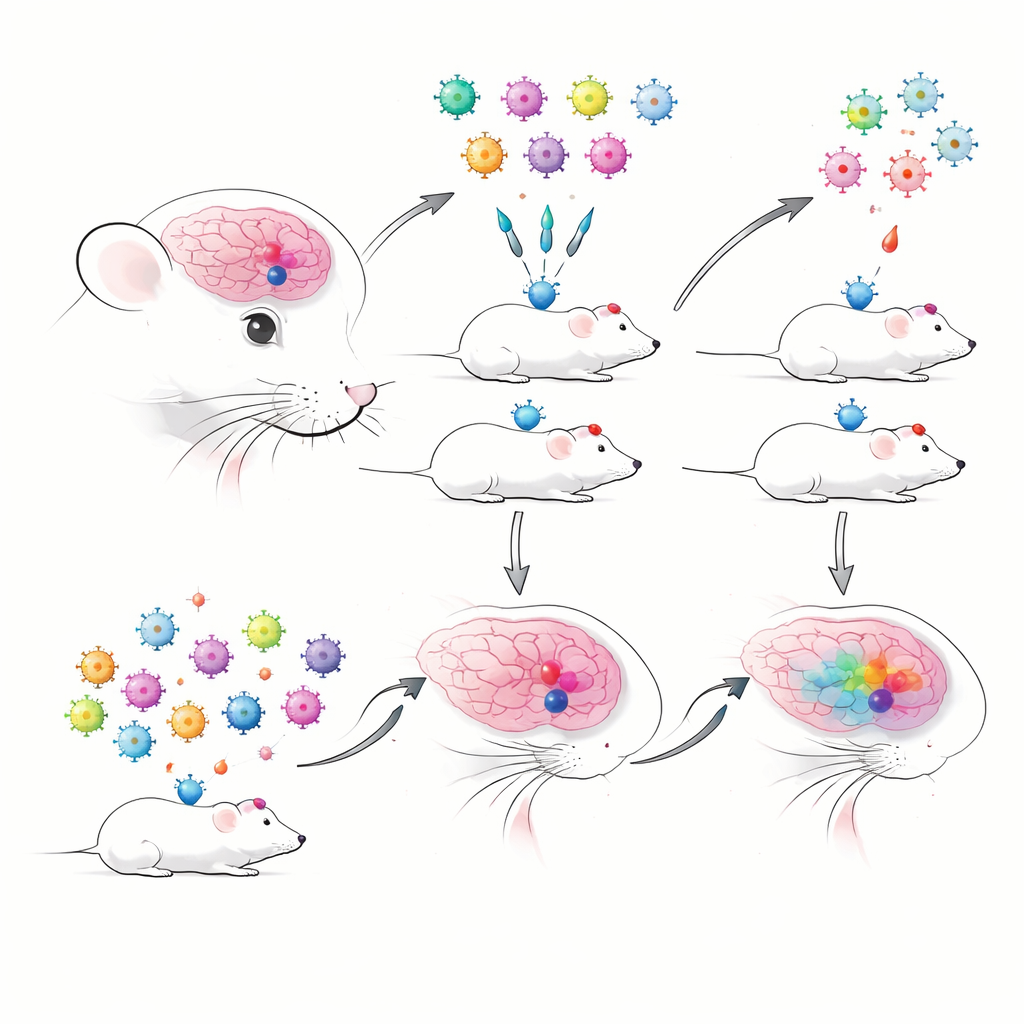
عندما تشارك تجارب كثيرة فأرًا واحدًا
بدأ المؤلفون ببناء AAVs مرمزة حملت معززات سبق توصيفها بدقة وتعرف بوسم أنواع خلايا دماغية محددة بدقة عالية. قاد كل معزز بروتينًا فلوريًا ووسم RNA قصيرًا يمكن تتبعه عن طريق التسلسل. قارنوا الحقن التقليدية واحدًا تلو الآخر مع الحقن المجمعة "المتعددة"، حيث تُسلَّم العديد من AAV-المعززات معًا وتُقرأ باستخدام تسلسل RNA أحادي الخلية القائم على القُطيرات. على الفور واجهوا عقبة عملية: في تجهيزات النوى—المفيدة للأنسجة المجمدة أو الحساسة—كانت وُسُمات الفيروس تُكتشف بشكل ضعيف جدًا، بينما التقطت تحضيرات الخلايا الكاملة نسخ الفيروسات بمعدلات أعلى بكثير. اضطروا لذلك إلى تفضيل الخلايا الكاملة، التي قد تكون أكثر هشاشة وقد لا تمثل بعض أنواع الخلايا بشكل كافٍ.
خلاط خفي في الجينومات الفيروسية
حتى مع تحسين التقاط النسخ، لم تُعيد الشاشات المجمعة الأنماط الواضحة والمتخصصة للخلايا التي شوهدت في اختبارات الواحد تلو الآخر. بدا أن العديد من المعززات أقل انتقائية، خاصة تلك الأضعف طبيعيًا أو التي تستهدف أنواع خلايا نادرة. للتحقق، قارن الفريق الفيروسات التي جرى تعبئتها بشكل فردي ثم خلطها، مقابل الفيروسات التي جرى تعبئتها معًا من تجمع بلازميدات واحد. باستخدام التسلسل طويل القراءة، اكتشفوا أن التعبئة المجمعة أنتجت معدلًا عاليًا من الجينومات "المُدمَجة"—جسيمات فيروسية تُلخبط فيها المعززات والوسوم وتُطابَق بصورة خاطئة. تضيف هذه الجسيمات المدمجة إشارات وسم مضللة وتخفض الدقة الظاهرة. استكشف المؤلفون أيضًا نظام وسم مزدوج ("scQers")، حيث يحمل كل فيروس وسمًا مرتبطًا بالتعبير ووسمًا تأسيسيًا منفصلاً. سمح مطابقة هذين الوسمين بترشيح بعض القراءات الخاطئة وتحسين الانتقائية، لكن ليس بما يكفي لاستعادة أداء التحقق الواحد تلو الآخر.
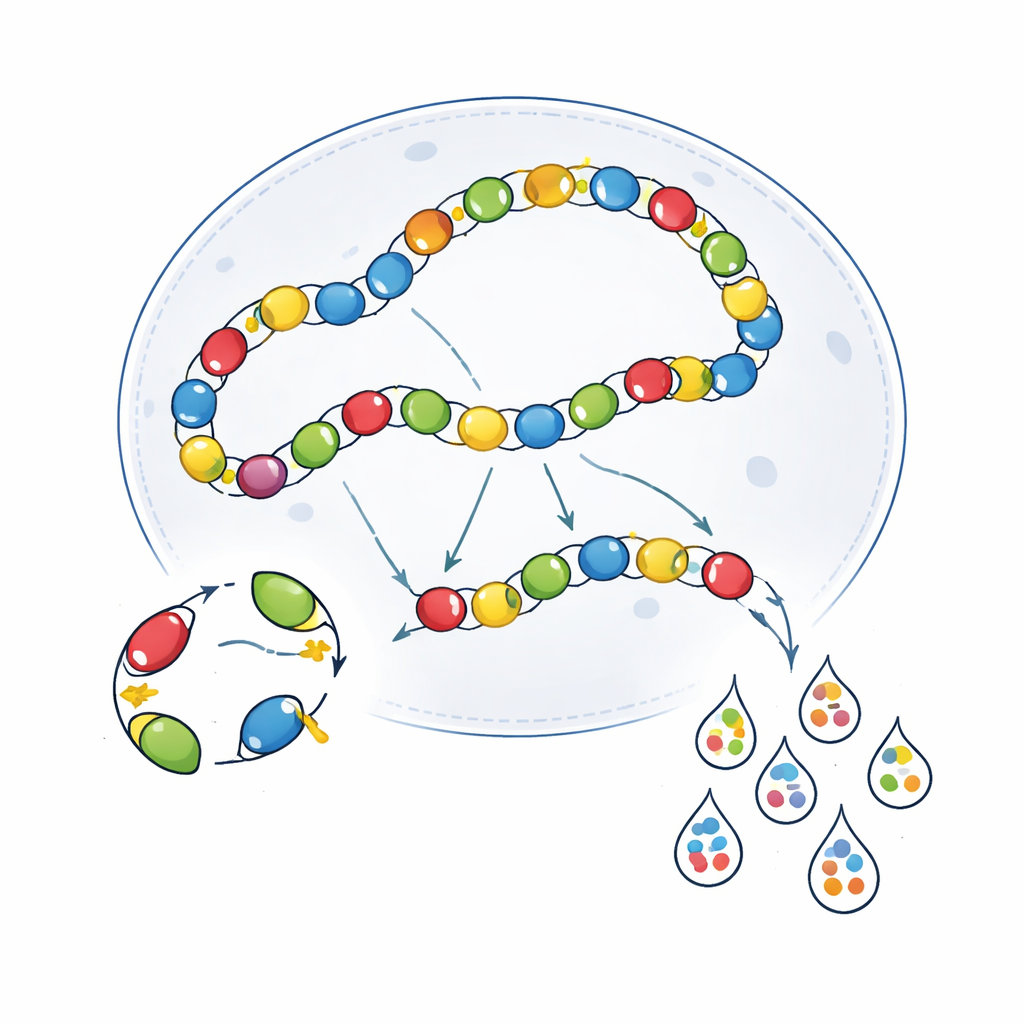
التداخل البيولوجي داخل الخلايا
كانت العيوب التقنية جزءًا من المشكلة فقط. تتفاعل الفيروسات داخل الخلايا بطرق تُطمس الصورة. بمجرد دخولها النواة، غالبًا ما ترتبط جينومات AAV نهاية إلى نهاية، مكونة سلاسل طويلة. في هذا الترتيب، يمكن لمعزز نشط في جينوم فيروسي واحد أن يدفع التعبير من جينوم مجاور عن غير قصد—ظاهرة تسمى التداخل النسخي. أظهر المؤلفون أنه عندما يُحقن فيروسان مختلفان معًا، يمكن أن يُحفِّز كل منهما نشاط الآخر في أنواع خلايا حيث عادة ما يكون أحدهما صامتًا بمفرده. استخدمت التجارب على فئران SCID ناقصة المناعة—والتي تقل فيها ظاهرة ارتباط جينومات AAV—فُقدانًا جزئيًا لهذا التداخل لبعض المعززات، لكن ذلك أضعف أيضًا مستوى التعبير العام، ولم يُحسّن الانتقائية بشكل ثابت عبر اللوحة. كما أظهرت المحاولات لعزل الجينومات الفيروسية بعناصر DNA فاصلة فوائد تعتمد على السياق، مفيدة في بعض مناطق الدماغ لكن ليس في الأخرى.
لماذا يؤثر الضجيج على بعض المعززات أكثر
بمقارنة العديد من المعززات جنبًا إلى جنب، وجدت الدراسة أن تلك التي تستهدف أنواع خلايا وافية وتنتج إشارات فلورية قوية تصمد أفضل في ظروف الفحص المجمعة. غُمرت المعززات الضعيفة أو النشطة في تجمعات خلوية نادرة بشكل غير متناسب بضجيج الخلفية الناتج عن الجينومات المدمجة، والتداخل النسخي، والوسوم المتبقية. ومن المهم أن عدّادات نسخ الوسوم في الشاشات المجمعة لم ترتبط جيدًا بمستويات البروتين المقاسة عندما اُختبرت كل معزز منفردًا، مما يشير إلى أن كثيرًا من إشارة الوسم في التجارب المجمعة لا تعكس بدقة نشاط المعزز الحقيقي.
ماذا يعني هذا لأدوات الدماغ المستقبلية
بالنسبة لغير المتخصصين، الخلاصة أنه جمع العديد من الفيروسات المزودة بالمعززات في حيوان اختبار واحد أكثر تعقيدًا مما يبدو. يمكن للفيروسات أن تعيد ترتيب نفسها أثناء الإنتاج، وتتفاعل فيما بينها داخل الخلايا، وتولد إشارات وسم مضللة تجعل المعززات الدقيقة تبدو مرتخية الدقة. يستنتج المؤلفون أن فحص المعززات المجمعة باستخدام AAV لا يمكنه بعد استبدال التحقق الدقيق واحدًا تلو الآخر، خاصة عند البحث على نطاق واسع عن أدوات جديدة ومستهدفة بدقة. ومع ذلك، قد تظل المجموعات الصغيرة والمصممة بعناية مفيدة لترتيب المعززات المتشابهة أو تحسين التصاميم قبل الالتزام بالتحقق الكامل. ستتطلب الشاشات المجمعة الكبيرة وغير المتحيزة تحسينات تقنية وبيولوجية جوهرية قبل أن تكشف بثقة عن أفضل "المفاتيح" الجينية لاستهداف أنواع خلايا دماغية محددة.
الاستشهاد: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
الكلمات المفتاحية: AAV مع معزز, توصيل الجينات, تسلسل RNA أحادي الخلية, وضع شفرات فيروسية, أنواع خلايا الدماغ