Clear Sky Science · pt
Fontes técnicas e biológicas de ruído confundem triagem multiplexada de potenciadores por AAV
Encontrando as chaves genéticas certas
Cientistas dependem cada vez mais de vírus que entregam genes para ligar ou desligar tipos específicos de células cerebrais, com objetivos tanto para pesquisa básica quanto para terapias futuras. Mas, para tornar essas ferramentas precisas, os pesquisadores devem anexar os “interruptores” corretos, chamados potenciadores, para que cada vírus seja ativado apenas no tipo celular desejado. Este estudo mostra que, quando muitos desses vírus equipados com potenciadores são testados juntos em um único experimento, ruído técnico e biológico oculto pode borrar fortemente os resultados, fazendo ferramentas promissoras parecerem muito menos precisas do que realmente são.
Por que o controle gênico específico por célula importa
Potenciadores são curtos trechos de DNA que ajudam a ativar genes em tipos celulares ou regiões cerebrais específicas. Ao acoplar esses potenciadores a vírus adeno-associados (AAVs), cientistas podem entregar marcadores fluorescentes ou genes terapêuticos especificamente a, por exemplo, um certo tipo de neurônio ou célula glial. Tradicionalmente, cada combinação potenciador–AAV é testada uma a uma em animais—um processo lento, caro e difícil de escalar. Abordagens multiplexadas prometem um atalho: misturar muitos AAVs com códigos de barras diferentes, injetá-los em um camundongo e então usar sequenciamento de RNA de célula única para ler qual potenciador esteve ativo em cada célula. Na teoria, isso deveria revelar dezenas de comportamentos de potenciadores em um único experimento.
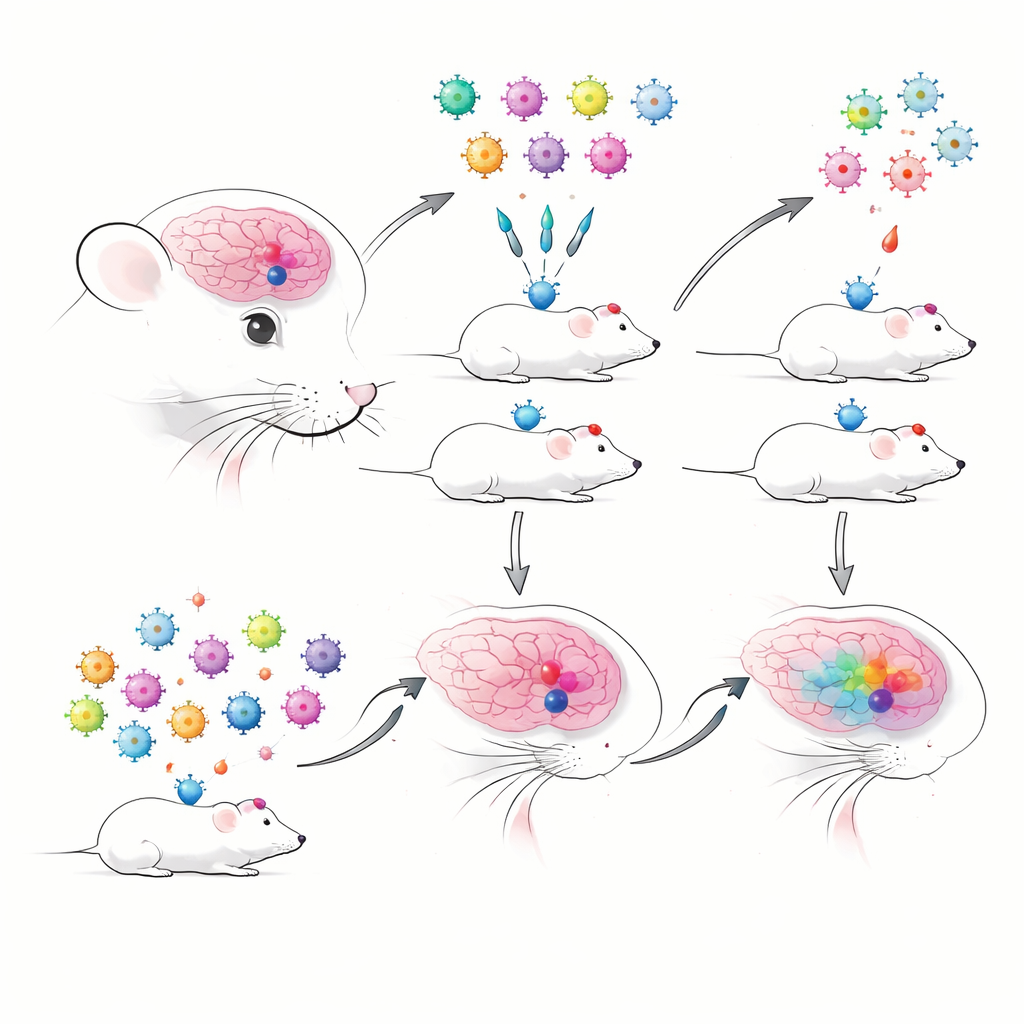
Quando muitos experimentos compartilham um único camundongo
Os autores começaram construindo AAVs codificados com barras que carregavam potenciadores previamente bem caracterizados, conhecidos por marcar tipos celulares cerebrais específicos com alta precisão. Cada potenciador dirigia uma proteína fluorescente e uma curta etiqueta de RNA codificada por barra, permitindo o rastreamento por sequenciamento. Eles compararam injeções tradicionais uma a uma com injeções em pool “multiplexadas”, onde muitos potenciador–AAVs foram administrados simultaneamente e lidos usando sequenciamento de RNA de célula única baseado em gotículas. Imediatamente, eles encontraram um obstáculo prático: em preparações baseadas em núcleos—úteis para tecidos congelados ou frágeis—as barras virais foram detectadas muito mal, enquanto preparações de células inteiras capturaram transcritos virais de forma muito mais confiável. Isso os forçou a favorecer células inteiras, que podem ser mais frágeis e podem subrepresentar alguns tipos celulares.
Confusões ocultas nos genomas virais
Mesmo com melhor captura de transcritos, as triagens multiplexadas não reproduziram os padrões nítidos e específicos por célula observados nos testes um a um. Muitos potenciadores pareceram muito menos seletivos, especialmente aqueles que eram naturalmente mais fracos ou miravam tipos celulares raros. Para investigar, a equipe comparou vírus que foram empacotados individualmente e depois misturados, versus vírus empacotados juntos a partir de um pool único de plasmídeos. Usando sequenciamento de leitura longa, descobriram que o empacotamento em pool produziu uma alta taxa de genomas “quiméricos”—partículas virais nas quais o potenciador e a barra foram embaralhados e desencontrados. Essas partículas quiméricas adicionam sinais de barra enganosos e reduzem a especificidade aparente. Os autores também exploraram um sistema de dupla codificação (“scQers”), onde cada vírus carregava tanto uma barra ligada à expressão quanto uma barra constitutiva separada. A combinação dessas barras permitiu filtrar algumas leituras errôneas e melhorou a especificidade, mas não o suficiente para recuperar o desempenho da validação um a um.
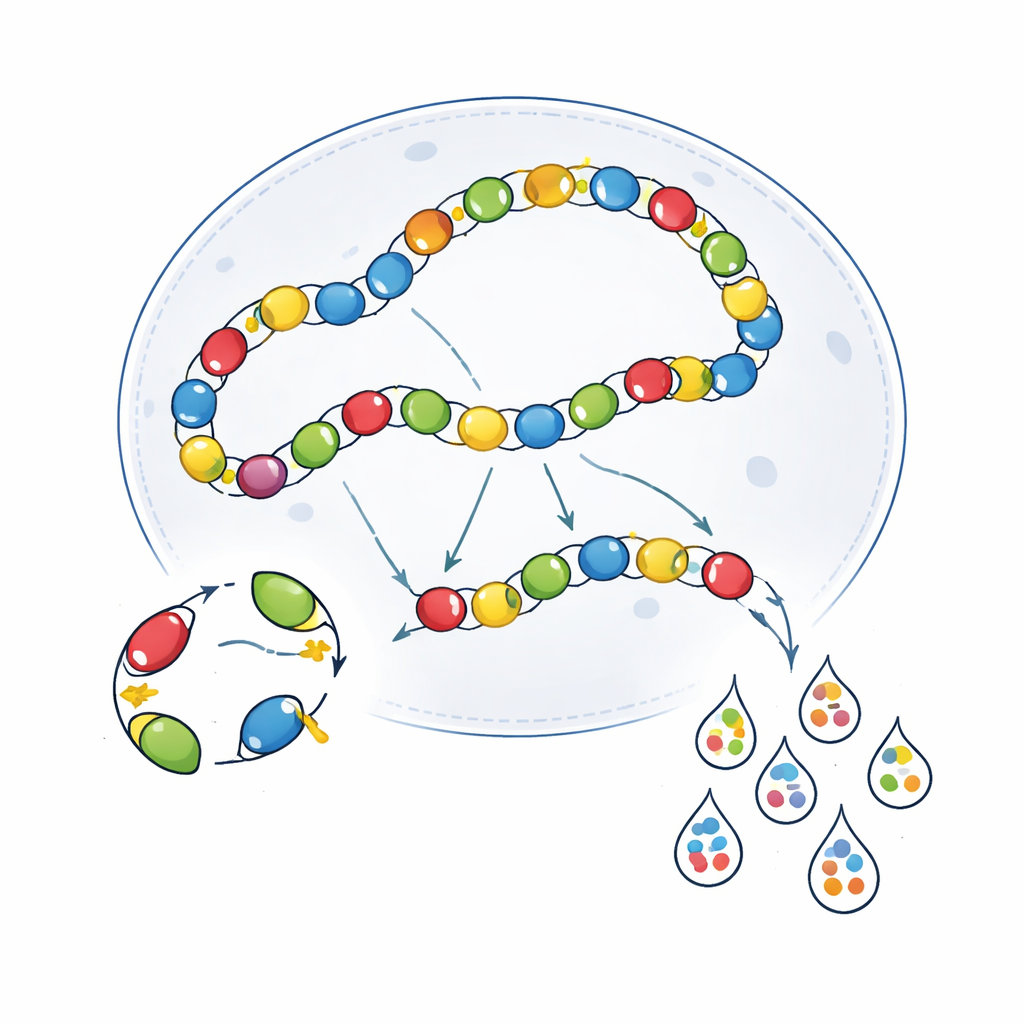
Crosstalk biológico dentro das células
Artefatos técnicos foram apenas parte do problema. Os próprios vírus interagem dentro das células de maneiras que borram o quadro. Uma vez dentro do núcleo, genomas de AAV frequentemente se ligam extremidade a extremidade, formando longas cadeias. Nessa configuração, um potenciador ativo em um genoma viral pode inadvertidamente dirigir a expressão a partir de um genoma vizinho—um fenômeno chamado crosstalk transcripcional. Os autores demonstraram que, quando dois potenciador–AAVs diferentes foram coinjetados, eles podiam estimular a atividade um do outro em tipos celulares onde um sozinho normalmente estaria silencioso. Usar camundongos SCID imunodeficientes, que apresentam concatenação de AAV reduzida, diminuiu parcialmente essa sobreposição para alguns potenciadores, mas também enfraqueceu a expressão geral e não melhorou de forma consistente a especificidade em todo o conjunto. Tentativas de isolar genomas virais com elementos de DNA barreira também mostraram benefícios dependentes do contexto, ajudando em algumas regiões cerebrais, mas não em outras.
Por que o ruído afeta alguns potenciadores mais severamente
Ao comparar muitos potenciadores lado a lado, o estudo constatou que aqueles que miram tipos celulares abundantes e produzem sinais fluorescentes fortes se saíram melhor em condições multiplexadas. Potenciadores fracos ou ativos em populações celulares raras foram desproporcionalmente abafados pelo ruído de fundo de genomas quiméricos, crosstalk e barras errantes. Importante, a contagem de transcritos de barras em triagens multiplexadas não correlacionou bem com os níveis de proteína medidos quando cada potenciador foi testado isoladamente, sugerindo que grande parte do sinal de barra em experimentos em pool não reflete fielmente a atividade dirigida pelo potenciador.
O que isso significa para ferramentas cerebrais do futuro
Para não especialistas, a conclusão é que combinar muitos vírus equipados com potenciadores em um único animal de teste é mais complicado do que aparenta. Os vírus podem se rearranjar durante a produção, interagir entre si dentro das células e gerar sinais de barra enganosos que fazem potenciadores precisos parecerem imprecisos. Os autores concluem que a triagem multiplexada atual de potenciadores por AAV ainda não pode substituir a validação cuidadosa um a um, especialmente ao buscar amplamente novas ferramentas finamente direcionadas. No entanto, pools pequenos e cuidadosamente projetados ainda podem ser úteis para ranquear potenciadores semelhantes ou otimizar designs antes de se comprometer com validação completa. Melhorias técnicas e biológicas substanciais serão necessárias antes que grandes triagens em pool, sem viés, possam revelar de forma confiável as melhores “chaves” genéticas para direcionar tipos celulares cerebrais específicos.
Citação: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
Palavras-chave: enhancer AAV, entrega de genes, sequenciamento de RNA de célula única, codificação viral, tipos de células cerebrais