Clear Sky Science · ja
多重化されたエンハンサーAAVスクリーニングをかき乱す技術的および生物学的ノイズ源
適切な遺伝的鍵を見つける
研究者は特定の脳細胞型をオンまたはオフにするために、遺伝子を運ぶウイルスにますます依存しています。基礎研究や将来の治療を見据えた動きです。しかし、これらのツールを正確にするには、各ウイルスが意図した細胞型だけで作動するように正しい「オン・スイッチ」であるエンハンサーを付ける必要があります。本研究は、多数のエンハンサー装備ウイルスを単一実験で同時に評価すると、潜在的な技術的および生物学的ノイズが結果を大きくぼかし、有望なツールが実際よりもはるかに不正確に見えてしまうことを示します。
細胞特異的遺伝子制御が重要な理由
エンハンサーは、特定の細胞型や脳領域で遺伝子をオンにするのを助ける短いDNA配列です。これらのエンハンサーをアデノ随伴ウイルス(AAV)に結びつけることで、研究者は蛍光マーカーや治療遺伝子を、例えば特定のニューロンや支持性グリア細胞に特異的に届けることができます。従来は各エンハンサー–AAVの組み合わせを動物で個別に評価しており、遅く高価でスケールしにくいという問題がありました。多重化アプローチは近道を約束します:異なるバーコードを持つ多くのエンハンサー–AAVを混合してマウスに注入し、単一細胞RNAシーケンスでどのエンハンサーがどの細胞で活動したかを読み出す。理論上は、単一実験で多数のエンハンサー挙動を明らかにできるはずです。
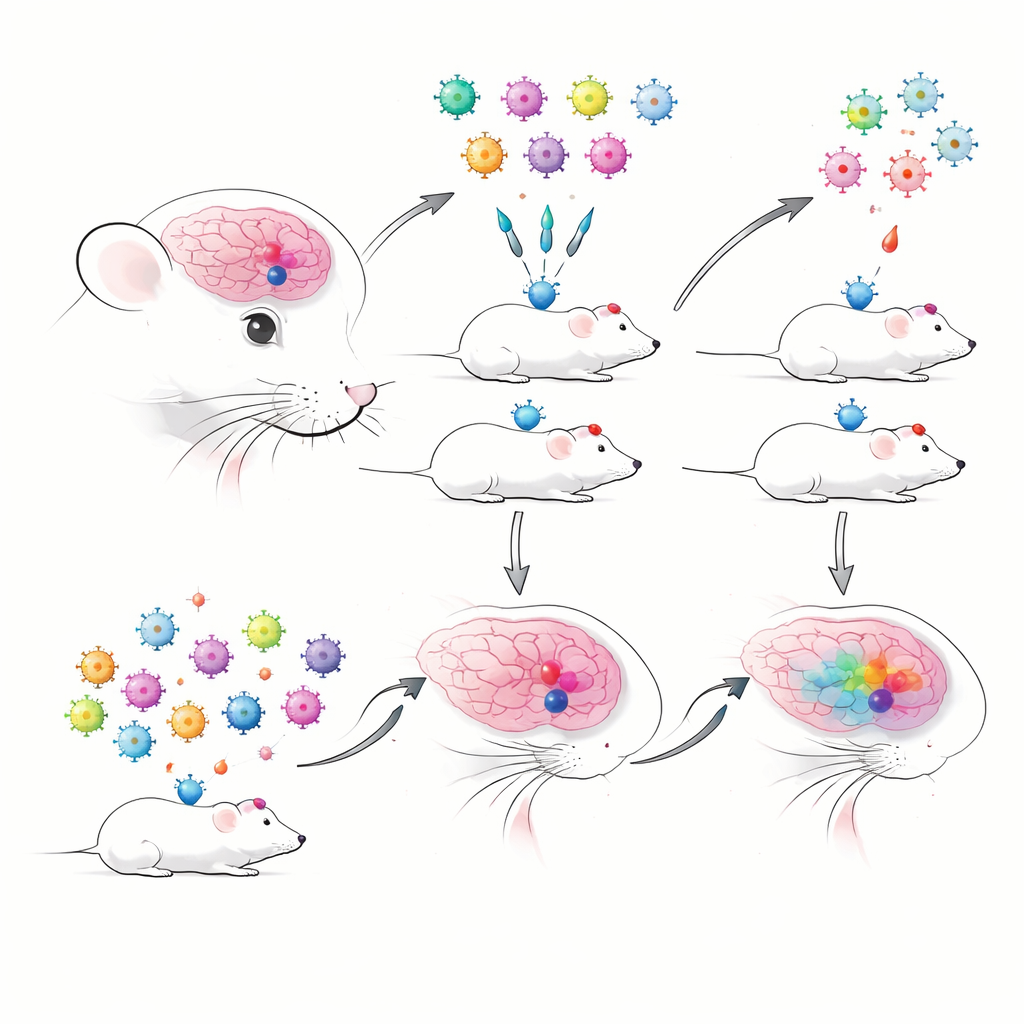
多くの実験が一匹のマウスを共有するとき
著者らはまず、特定の脳細胞型を高い精度で標識することが以前に特徴づけられたエンハンサーを搭載したバーコード付きAAVを構築しました。各エンハンサーは蛍光タンパク質と短いRNAバーコードタグを駆動し、シーケンスで追跡できるようにしました。従来の個別注入と、多数のエンハンサー–AAVを同時に投与してドロップレット型単一細胞RNAシーケンスで読み出すプール化(多重)注入を比較しました。すぐに実務的な障害に直面しました:凍結組織やデリケートな組織に有用な核ベースの調製ではウイルスバーコードが非常に検出されにくく、一方で全細胞調製はウイルストランスクリプトをはるかに確実に捕捉しました。これにより、よりもろく一部の細胞型を過小評価する可能性のある全細胞法を選ばざるを得なくなりました。
ウイルスゲノムの隠れた混入
トランスクリプト捕捉が改善されても、多重化スクリーニングは個別試験で観察される明瞭な細胞特異的パターンを再現しませんでした。多くのエンハンサーは特に、もともと弱いものや稀な細胞型を標的とするものは選択性がはるかに低く見えました。調査のために、個別にパッケージされたウイルスを混合した場合と、単一のプラスミドプールから一緒にパッケージした場合を比較しました。ロングリードシーケンシングを用いると、プール化パッケージングではエンハンサーとバーコードが錯綜し不一致になる「キメラ」ゲノムの高い割合が生じていることが明らかになりました。これらのキメラ粒子は誤ったバーコード信号を追加し、見かけ上の特異性を低下させます。著者らはまた二重バーコーディングシステム(“scQers”)を検討し、各ウイルスが発現連結バーコードと別個の構成的バーコードの両方を持つ方式で、これらのペアを照合することで一部の誤ったリードをフィルタリングして特異性を改善できましたが、個別検証の性能を回復するには十分ではありませんでした。
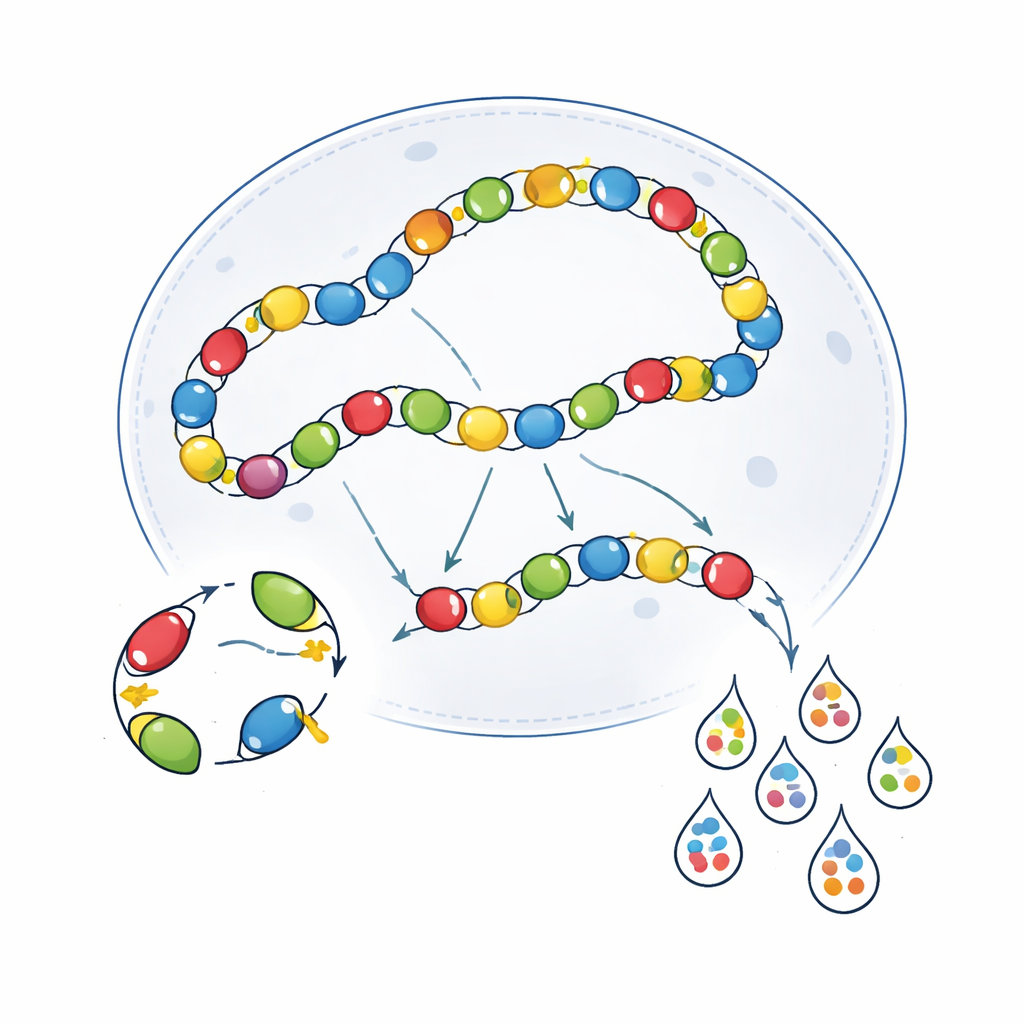
細胞内での生物学的なクロストーク
技術的アーティファクトは問題の一部にすぎませんでした。ウイルス自体が細胞内で相互作用し、図をぼかすことがあります。核内に入ると、AAVゲノムはしばしば端と端が連結して長い鎖を形成します。この配置では、一つのウイルスゲノム上の活性化されたエンハンサーが隣接するゲノムからの発現を意図せず駆動することがあり、これを転写クロストークと呼びます。著者らは、二つの異なるエンハンサー–AAVを共注入した場合、単独では通常沈黙するはずの細胞型で互いの活性を促進し得ることを示しました。AAVの連結が減る免疫不全SCIDマウスを用いると、一部のエンハンサーではこの重なりが部分的に低減しましたが、同時に全体の発現が弱まり、全体として一貫して特異性を改善するには至りませんでした。バリアDNA要素でウイルスゲノムを絶縁しようとする試みも、脳の一部の領域では効果があったものの、他では利点が限定的であり文脈依存であることが示されました。
なぜノイズが一部のエンハンサーをより強く襲うのか
多くのエンハンサーを並べて比較することで、豊富に存在する細胞型を標的とし強い蛍光信号を出すエンハンサーは、多重化条件下でよりうまく振る舞うことが分かりました。弱いエンハンサーや稀な細胞集団で活性を示すものは、キメラゲノム、クロストーク、迷い込んだバーコードからのバックグラウンドノイズに不釣り合いに飲み込まれました。重要なのは、プール化スクリーニングでカウントされたバーコード転写物の数は、各エンハンサーを単独で試験したときに測定されたタンパク質量とよく相関しなかったことで、プール実験で得られるバーコード信号の多くは真のエンハンサー駆動活性を忠実に反映していないことを示唆します。
将来の脳向けツールにとっての意味
専門外の方への結論は、多数のエンハンサー装備ウイルスを単一の被験動物に組み合わせることは見た目よりも複雑だということです。ウイルスは産生過程で再配列し、細胞内で互いに影響し合い、正確なエンハンサーを粗雑に見せる誤ったバーコード信号を生み出します。著者らは、現時点の多重化エンハンサーAAVスクリーニングは、特に幅広く新規で精密に標的化されたツールを探索する場合、慎重な個別検証に代わるものにはまだなり得ないと結論づけています。ただし、慎重に設計された小規模プールは、類似したエンハンサーの順位付けや、完全な検証に入る前の設計最適化には依然有用である可能性があります。大規模で偏りのないプール化スクリーニングが特定の脳細胞型を標的とする最良の遺伝的「鍵」を信頼できる形で明らかにするためには、実質的な技術的および生物学的改善が必要です。
引用: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
キーワード: エンハンサー AAV, 遺伝子導入, 単一細胞RNAシーケンシング, ウイルスバーコーディング, 脳の細胞型