Clear Sky Science · it
Sorgenti tecniche e biologiche di rumore confondono gli screening multiplexati di potenziatori con AAV
Trovare le giuste chiavi genetiche
Gli scienziati si affidano sempre più a virus che trasferiscono geni per attivare o disattivare tipi cellulari cerebrali specifici, con ricadute sia sulla ricerca fondamentale sia su possibili terapie future. Per rendere questi strumenti precisi, però, i ricercatori devono collegare gli “interruttori” corretti, detti potenziatori (enhancer), in modo che ogni virus si attivi solo nel tipo cellulare desiderato. Questo studio mostra che quando molti di questi virus dotati di potenziatori vengono testati insieme in un unico esperimento, rumori tecnici e biologici nascosti possono offuscare fortemente i risultati, facendo apparire strumenti promettenti molto meno accurati di quanto siano realmente.
Perché il controllo genico specifico per cellula è importante
I potenziatori sono brevi tratti di DNA che aiutano ad accendere geni in tipi cellulari o regioni cerebrali particolari. Accoppiando questi potenziatori ad adeno-associated virus (AAV), gli scienziati possono consegnare marcatori fluorescenti o geni terapeutici specificamente a, per esempio, un certo tipo di neurone o a cellule gliali di supporto. Tradizionalmente, ogni combinazione potenziatore–AAV viene testata una per volta negli animali: un processo lento, costoso e difficile da scalare. Gli approcci multiplexati promettono una scorciatoia: mescolare molti AAV con codici a barre diversi, iniettarli in un topo e poi usare il sequenziamento RNA a singola cellula per leggere quale potenziatore è stato attivo in quale cellula. In teoria, questo dovrebbe rivelare il comportamento di decine di potenziatori in un singolo esperimento.
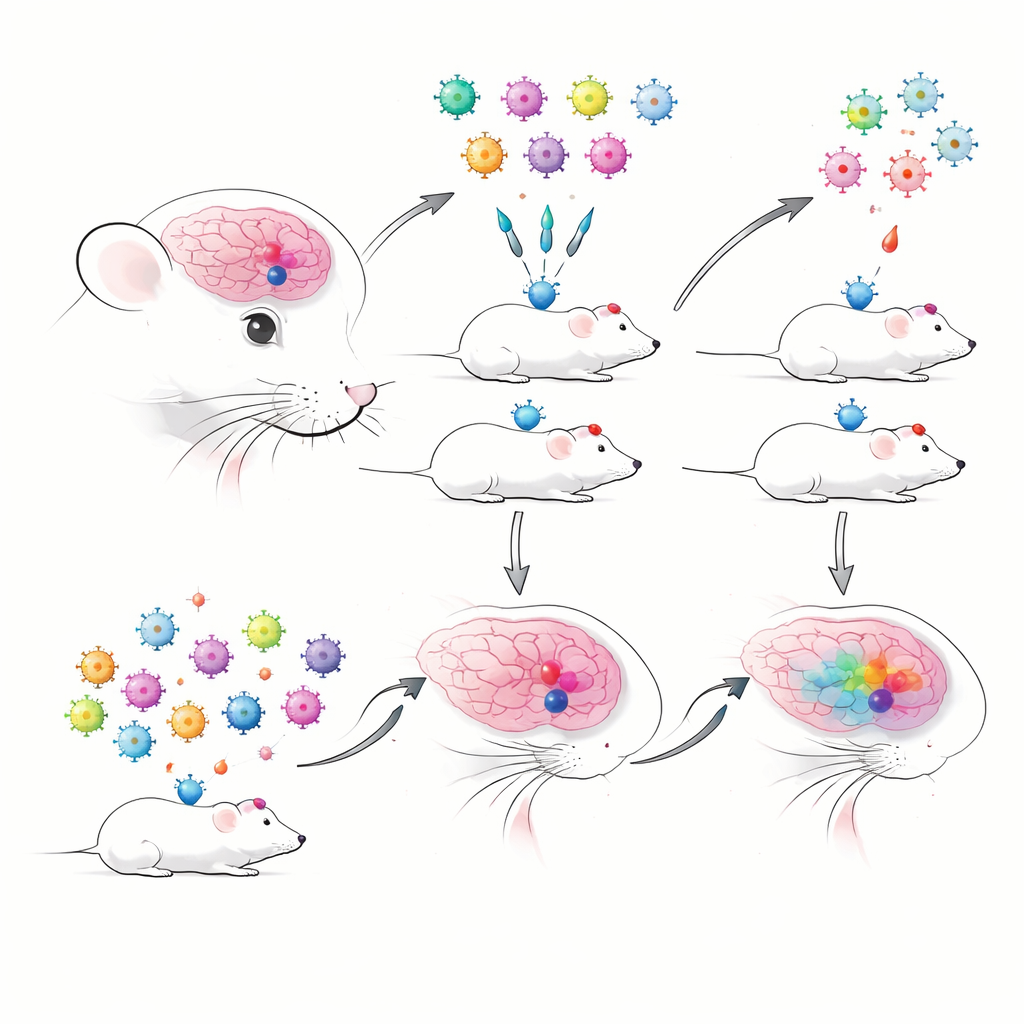
Quando molti esperimenti condividono un solo topo
Gli autori hanno iniziato costruendo AAV codificati con barcode contenenti potenziatori precedentemente ben caratterizzati, noti per etichettare tipi cellulari cerebrali specifici con alta accuratezza. Ogni potenziatore esprimeva una proteina fluorescente e un breve tag di RNA barcode, permettendo il tracciamento tramite sequenziamento. Hanno confrontato le iniezioni tradizionali una per volta con le iniezioni “multiplex” in cui molti enhancer-AAV venivano somministrati insieme e letti tramite sequenziamento RNA a singola cellula basato su droplet. Subito hanno incontrato un ostacolo pratico: nelle preparazioni basate sui nuclei — utili per tessuti congelati o delicati — i barcode virali venivano rilevati molto male, mentre le preparazioni di cellule intere catturavano i trascritti virali in modo molto più affidabile. Questo li ha costretti a preferire cellule intere, che però possono essere più fragili e rischiare di sottorappresentare alcuni tipi cellulari.
Scambi nascosti nei genomi virali
Anche con una migliore cattura dei trascritti, gli screening multiplexati non riproducevano i pattern netti e specifici per cellula osservati nei test uno per uno. Molti potenziatori apparivano molto meno selettivi, specialmente quelli naturalmente più deboli o diretti a tipi cellulari rari. Per indagare, il gruppo ha confrontato virus confezionati singolarmente e poi miscelati, rispetto a virus confezionati insieme a partire da un pool di plasmidi. Mediante sequenziamento a lettura lunga, hanno scoperto che il confezionamento in pool produceva un alto tasso di genomi “chimerici” — particelle virali in cui potenziatore e barcode erano stati mescolati e abbinati in modo errato. Queste particelle chimeriche introducono segnali di barcode fuorvianti e riducono la specificità apparente. Gli autori hanno anche esplorato un sistema a doppio barcode (“scQers”), in cui ogni virus portava sia un barcode legato all’espressione sia un barcode costituzionale separato. Il confronto di queste coppie ha permesso di filtrare alcune letture erronee e ha migliorato la specificità, ma non quanto necessario per recuperare le prestazioni della validazione uno per uno.
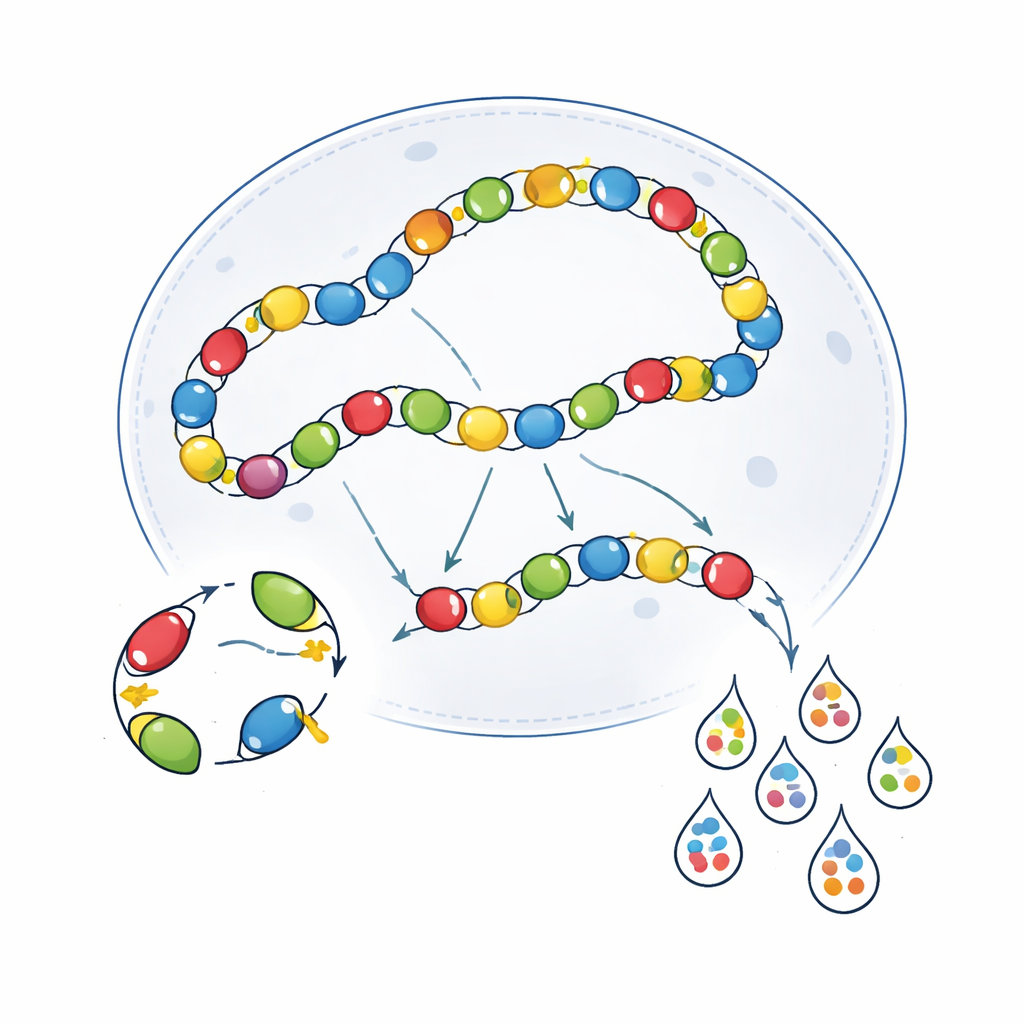
Crosstalk biologico all’interno delle cellule
Gli artefatti tecnici erano solo parte del problema. Anche i virus interagiscono all’interno delle cellule in modi che sfumano i risultati. Una volta nel nucleo, i genomi AAV spesso si concatenano estremità a estremità, formando lunghe catene. In questa disposizione, un potenziatore attivo su un genoma virale può involontariamente promuovere l’espressione da un genoma vicino — un fenomeno chiamato crosstalk trascrizionale. Gli autori hanno dimostrato che quando due diversi enhancer-AAV venivano co-iniettati, potevano stimolare reciprocamente l’attività in tipi cellulari in cui uno da solo sarebbe stato normalmente silente. L’uso di topi immunodeficienti SCID, che mostrano concatenazione AAV ridotta, ha parzialmente ridotto questa sovrapposizione per alcuni potenziatori ma ha anche indebolito l’espressione complessiva, e non ha migliorato in modo coerente la specificità in tutti i casi. I tentativi di isolare i genomi virali con elementi di DNA barriera hanno mostrato benefici dipendenti dal contesto, utili in alcune regioni cerebrali ma non in altre.
Perché il rumore penalizza alcuni potenziatori più di altri
Confrontando molti potenziatori fianco a fianco, lo studio ha rilevato che quelli diretti a tipi cellulari abbondanti e che producevano segnali fluorescenti forti resistevano meglio alle condizioni multiplexate. I potenziatori deboli o attivi in popolazioni cellulari rare venivano in misura sproporzionata sovrastati dal rumore di fondo proveniente da genomi chimerici, crosstalk e barcode spurie. È importante notare che i conteggi dei trascritti barcode negli screening multiplexati non correlavano bene con i livelli proteici misurati quando ogni potenziatore veniva testato da solo, suggerendo che gran parte del segnale di barcode negli esperimenti in pool non riflette fedelmente l’attività realmente guidata dal potenziatore.
Cosa significa per i futuri strumenti cerebrali
Per i non specialisti, la conclusione è che combinare molti virus dotati di potenziatori in un singolo animale di test è più complicato di quanto sembri. I virus possono riarrangiarsi durante la produzione, interagire tra loro all’interno delle cellule e generare segnali di barcode fuorvianti che fanno apparire potenziatori precisi come imprecisi. Gli autori concludono che gli screening multiplexati attuali per potenziatori con AAV non possono ancora sostituire la convalida accurata uno per uno, specialmente quando si cerca in modo ampio nuovi strumenti finemente mirati. Tuttavia, pool piccoli e progettati con cura possono ancora essere utili per classificare potenziatori simili o ottimizzare i progetti prima di impegnarsi in una validazione completa. Sono necessari miglioramenti tecnici e biologici sostanziali prima che grandi screening in pool non pilotati possano rivelare in modo affidabile le migliori “chiavi” genetiche per mirare a tipi cellulari cerebrali specifici.
Citazione: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
Parole chiave: AAV potenziatore, consegna di geni, sequenziamento RNA a singola cellula, barcoding virale, tipi di cellule cerebrali