Clear Sky Science · sv
Tekniska och biologiska källor till brus försvårar multiplexad screening av enhancers med AAV
Hitta rätt genetiska nycklar
Forskare förlitar sig alltmer på genlevererande virus för att slå av eller på specifika hjärncellstyper, med förhoppningar både för grundforskning och framtida terapier. För att göra dessa verktyg precisa måste man fästa rätt ”på/av‑brytare”, så kallade enhancers, så att varje virus aktiveras bara i den avsedda celltypen. Denna studie visar att när många enhancer‑utrustade virus testas tillsammans i ett enda experiment kan doldt tekniskt och biologiskt brus kraftigt sudda ut resultaten, vilket får lovande verktyg att framstå som mycket mindre specifika än de egentligen är.
Varför cellspecifik genkontroll är viktig
Enhancers är korta DNA‑sekvenser som hjälper till att slå på gener i särskilda celltyper eller hjärnregioner. Genom att koppla dessa enhancers till adeno‑associated virus (AAV) kan forskare leverera fluorescerande markörer eller terapeutiska gener specifikt till exempelvis en viss typ av neuron eller stödjande gliacell. Traditionellt testas varje enhancer‑AAV‑kombination en i taget i djur—långsamt, dyrt och svårt att skala upp. Multiplexade metoder lovar en genväg: blanda många olika streckkodade enhancer‑AAVs, injicera dem i en mus och använd sedan single‑cell RNA‑sekvensering för att läsa av vilken enhancer som varit aktiv i vilken cell. I teorin borde detta kunna avslöja flera dussin enhancers beteenden i ett enda experiment.
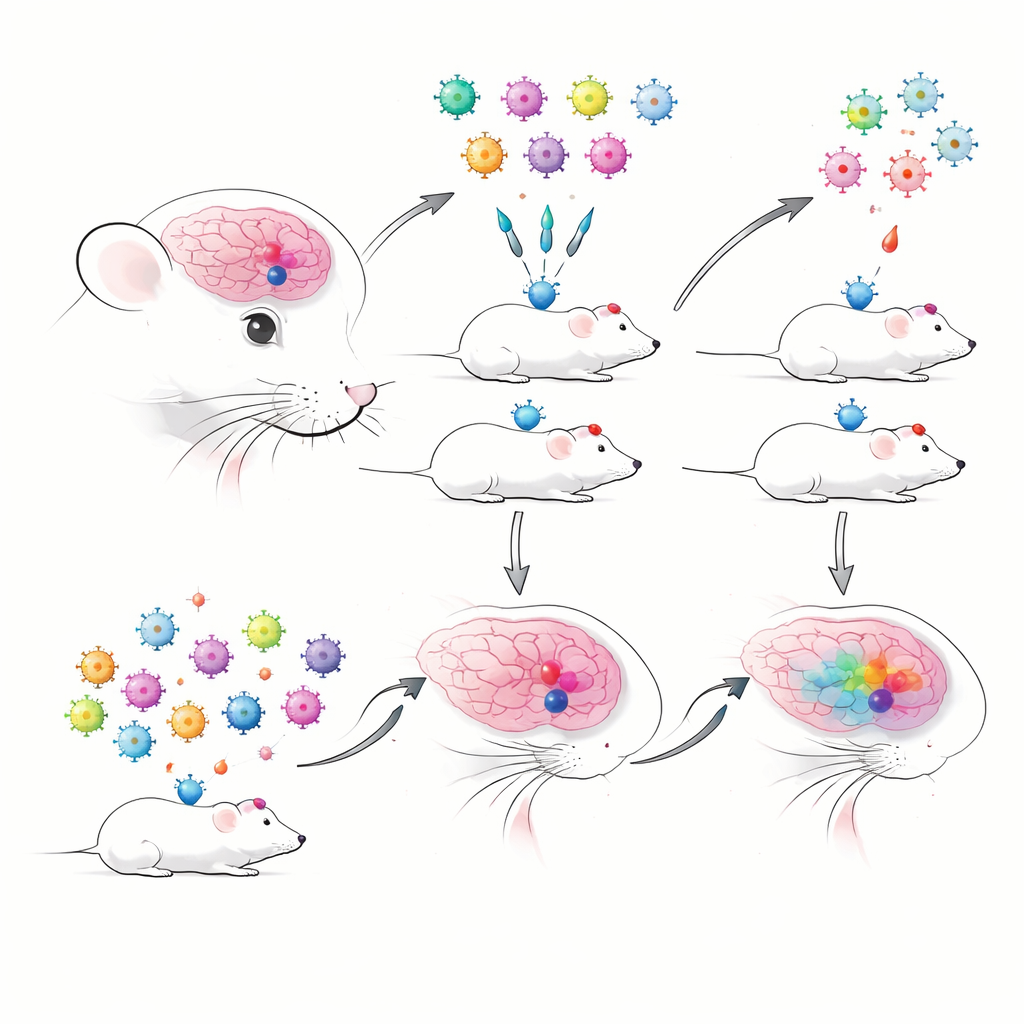
När många experiment delar en mus
Författarna började med att konstruera streckkodade AAVs som bar tidigare välkarakteriserade enhancers som är kända för att märka specifika hjärncellstyper med hög noggrannhet. Varje enhancer styrde ett fluorescerande protein och en kort RNA‑streckkod, vilket möjliggjorde spårning med sekvensering. De jämförde traditionella en‑och‑en‑injektioner med poolade ”multiplex”‑injektioner, där många enhancer‑AAVs levererades samtidigt och avläsning gjordes med droppbaserad single‑cell RNA‑sekvensering. Redan här stötte de på ett praktiskt problem: i nukleusbansierade preparat—användbara för frusna eller känsliga vävnader—detekterades de virala streckkoderna mycket dåligt, medan hela cellpreparat fångade virala transkript mycket mer pålitligt. Detta tvingade dem att föredra hela celler, som kan vara mer sköra och därmed underrepresentera vissa celltyper.
Dolda sammanblandningar i viral genom
Även med bättre transkriptfångst återgav inte multiplexade skärmar de skarpa, cellspecifika mönstren som sågs vid en‑och‑en‑tester. Många enhancers framstod som betydligt mindre selektiva, särskilt de som naturligt var svagare eller riktade sällsynta celltyper. För att undersöka detta jämförde teamet virus som paketerats individuellt och sedan blandats, med virus som paketerats tillsammans från en enda plasmidpool. Med lång avläsningssekvensering upptäckte de att poolad paketering gav en hög frekvens av ”kimeriska” genom—viruspartiklar där enhancer och streckkod hade blivit omkastade och felparade. Dessa kimeriska partiklar lägger till vilseledande streckkodssignaler och sänker den uppenbara specificiteten. Författarna utforskade också ett dubbelstreckkodssystem (”scQers”), där varje virus bar både en uttrycksrelaterad streckkod och en separat konstitutiv streckkod. Genom att matcha dessa par kunde vissa felaktiga läsningar filtreras bort och specificiteten förbättrades, men inte tillräckligt för att återställa prestandan hos en‑och‑en‑validering.
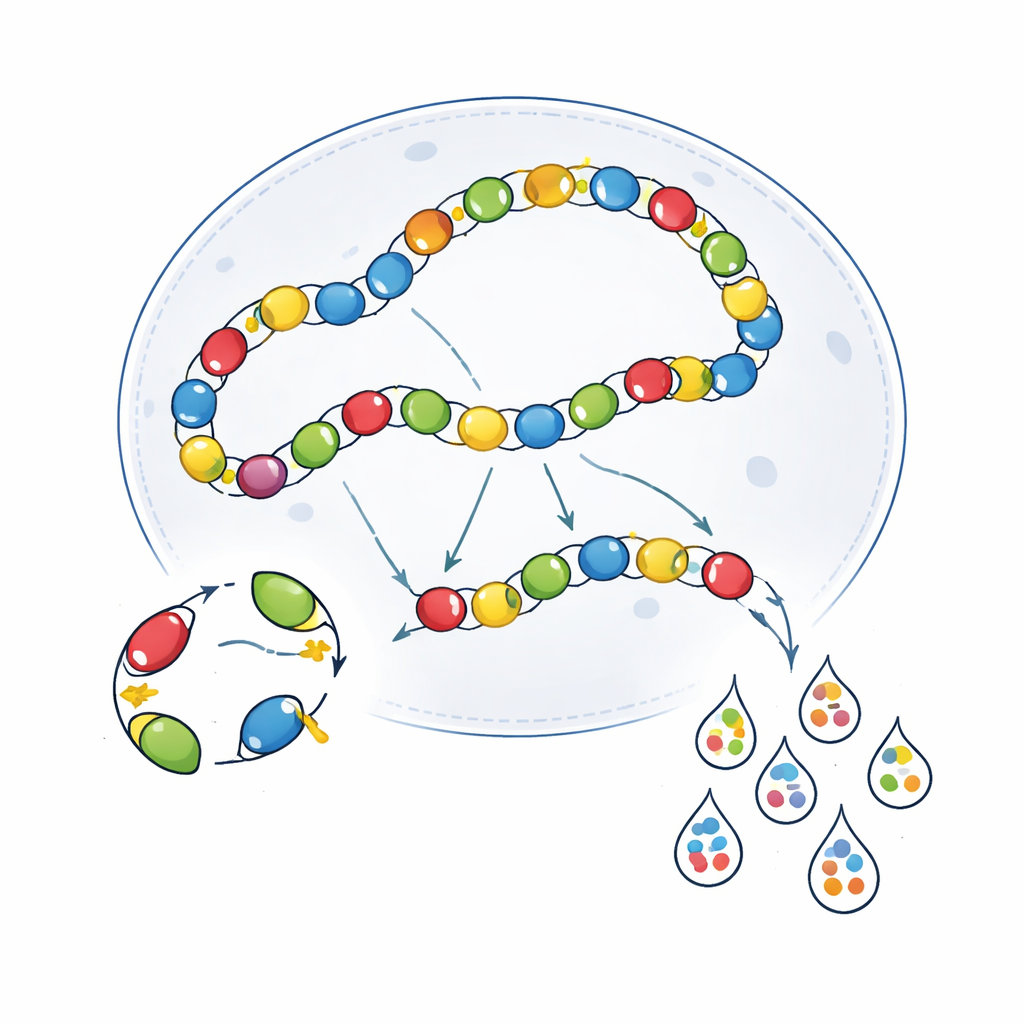
Biologisk korsprat inuti celler
Tekniska artefakter var bara en del av problemet. Virusen interagerar även inuti celler på sätt som suddar ut bilden. När de väl är inne i kärnan länkar AAV‑genom ofta ihop sig i ända‑till‑ända‑kedjor. I en sådan konfiguration kan en aktiv enhancer på ett viralt genom av misstag driva uttryck från ett intilliggande genom—ett fenomen kallat transkriptionellt korsprat. Författarna visade att när två olika enhancer‑AAVs ko‑injicerades kunde de stimulera varandras aktivitet i celltyper där den ena ensam normalt skulle vara tyst. Genom att använda immunodeficienta SCID‑möss, som har minskad AAV‑konkatenering, minskade man delvis detta överlapp för vissa enhancers men samtidigt försvagades det övergripande uttrycket och specificiteten förbättrades inte konsekvent. Försök att isolera virala genom med barriär‑DNA‑element visade likaledes endast kontextberoende fördelar och hjälpte i vissa hjärnregioner men inte i andra.
Varför brus slår hårdare mot vissa enhancers
Genom att jämföra många enhancers sida vid sida fann studien att de som riktar sig mot vanliga celltyper och ger starka fluorescenssignaler klarar sig bättre under multiplexade förhållanden. Svaga enhancers eller de som är aktiva i sällsynta cellpopulationer dränks oproportionerligt av bakgrundsbrus från kimeriska genom, korsprat och feldistribuerade streckkoder. Viktigt är att antal streckkodstranskript i multiplexade skärmar inte korrelerade väl med proteinnivåerna som mättes när varje enhancer testades för sig, vilket tyder på att mycket av streckkodssignalen i poolade experiment inte troget speglar verkligt enhancer‑drivet aktivitet.
Vad detta betyder för framtida verktyg för hjärnan
För icke‑specialister är slutsatsen att kombinera många enhancer‑utrustade virus i ett enda testdjur är mer komplicerat än det verkar. Virus kan omarrangera sig under produktion, påverka varandra inuti celler och generera vilseledande streckkodssignaler som får precisa enhancers att framstå som slarviga. Författarna drar slutsatsen att nuvarande multiplexade enhancer‑AAV‑screening ännu inte kan ersätta noggrann en‑och‑en‑validering, särskilt när man söker brett efter nya, finmaskigt riktade verktyg. Mindre och omsorgsfullt utformade pooler kan dock fortfarande vara användbara för att rangordna likartade enhancers eller optimera konstruktioner innan man går vidare till fullständig validering. Betydande tekniska och biologiska förbättringar krävs innan stora, opartiska poolade skärmar pålitligt kan avslöja de bästa genetiska ”nycklarna” för att rikta specifika hjärncellstyper.
Citering: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
Nyckelord: enhancer AAV, genleverans, single-cell RNA-sekvensering, viral barcoding, hjärncellstyper