Clear Sky Science · fr
Sources techniques et biologiques de bruit perturbent le criblage multiplexé d'améliorateurs par AAV
Trouver les bonnes clés génétiques
Les scientifiques s'appuient de plus en plus sur des virus vecteurs de gènes pour activer ou désactiver des types cellulaires cérébraux spécifiques, tant pour la recherche fondamentale que pour de potentielles thérapies. Mais pour rendre ces outils précis, il faut leur attacher les bons « interrupteurs », appelés améliorateurs, afin que chaque virus ne s'active que dans le type cellulaire visé. Cette étude montre que lorsque de nombreux virus équipés d'améliorateurs sont testés ensemble dans une même expérience, du bruit technique et biologique caché peut fortement brouiller les résultats, faisant paraître des outils prometteurs bien moins précis qu'ils ne le sont réellement.
Pourquoi le contrôle génique spécifique aux cellules est important
Les améliorateurs sont de courtes portions d'ADN qui favorisent l'activation de gènes dans des types cellulaires ou des régions cérébrales particuliers. En couplant ces améliorateurs à des adénovirus AAV, les chercheurs peuvent délivrer des marqueurs fluorescents ou des gènes thérapeutiques spécifiquement à, par exemple, un type de neurone ou une cellule gliale de support. Traditionnellement, chaque combinaison améliorateur–AAV est testée une par une chez l'animal — une méthode lente, coûteuse et difficile à étendre. Les approches multiplexées promettent un raccourci : mélanger de nombreux AAV portant des codes-barres différents, les injecter dans une souris, puis utiliser le séquençage ARN unicellulaire pour lire quel améliorateur était actif dans quelle cellule. En théorie, cela devrait révéler des dizaines de comportements d'améliorateurs en une seule expérience.
Quand de nombreuses expériences partagent une même souris
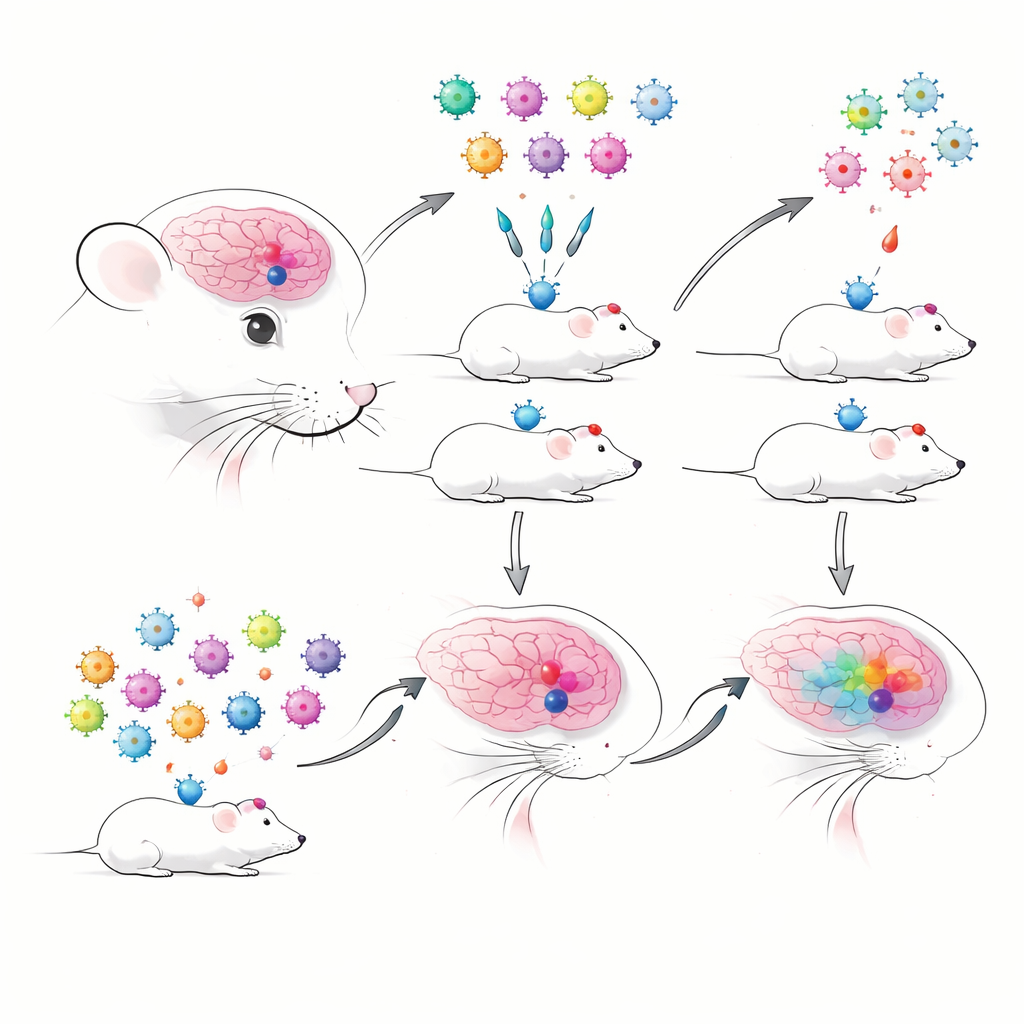
Les auteurs ont commencé par construire des AAV codés-barres qui portaient des améliorateurs bien caractérisés et connus pour cibler précisément certains types cellulaires cérébraux. Chaque améliorateur pilotait une protéine fluorescente et un court code-barres ARN, permettant le suivi par séquençage. Ils ont comparé les injections traditionnelles une par une aux injections « multiplexées » en pool, où de nombreux AAV-améliorateurs étaient délivrés simultanément et analysés par séquençage ARN unicellulaire en gouttelettes. Ils ont rapidement rencontré un obstacle pratique : dans les préparations basées sur les noyaux — utiles pour des tissus congelés ou fragiles — les codes-barres viraux étaient très mal détectés, tandis que les préparations de cellules entières capturaient beaucoup mieux les transcrits viraux. Cela les a contraints à privilégier les cellules entières, qui peuvent être plus fragiles et sous-représenter certains types cellulaires.
Mélanges cachés dans les génomes viraux
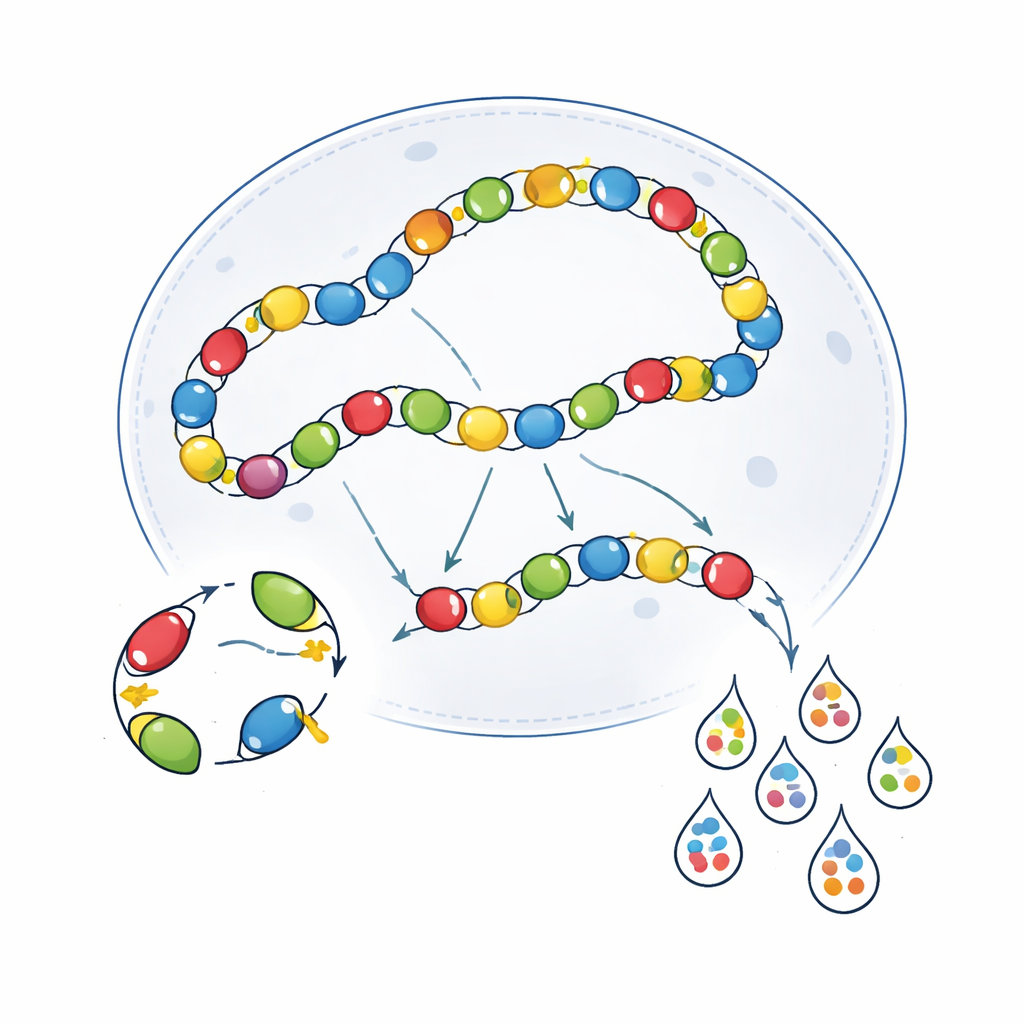
Même avec une meilleure capture des transcrits, les écrans multiplexés n'ont pas reproduit les motifs nets et spécifiques observés dans les tests un par un. De nombreux améliorateurs semblaient beaucoup moins sélectifs, en particulier ceux qui étaient naturellement plus faibles ou visant des types cellulaires rares. Pour enquêter, l'équipe a comparé des virus emballés individuellement puis mélangés, à des virus empaquetés ensemble à partir d'un pool de plasmides. Grâce au séquençage longue lecture, ils ont découvert que l'empaquetage en pool produisait un taux élevé de génomes « chimériques » — des particules virales dans lesquelles l'améliorateur et le code-barres avaient été brouillés et appariés de manière incorrecte. Ces particules chimériques ajoutent des signaux de code-barres trompeurs et diminuent la spécificité apparente. Les auteurs ont aussi testé un système à double code-barres (« scQers »), où chaque virus porte à la fois un code-barres lié à l'expression et un code-barres constitutif distinct. L'appariement de ces paires a permis de filtrer certaines lectures erronées et d'améliorer la spécificité, mais pas suffisamment pour retrouver les performances de la validation un par un.
Crosstalk biologique à l'intérieur des cellules
Les artefacts techniques n'expliquent qu'une partie du problème. Les virus eux-mêmes interagissent à l'intérieur des cellules d'une manière qui brouille les résultats. Une fois dans le noyau, les génomes AAV se lient souvent bout à bout, formant de longues concaténations. Dans cette configuration, un améliorateur actif sur un génome viral peut involontairement piloter l'expression depuis un génome voisin — un phénomène appelé crosstalk transcriptionnel. Les auteurs ont démontré que lorsque deux AAV-améliorateurs différents étaient co-injectés, ils pouvaient stimuler l'activité l'un de l'autre dans des types cellulaires où l'un seul serait normalement silencieux. L'utilisation de souris SCID immunodéficientes, caractérisées par une concaténation AAV réduite, a partiellement diminué ce recoupement pour certains améliorateurs mais a aussi affaibli l'expression globale, et n'a pas amélioré de manière systématique la spécificité. Les tentatives d'isoler les génomes viraux avec des éléments d'ADN barrières ont montré des bénéfices dépendant du contexte, utiles dans certaines régions du cerveau mais pas dans d'autres.
Pourquoi le bruit affecte certains améliorateurs davantage
En comparant de nombreux améliorateurs côte à côte, l'étude a montré que ceux ciblant des types cellulaires abondants et produisant des signaux fluorescents forts résistaient mieux aux conditions multiplexées. Les améliorateurs faibles ou actifs dans des populations cellulaires rares étaient disproportionnellement noyés par le bruit de fond provenant des génomes chimériques, du crosstalk et des codes-barres parasites. Il est important de noter que le nombre de transcrits de codes-barres dans les écrans multiplexés ne corrélait pas bien avec les niveaux de protéine mesurés lorsque chaque améliorateur était testé individuellement, ce qui suggère qu'une grande partie du signal de code-barres dans les expériences en pool ne reflète pas fidèlement l'activité réellement dirigée par l'améliorateur.
Qu'est-ce que cela signifie pour les outils cérébraux à venir
Pour les non-spécialistes, la conclusion est que combiner de nombreux virus porteurs d'améliorateurs dans un seul animal d'essai est plus compliqué qu'il n'y paraît. Les virus peuvent se réarranger lors de la production, interagir entre eux à l'intérieur des cellules et générer des signaux de code-barres trompeurs qui font paraître des améliorateurs précis comme peu fiables. Les auteurs concluent que les criblages multiplexés d'améliorateurs par AAV ne peuvent pas encore remplacer une validation soigneuse un par un, en particulier lorsqu'on cherche largement de nouveaux outils finement ciblés. Toutefois, de petits pools conçus avec soin peuvent rester utiles pour classer des améliorateurs similaires ou optimiser des designs avant de s'engager dans une validation complète. Des améliorations techniques et biologiques substantielles seront nécessaires avant que de larges écrans en pool, non biaisés, puissent révéler de manière fiable les meilleures « clés » génétiques pour cibler des types cellulaires cérébraux spécifiques.
Citation: Hunker, A.C., Mich, J.K., Taskin, N. et al. Technical and biological sources of noise confound multiplexed enhancer AAV screening. Nat Commun 17, 3738 (2026). https://doi.org/10.1038/s41467-026-72147-8
Mots-clés: enhancer AAV, livraison de gènes, séquençage ARN unicellulaire, codage viral, types cellulaires cérébraux