Clear Sky Science · zh
一种病毒性APOBEC3拮抗子将HHV-6A与HHV-6B区分开来
为何一些常见病毒使我们生病而另一些保持沉默
大多数成年人终生携带若干疱疹病毒,但只有其中一部分“搭便车者”会引起严重疾病。本研究提出了一个简单却意义深远的问题:在人类疱疹病毒6家族中,为什么一个成员(HHV-6B)常使婴儿和移植患者生病,而其近似亲缘体(HHV-6A)通常潜伏且不被察觉?通过追踪这些病毒与细胞内一套内建DNA防御系统的冲突,作者揭示了一场分子级的拉锯战,帮助解释它们截然不同的临床表现。 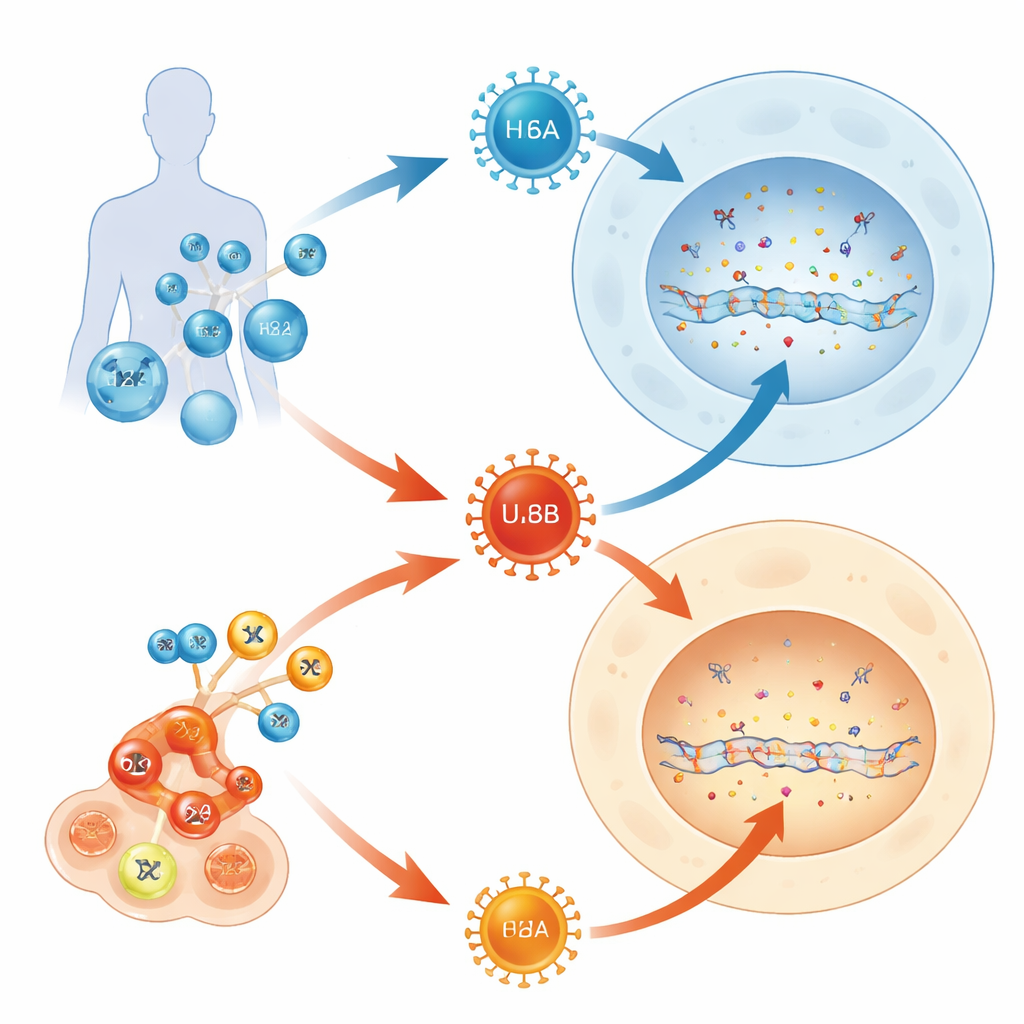
两种密切相关病毒的故事
HHV-6A和HHV-6B是高度相似的病毒,它们靶向相同类型的免疫细胞并共享超过90%的基因。然而它们在人体内的行为不同。HHV-6B是玫瑰疹的主要病原体,这是一种常见的儿童皮疹,在接受骨髓或高级T细胞治疗的患者中有时会导致脑炎。相比之下,HHV-6A通常沉默,很少与明确的疾病相关。由于两种病毒都使用已知受体进入细胞,作者怀疑关键差异发生在进入之后——即细胞自身处理DNA的机制内部。
细胞内建的DNA编辑器介入
我们的细胞会表达一组称为APOBEC3的酶,它们巡视DNA并能通过化学方式改变某些碱基来破坏病毒基因组,引发大量突变。通过比较不同T细胞系的基因活性,研究团队注意到几种APOBEC3基因在允许HHV-6B但不允许HHV-6A生长的细胞中更为活跃。当他们测序来自感染细胞的一段GC富集的病毒DNA时,HHV-6A携带了大量APOBEC特征的突变,而HHV-6B则基本完好。关闭单个APOBEC3基因,尤其是APOBEC3B和APOBEC3C,可促进HHV-6A的复制并显著降低其突变负荷,表明这一宿主防御系统确实限制HHV-6A。然而,在相同细胞中,HHV-6B在很大程度上逃避了这种DNA编辑。
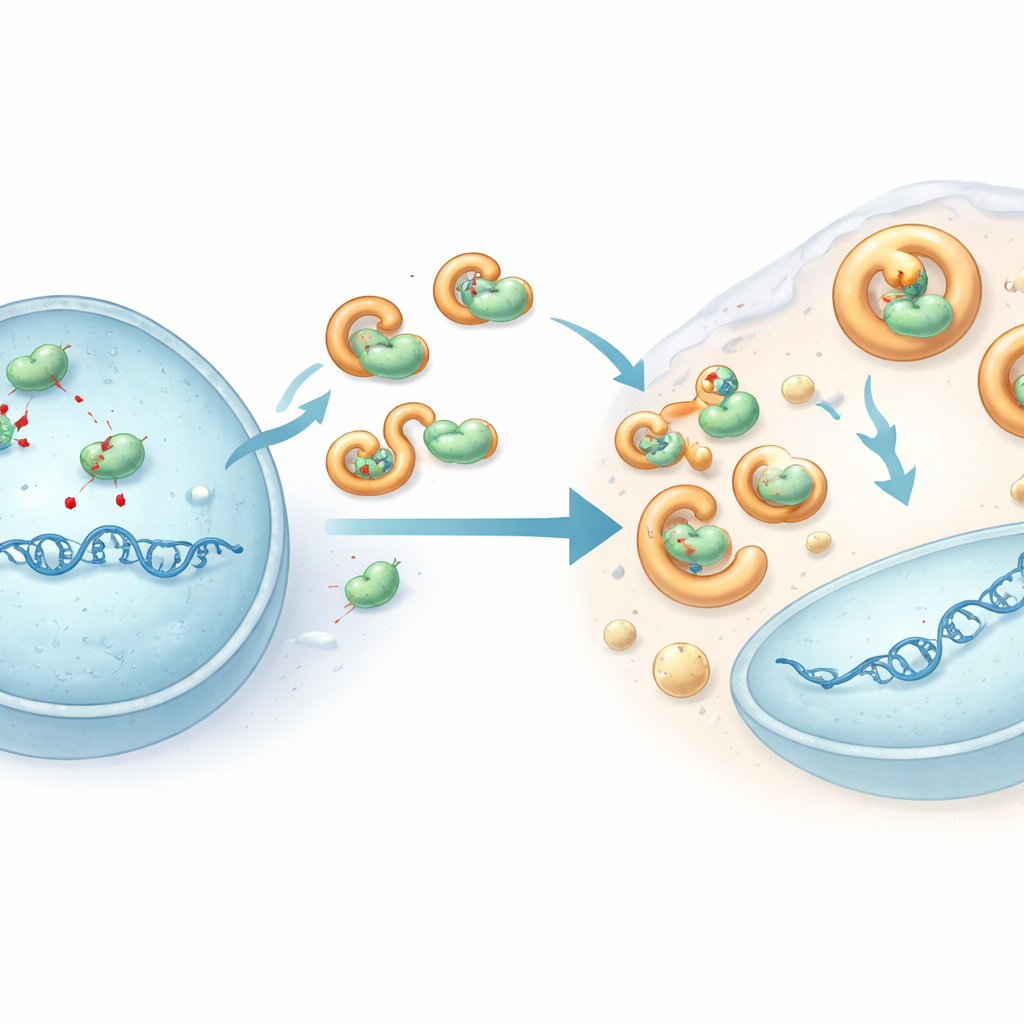
使编辑器失效的病毒盾牌
为理解HHV-6B如何躲避这一攻击,研究人员将注意力集中在一种称为U28的病毒蛋白上,这是一种许多疱疹病毒用于DNA合成的酶的改造形式。在HHV-6B感染的细胞中,APOBEC3B和APOBEC3C被从核(病毒DNA复制所在处)驱逐到细胞质,并且其总体水平下降。工程化细胞的实验表明,HHV-6B的U28蛋白可以物理结合多种APOBEC3蛋白,将它们拉入与细胞降解通路相连的类液滴结构,并促进它们的降解。这种隔离使这些酶远离病毒DNA,防止它们造成大规模损伤。当感染细胞中U28被减少时,APOBEC3水平回升,HHV-6B基因组累积更多突变,证实了U28作为抵抗这种抗病毒编辑的保护装置的作用。
表达上的小差异,结局上的大不同
有趣的是,HHV-6A的U28蛋白在序列上几乎与HHV-6B相同,并且在人为过表达时也能结合并降低APOBEC3蛋白。关键区别在于数量而非质量:在自然感染过程中,HHV-6B比HHV-6A更强烈地启动U28的表达。实验室感染和外周血原代细胞的测量显示,HHV-6B中U28的RNA水平远高于HHV-6A,同时其基因组得以更好地保存。在一例罕见的携带遗传性HHV-6A基因组并发生重新激活的患者中,研究团队检测到一组高度多样的HHV-6A变体,充满了APOBEC样突变,这与在移植和脑炎患者中观察到的相对稳定的HHV-6B序列形成对比。作者提出,HHV-6A较弱的U28表达使其易受细胞DNA编辑器的打击,从而限制其高效复制和传播的能力。
这对健康与疾病的意义
从通俗角度看,HHV-6B学会了解除一项关键的细胞警报,使其能够清洁地复制DNA并建立更强、更有时有害的感染。未能完全沉默这一防御的HHV-6A则被突变严重“刻痕”,因此可能复制较少并导致较少明显的疾病。通过将这些不同结果与控制U28表达强度的单一病毒开关联系起来,这项研究为为什么两种几乎相同的病毒会有如此不同的临床足迹提供了具体的分子解释。研究还强调了APOBEC3酶作为潜在的病毒进化塑造者,以及作为未来抗病毒策略的可能杠杆——这些策略既可旨在加强细胞的编辑器来对抗危险病毒,也可用于理解为何某些感染保持温和。
引用: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
关键词: 人类疱疹病毒6, APOBEC3, 病毒免疫逃逸, 病毒突变, U28 蛋白