Clear Sky Science · fr
Un antagoniste viral d’APOBEC3 distingue HHV-6A de HHV-6B
Pourquoi certains virus courants nous rendent malades et d’autres restent discrets
La plupart des adultes hébergent plusieurs herpèsvirus à vie, mais seuls certains de ces passagers occasionnent des maladies graves. Cette étude pose une question simple aux implications larges : pourquoi un membre de la famille du virus herpès humain 6 (HHV-6B) rend‑il souvent les nourrissons et les patients transplantés malades, tandis que son quasi‑jumeau (HHV-6A) reste généralement indétecté ? En retraçant la confrontation de ces virus avec un système de défense ADN intégré à nos cellules, les auteurs dévoilent une lutte moléculaire qui aide à expliquer leurs comportements cliniques très différents. 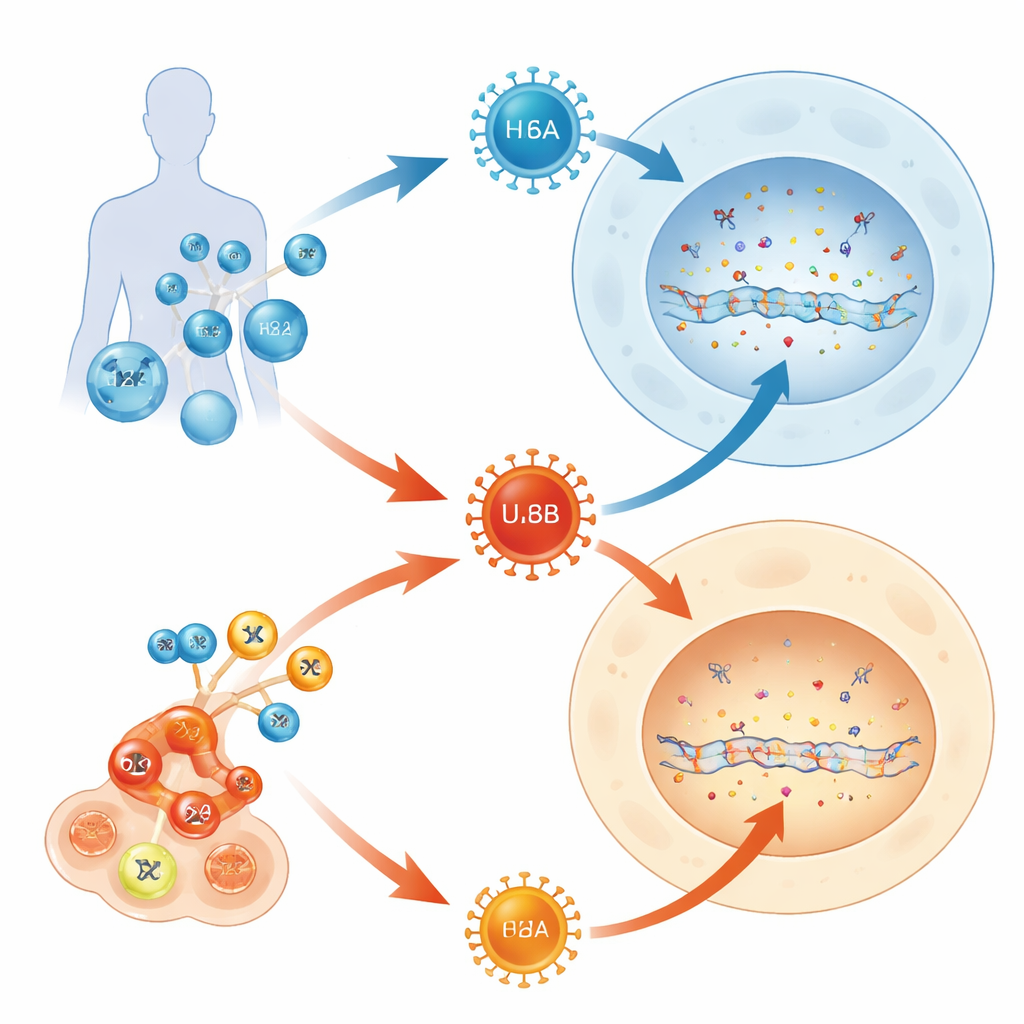
Le récit de deux virus étroitement liés
HHV-6A et HHV-6B sont des virus extrêmement similaires qui ciblent les mêmes types de cellules immunitaires et partagent plus de 90 % de leurs gènes. Pourtant, ils se comportent différemment chez l’homme. HHV-6B est la principale cause de la roséole, une éruption infantile fréquente qui peut parfois entraîner une inflammation cérébrale, en particulier chez les patients soumis à une greffe de moelle osseuse ou à des thérapies avancées à base de cellules T. HHV-6A, en revanche, reste généralement silencieux et est rarement associé à une maladie nette. Parce que les deux virus utilisent des récepteurs connus pour pénétrer dans les cellules, les auteurs ont supposé que ce qui se passe après l’entrée — au sein des mécanismes de gestion de l’ADN de la cellule — pourrait être la clé de leur impact différent.
L’éditeur d’ADN intégré de la cellule intervient
Nos cellules expriment un groupe d’enzymes appelées protéines APOBEC3 qui patrouillent l’ADN et peuvent saboter les génomes viraux en convertissant chimiquement certaines bases, déclenchant une tempête de mutations. En comparant l’activité génique dans différentes lignées de cellules T, l’équipe a remarqué que plusieurs gènes APOBEC3 étaient plus actifs dans des cellules qui permettent la croissance de HHV-6B, mais pas de HHV-6A. Lorsqu’ils ont séquencé une région riche en GC de l’ADN viral provenant de cellules infectées, HHV-6A portait un lourd fardeau de mutations de type APOBEC, tandis que HHV-6B restait en grande partie intact. La désactivation de gènes APOBEC3 individuels, en particulier APOBEC3B et APOBEC3C, a augmenté la réplication de HHV-6A et réduit fortement sa charge mutationnelle, montrant que ce système de défense de l’hôte limite réellement HHV-6A. HHV-6B, cependant, échappait en grande partie à cette édition de l’ADN dans les mêmes cellules.
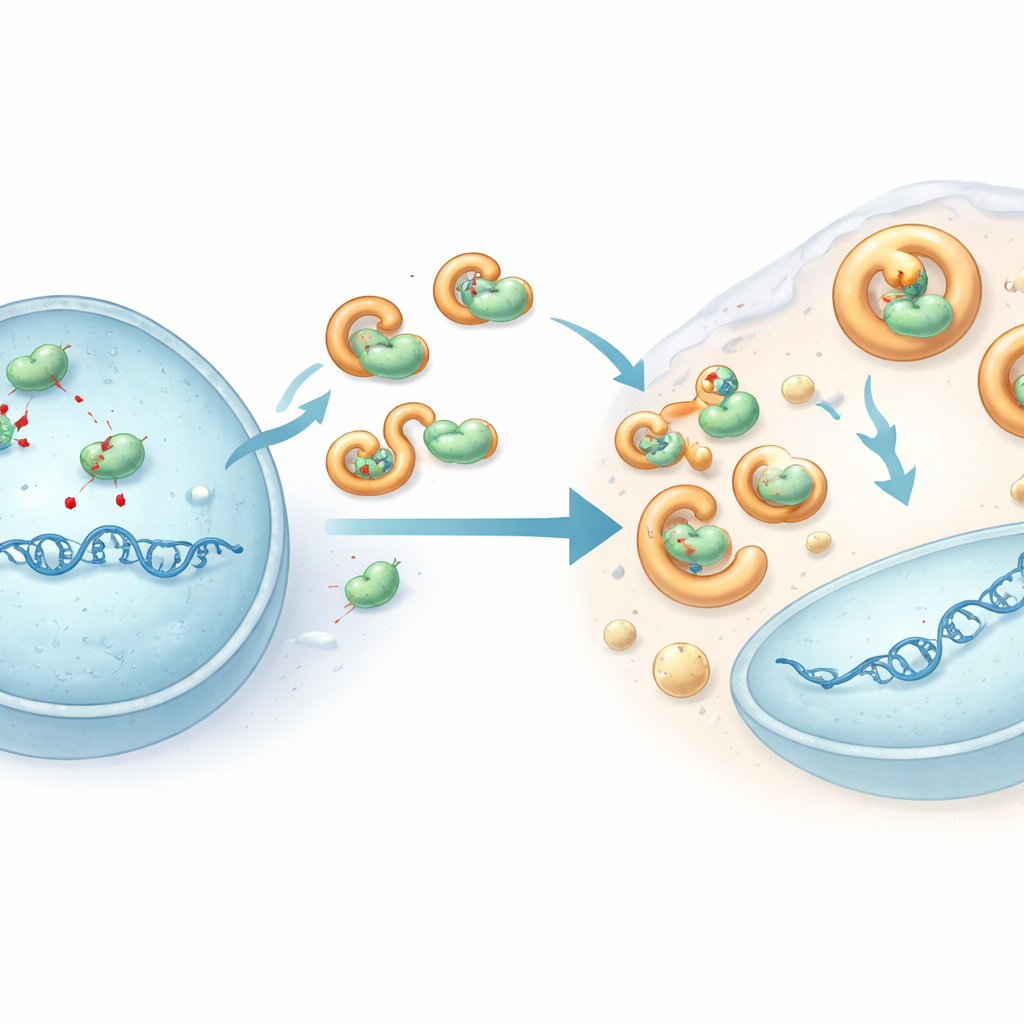
Un bouclier viral qui désarme l’éditeur
Pour comprendre comment HHV-6B évite cette attaque, les chercheurs se sont concentrés sur une protéine virale appelée U28, une version modifiée d’une enzyme que de nombreux herpèsvirus utilisent pour la synthèse de l’ADN. Dans les cellules infectées par HHV-6B, APOBEC3B et APOBEC3C étaient expulsées du noyau (où l’ADN viral est copié) vers le fluide environnant et leurs niveaux globaux diminuaient. Des expériences dans des cellules modifiées ont montré que la protéine U28 de HHV-6B se lie physiquement à plusieurs protéines APOBEC3, les entraîne dans des gouttelettes à apparence liquide liées aux voies d’élimination cellulaires, et favorise leur dégradation. Cette séquestration éloigne les enzymes de l’ADN viral et les empêche d’infliger des dommages étendus. Lorsque U28 était réduit dans des cellules infectées, les niveaux d’APOBEC3 rebondissaient et les génomes de HHV-6B accumulaient davantage de mutations, confirmant que U28 agit comme une armure contre cette édition antivirale.
De petites différences d’expression, de grands écarts de résultat
Curieusement, la protéine U28 de HHV-6A est presque identique en séquence à celle de HHV-6B et peut aussi se lier et diminuer les protéines APOBEC3 lorsqu’elle est surexprimée artificiellement. La distinction cruciale est quantitative, non qualitative : au cours d’une infection naturelle, HHV-6B active U28 beaucoup plus fortement que HHV-6A. Des mesures lors d’infections en laboratoire et dans des cellules sanguines primaires ont montré des niveaux d’ARN U28 bien plus élevés pour HHV-6B, ainsi qu’une meilleure préservation de son génome. Chez un patient rare présentant une réactivation d’un génome HHV-6A hérité, l’équipe a détecté une population remarquablement diverse de variantes HHV-6A remplies de mutations de type APOBEC, en contraste avec les séquences relativement stables de HHV-6B observées chez des patients transplantés et atteints d’encéphalite. Les auteurs proposent que l’expression faible de U28 chez HHV-6A le laisse vulnérable à l’éditeur d’ADN de la cellule, limitant sa capacité à se répliquer efficacement et à se propager.
Ce que cela signifie pour la santé et la maladie
Du point de vue grand public, HHV-6B a appris à désarmer une alarme cellulaire clé, lui permettant de copier son ADN proprement et d’établir des infections plus robustes, parfois nuisibles. HHV-6A, qui n’arrive pas à neutraliser complètement cette défense, est fortement marquée par des mutations et peut donc se répliquer moins et provoquer moins de maladies évidentes. En reliant ces issues à un interrupteur viral unique qui contrôle l’intensité de production de U28, l’étude propose une explication moléculaire concrète à la raison pour laquelle deux virus quasi identiques peuvent avoir des empreintes cliniques si différentes. Elle met également en lumière les enzymes APOBEC3 comme des acteurs potentiels de l’évolution virale et comme leviers possibles pour de futures stratégies antivirales visant soit à renforcer l’éditeur cellulaire contre les virus dangereux, soit à comprendre pourquoi certaines infections restent bénignes.
Citation: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Mots-clés: herpèsvirus humain 6, APOBEC3, échappement immunitaire viral, mutation virale, protéine U28