Clear Sky Science · sv
En viral APOBEC3‑antagonist skiljer HHV‑6A från HHV‑6B
Varför vissa vanliga virus gör oss sjuka medan andra förblir tysta
De flesta vuxna bär på flera herpesvirus livet ut, men bara några av dessa följeslagare orsakar någonsin allvarliga sjukdomar. Denna studie ställer en enkel fråga med långtgående konsekvenser: varför gör ett medlem i familjen humant herpesvirus 6 (HHV‑6B) ofta spädbarn och transplanterade patienter sjuka, medan dess nära tvilling (HHV‑6A) vanligtvis ligger oupptäckt? Genom att följa hur dessa virus krockar med ett inbyggt DNA‑försvar i våra celler avslöjar författarna ett molekylärt dragkamp som hjälper till att förklara deras mycket olika kliniska beteenden. 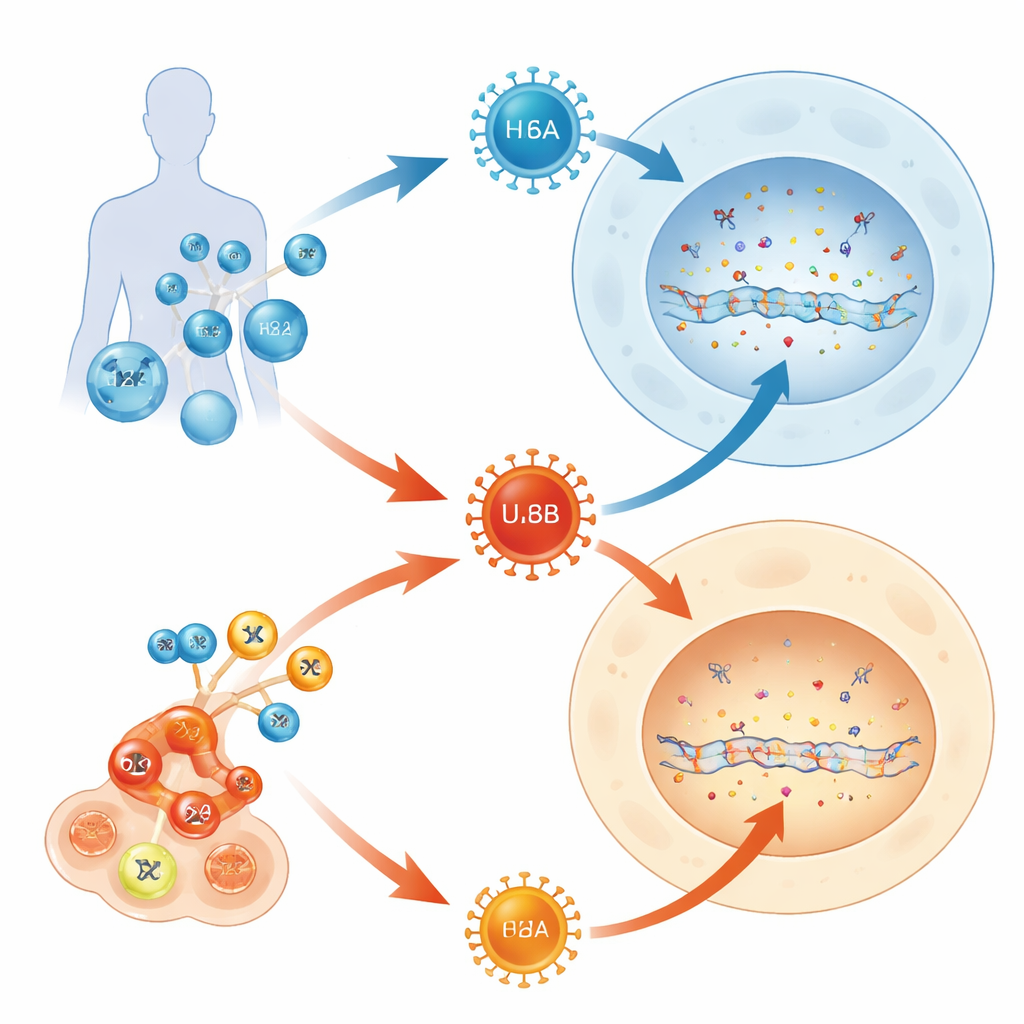
En berättelse om två nära besläktade virus
HHV‑6A och HHV‑6B är mycket lika virus som riktar sig mot samma typer av immunceller och delar mer än 90 % av sina gener. Ändå beter de sig olika hos människor. HHV‑6B är huvudorsaken till rosfeber (roseola), ett vanligt barnutslag som ibland kan leda till hjärninflammation, särskilt hos patienter som genomgår benmärgs‑ eller avancerade T‑cellsbehandlingar. HHV‑6A däremot är vanligtvis tyst och sällan kopplat till tydlig sjukdom. Eftersom båda virusen använder kända receptorer för att ta sig in i celler misstänkte författarna att vad som händer efter inträdet — inne i cellens egen DNA‑hanteringsmaskin — kan vara nyckeln till deras olika påverkan.
Cellens inbyggda DNA‑redigerare går in i bilden
Våra celler uttrycker en grupp enzymer kallade APOBEC3‑proteiner som patrullerar DNA och kan sabotera virusgenom genom att kemiskt omvandla vissa DNA‑bokstäver, vilket utlöser en storm av mutationer. Genom att jämföra genaktivitet i olika T‑cellslinjer noterade teamet att flera APOBEC3‑gener var mer aktiva i celler som tillåter HHV‑6B, men inte HHV‑6A, att växa. När de sekvenserade en GC‑rik sträcka av viralt DNA från infekterade celler bar HHV‑6A en tung börda av APOBEC‑liknande mutationer, medan HHV‑6B förblev i stort sett intakt. Att stänga av enskilda APOBEC3‑gener, särskilt APOBEC3B och APOBEC3C, ökade HHV‑6A‑replikationen och minskade kraftigt dess mutationsbörda, vilket visar att detta värdförsvar verkligen begränsar HHV‑6A. HHV‑6B undkom däremot i stor utsträckning denna DNA‑redigering i samma celler.
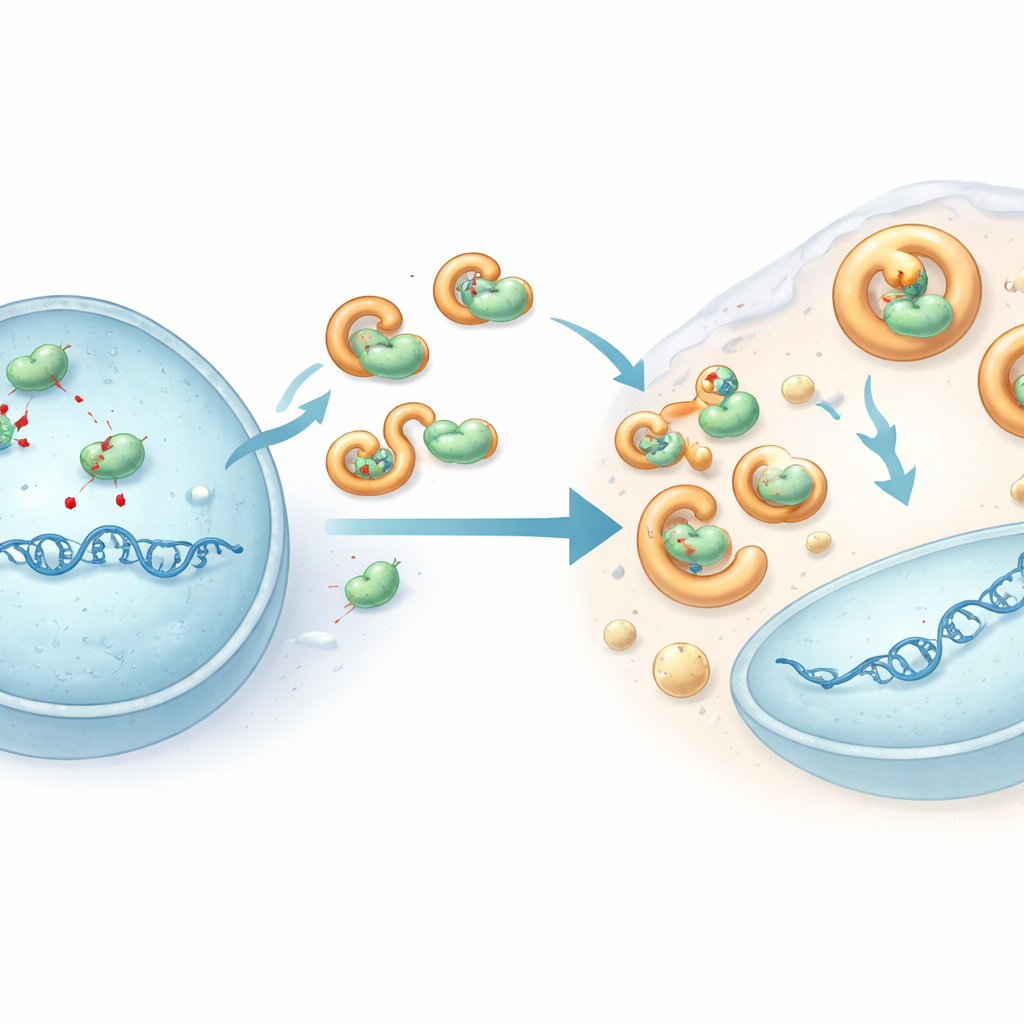
En viral sköld som avväpnar redigeraren
För att förstå hur HHV‑6B undviker denna attack fokuserade forskarna på ett viralt protein kallat U28, en modifierad version av ett enzym som många herpesvirus använder för DNA‑byggnad. I HHV‑6B‑infekterade celler fördes APOBEC3B och APOBEC3C ut ur kärnan (där viralt DNA kopieras) och in i den omgivande vätskan, och deras totala nivåer sjönk. Experiment i konstruerade celler visade att HHV‑6B‑U28 fysiskt binder flera APOBEC3‑proteiner, drar dem in i vätskeliknande droppar kopplade till cellulära nedbrytningsvägar och främjar deras nedbrytning. Denna sequestrering håller enzymerna borta från viralt DNA och förhindrar att de åstadkommer omfattande skada. När U28 reducerades i infekterade celler återhämtade sig APOBEC3‑nivåerna och HHV‑6B‑genom samlade på sig fler mutationer, vilket bekräftar att U28 fungerar som en rustning mot denna antivirala redigering.
Små skillnader i uttryck, stora skillnader i utfall
Det är anmärkningsvärt att U28‑proteinet från HHV‑6A nästan är identiskt i sekvens med det från HHV‑6B och kan också binda och sänka APOBEC3‑proteiner när det överproduceras konstgjort. Den avgörande skillnaden är kvantitet, inte kvalitet: under naturlig infektion slår HHV‑6B på U28 mycket starkare än HHV‑6A. Mätningar i laboratorieinfektioner och i primära blodceller visade mycket högre nivåer av U28‑RNA i HHV‑6B, tillsammans med bättre bevarande av dess genom. Hos en sällsynt patient med reaktivering av ett ärvt HHV‑6A‑genom upptäckte teamet en påfallande divers grupp HHV‑6A‑varianter fulla av APOBEC‑liknande mutationer, i kontrast till de relativt stabila HHV‑6B‑sekvenser som ses hos transplanterade patienter och i encefalitfall. Författarna föreslår att HHV‑6A:s svaga U28‑uttryck lämnar det sårbart för cellens DNA‑redigerare, vilket begränsar dess förmåga att replikera effektivt och spridas.
Vad detta betyder för hälsa och sjukdom
Ur ett lekmannaperspektiv har HHV‑6B lärt sig att avväpna ett viktigt cellulärt larm, vilket låter det kopiera sitt DNA rent och etablera starkare, ibland skadliga infektioner. HHV‑6A, som inte helt lyckas tysta detta försvar, blir hårt märkt av mutationer och kan därför replikera mindre och orsaka färre tydliga sjukdomar. Genom att koppla dessa utfall till en enda viral brytare som styr hur starkt U28 produceras erbjuder studien en konkret molekylär förklaring till varför två nästan identiska virus kan ha så olika kliniska fotavtryck. Den lyfter också fram APOBEC3‑enzymer som potentiella formare av viral evolution och som möjliga verktyg för framtida antivirala strategier som antingen syftar till att förstärka cellens redigerare mot farliga virus eller att förstå varför vissa infektioner förblir lindriga.
Citering: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Nyckelord: humant herpesvirus 6, APOBEC3, viral immunundvikelse, virusmutation, U28‑protein