Clear Sky Science · nl
Een viraal APOBEC3-antagonist onderscheidt HHV-6A van HHV-6B
Waarom sommige alledaagse virussen ons ziek maken en andere stil blijven
De meeste volwassenen dragen meerdere herpesvirussen levenslang bij zich, maar slechts enkele van deze inzittenden veroorzaken ooit ernstige ziekte. Deze studie stelt een eenvoudige vraag met verstrekkende implicaties: waarom maakt het ene lid van de familie humaan herpesvirus 6 (HHV-6B) vaak zuigelingen en transplantatiepatiënten ziek, terwijl zijn bijna‑tweeling (HHV-6A) meestal onopgemerkt blijft? Door te volgen hoe deze virussen botsen met een ingebouwd DNA-verdedigingssysteem in onze cellen, onthullen de auteurs een moleculaire touwtrekwedstrijd die helpt hun heel verschillende klinische gedragingen te verklaren. 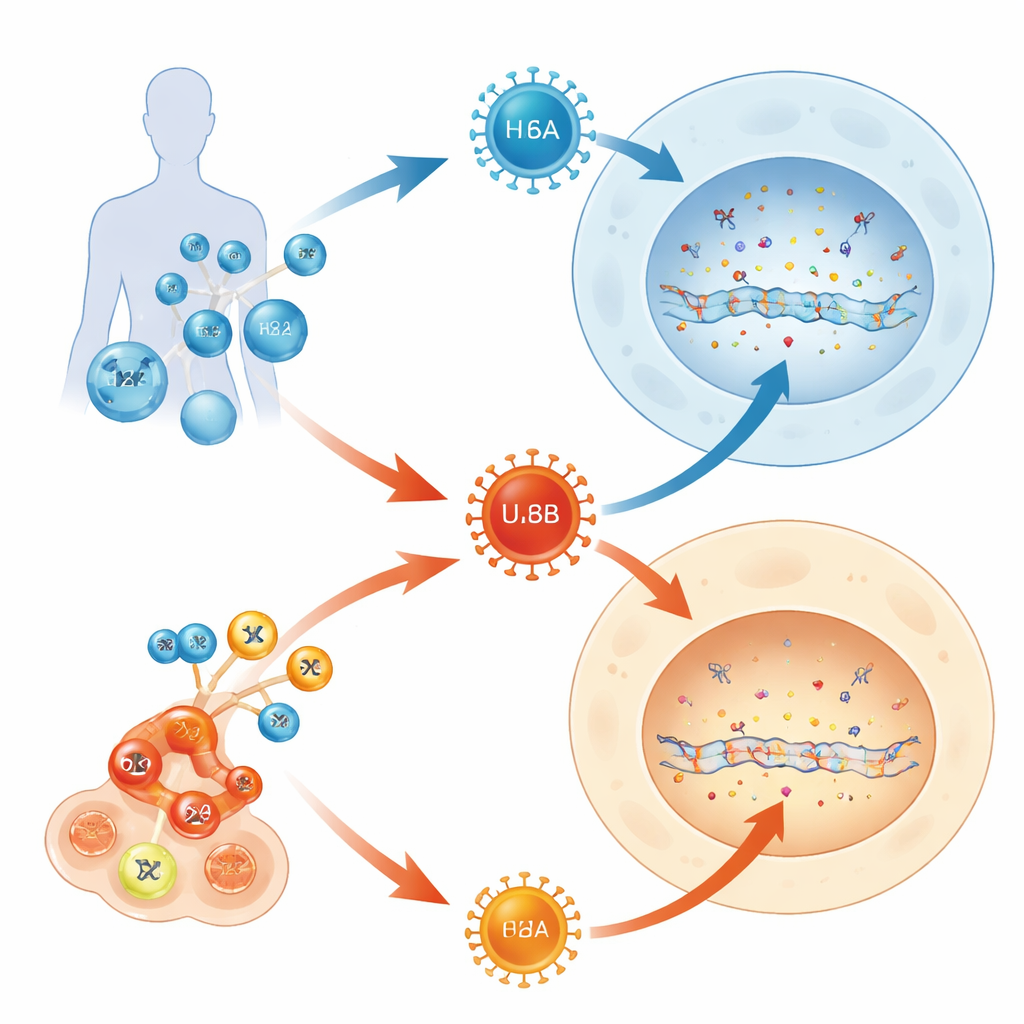
Een verhaal van twee nauw verwante virussen
HHV-6A en HHV-6B zijn extreem vergelijkbare virussen die dezelfde typen immuuncellen aantasten en meer dan 90% van hun genen delen. Toch gedragen ze zich verschillend in mensen. HHV-6B is de belangrijkste oorzaak van exanthema subitum (rozehondje), een veelvoorkomende kinderuitslag die soms kan leiden tot hersenontsteking, vooral bij patiënten die een beenmergtransplantatie of geavanceerde T‑celtherapieën ondergaan. HHV-6A daarentegen is meestal stil en zelden duidelijk gekoppeld aan ziekte. Omdat beide virussen bekende receptoren gebruiken om cellen binnen te dringen, vermoedden de auteurs dat wat er na binnenkomst gebeurt — binnen de DNA‑verwerkingsmachinerie van de cel — wel eens de sleutel tot hun verschillende impact zou kunnen zijn.
De ingebouwde DNA‑editor van de cel grijpt in
Onze cellen maken een groep enzymen aan die APOBEC3-eiwitten worden genoemd; die patrouilleren DNA en kunnen virale genomen saboteren door bepaalde DNA‑letters chemisch om te zetten, waardoor een storm van mutaties ontstaat. Door genactiviteit te vergelijken in verschillende T‑cellijnen merkte het team dat meerdere APOBEC3-genen actiever waren in cellen die HHV-6B, maar niet HHV-6A, toestonden te groeien. Toen ze een GC‑rijke regio van viraal DNA uit geïnfecteerde cellen sequentieerden, droeg HHV-6A een zware last aan APOBEC‑achtige mutaties, terwijl HHV-6B grotendeels intact bleef. Het uitschakelen van afzonderlijke APOBEC3-genen, vooral APOBEC3B en APOBEC3C, versterkte HHV-6A‑replicatie en verminderde scherp de mutatielast, wat aantoont dat dit gastheerverdedigingssysteem HHV-6A daadwerkelijk beperkt. HHV-6B ontsnapte in dezelfde cellen grotendeels aan deze DNA‑editing.
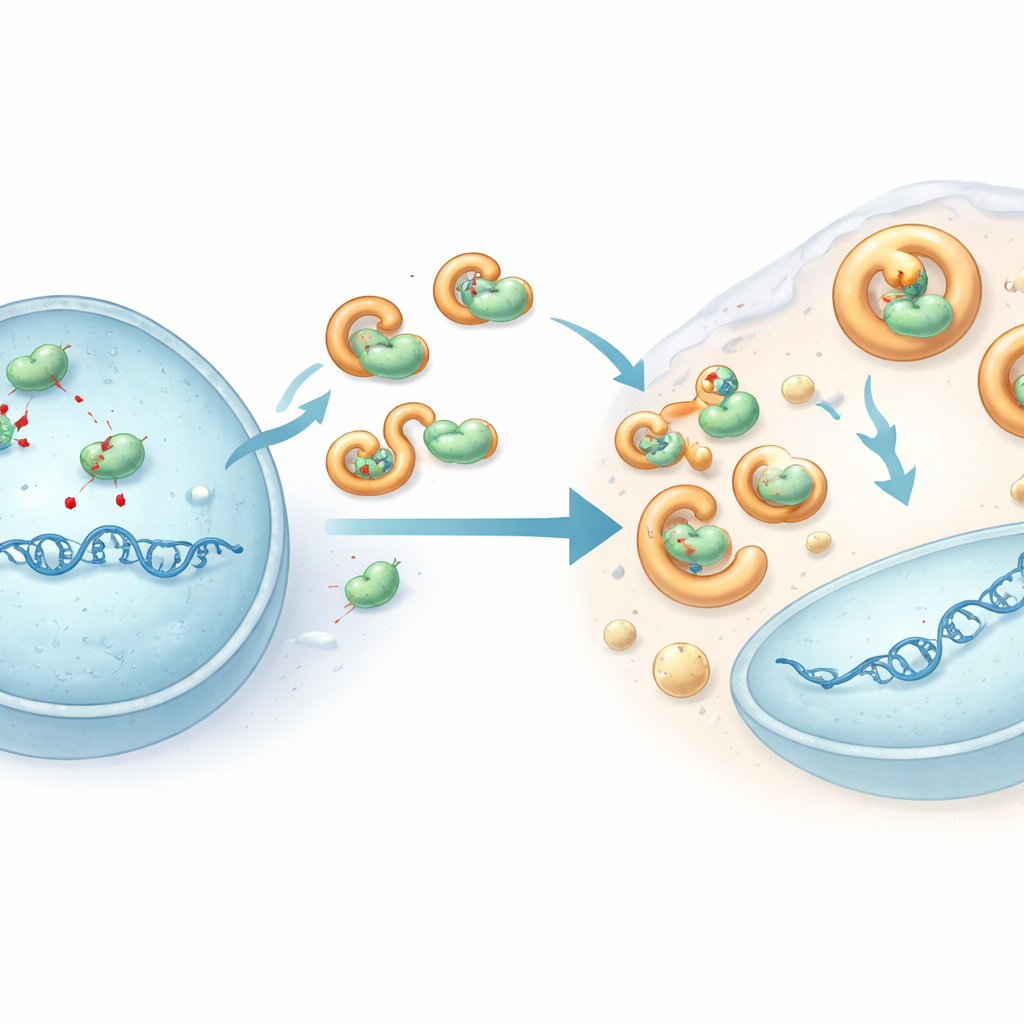
Een viraal schild dat de editor ontwapent
Om te begrijpen hoe HHV-6B deze aanval ontwijkt, richtten de onderzoekers zich op één viraal eiwit genaamd U28, een aangepaste versie van een enzym dat veel herpesvirussen gebruiken voor DNA‑bouw. In HHV-6B‑geïnfecteerde cellen werden APOBEC3B en APOBEC3C uit de kern (waar viraal DNA wordt gekopieerd) naar het omliggende cytosol geduwd en daalden hun totale niveaus. Experimenten in gemodificeerde cellen lieten zien dat het HHV-6B U28‑eiwit fysiek aan meerdere APOBEC3‑eiwitten vastklikt, ze in vloeibare‑achtige druppels trekt die verbonden zijn met cellulaire afvoerpaden, en hun afbraak bevordert. Deze sequestratie houdt de enzymen weg van viraal DNA en voorkomt dat ze wijdverspreide schade aanrichten. Wanneer U28 in geïnfecteerde cellen werd verminderd, herstelden de APOBEC3‑niveaus en stapelden HHV-6B‑genomen meer mutaties op, wat bevestigt dat U28 fungeert als pantser tegen deze antivirale editing.
Kleine verschillen in expressie, grote verschillen in uitkomst
Interessant genoeg is het U28‑eiwit van HHV-6A bijna identiek in sequentie aan dat van HHV-6B en kan het ook binden aan en APOBEC3‑eiwitten verlagen wanneer het kunstmatig overgeproduceerd wordt. Het cruciale verschil is hoeveelheid, niet kwaliteit: tijdens natuurlijke infectie zet HHV-6B U28 veel sterker aan dan HHV-6A. Metingen in laboratoriuminfecties en in primaire bloedcellen toonden veel hogere U28‑RNA‑niveaus in HHV-6B, samen met betere instandhouding van zijn genoom. In een zeldzame patiënt met reactivering van een geërfd HHV-6A‑genoom detecteerde het team een opvallend diverse zwerm van HHV-6A‑varianten vol APOBEC‑achtige mutaties, in tegenstelling tot de relatief stabiele HHV-6B‑sequenties die werden gezien bij transplantatie‑ en encefalitispatiënten. De auteurs stellen voor dat de zwakke U28‑expressie van HHV-6A het kwetsbaar maakt voor de DNA‑editor van de cel, waardoor zijn vermogen om efficiënt te repliceren en zich te verspreiden beperkt wordt.
Wat dit betekent voor gezondheid en ziekte
Voor een lekenperspectief heeft HHV-6B geleerd een sleutelsignaal van de cel uit te schakelen, waardoor het zijn DNA schoon kan kopiëren en sterkere, soms schadelijke infecties kan vestigen. HHV-6A, dat er niet in slaagt deze verdediging volledig te onderdrukken, raakt zwaar getekend door mutaties en kan daardoor minder repliceren en minder vaak duidelijke ziekten veroorzaken. Door deze uitkomsten te koppelen aan een enkele virale schakel die bepaalt hoe sterk U28 wordt geproduceerd, biedt de studie een concreet moleculair verklaringsmodel voor waarom twee bijna identieke virussen zulke verschillende klinische voetafdrukken kunnen hebben. Het benadrukt ook APOBEC3‑enzymen als potentiële vormers van virale evolutie en als mogelijke knoppen voor toekomstige antivirale strategieën die ernaar streven óf de editor van de cel tegen gevaarlijke virussen te versterken, óf te begrijpen waarom sommige infecties mild blijven.
Bronvermelding: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Trefwoorden: humaan herpesvirus 6, APOBEC3, viraire immuunontwijking, virusmutatie, U28-eiwit