Clear Sky Science · tr
Viral bir APOBEC3 antagonisti HHV-6A ile HHV-6B’yi ayırt ediyor
Neden bazı yaygın virüsler hastalık yapar, bazıları sessiz kalır
Çoğu yetişkin yaşam boyu birkaç herpesvirüs taşır, ancak bu yolcuların sadece bazıları ciddi hastalıklara yol açar. Bu çalışma, geniş çaplı çıkarımları olan basit bir soruyu soruyor: insan herpesvirüsü 6 ailesinin bir üyesi (HHV-6B) neden sıklıkla bebeklerde ve nakil hastalarında hastalığa neden olurken, onun neredeyse ikizi olan HHV-6A genellikle fark edilmeden mi kalıyor? Bu virüslerin hücrelerimizdeki yerleşik DNA savunma sistemiyle nasıl çatıştığını izleyerek, yazarlar klinik davranışlarındaki bu büyük farkı açıklamaya yardımcı olan moleküler bir çekişmeyi ortaya koyuyor. 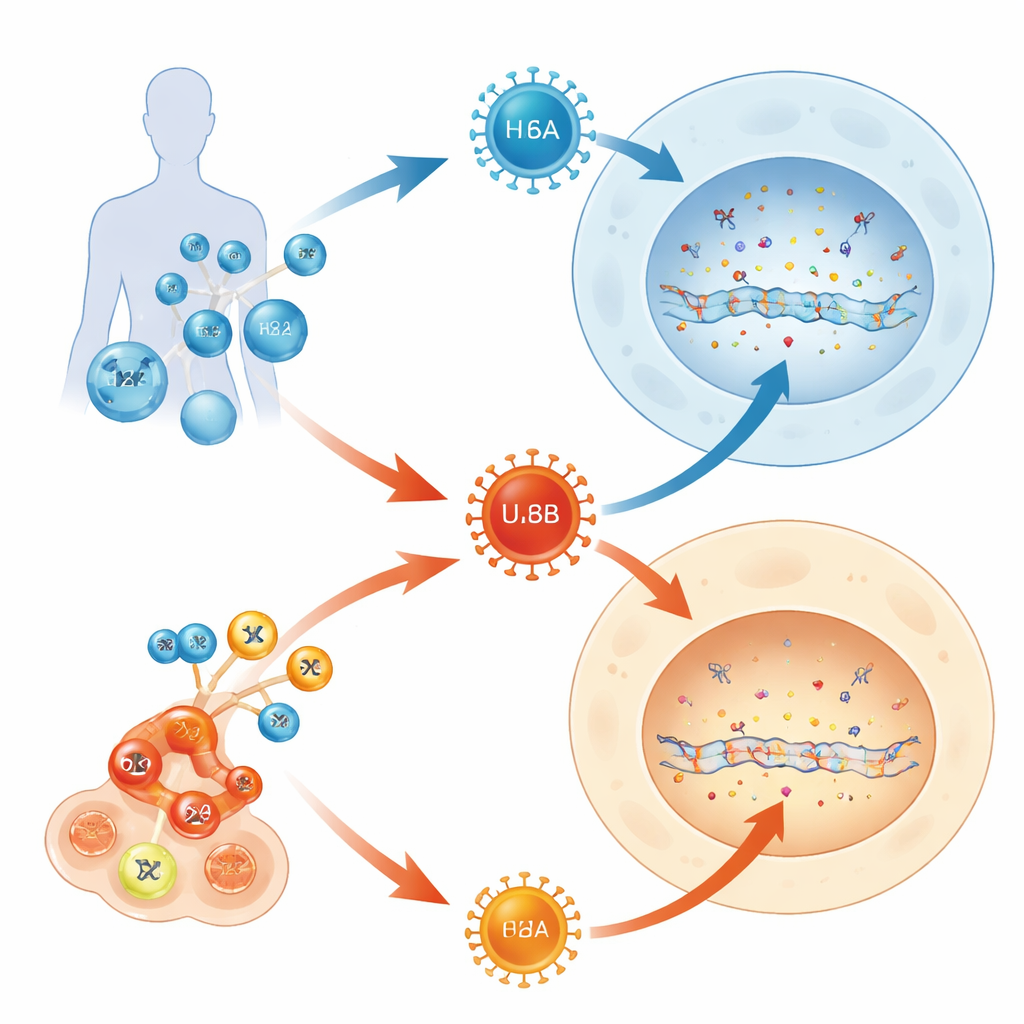
Çok yakın akraba iki virüsün öyküsü
HHV-6A ve HHV-6B, aynı tür bağışıklık hücrelerini hedefleyen ve genlerinin %90’ından fazlasını paylaşan son derece benzer virüslerdir. Yine de insanlardaki davranışları farklıdır. HHV-6B, bazen özellikle kemik iliği nakli veya ileri T‑hücre tedavileri gören hastalarda beyin iltihaline yol açabilen yaygın bir çocuk döküntüsü olan roseolanın başlıca nedenidir. Buna karşın HHV-6A genellikle sessizdir ve nadiren açık bir hastalıkla ilişkilendirilir. Her iki virüs de hücreye giriş için bilinen reseptörleri kullandığından, yazarlar girişten sonra—hücrenin kendi DNA işlemleri içinde—gerçekleşenin farklı etkilerin anahtarı olabileceğini düşündüler.
Hücresel yerleşik DNA editörü devreye giriyor
Hücrelerimiz, DNA’yı devriye gezen ve viral genomları belirli DNA harflerini kimyasal olarak dönüştürerek sabote edebilen APOBEC3 proteinleri adlı bir enzim grubunu ifade eder. Farklı T‑hücre dizilerinde gen etkinliğini karşılaştırarak ekip, birkaç APOBEC3 geninin HHV-6B’nin büyümesine izin veren ancak HHV-6A’nın büyümesine izin vermeyen hücrelerde daha aktif olduğunu fark etti. Enfekte hücrelerden alınan GC‑zengin bir viral DNA dizisini sıraladıklarında, HHV-6A ağır bir APOBEC‑stil mutasyon yükü taşırken HHV-6B çoğunlukla sağlam kaldı. Bireysel APOBEC3 genlerini, özellikle APOBEC3B ve APOBEC3C’yi kapattıklarında HHV-6A replikasyonu arttı ve mutasyon yükü keskin biçimde azaldı; bu da bu konak savunma sisteminin gerçekten HHV-6A’yı sınırladığını gösterdi. Öte yandan HHV-6B aynı hücrelerde büyük ölçüde bu DNA düzenlemesinden kaçıyordu.
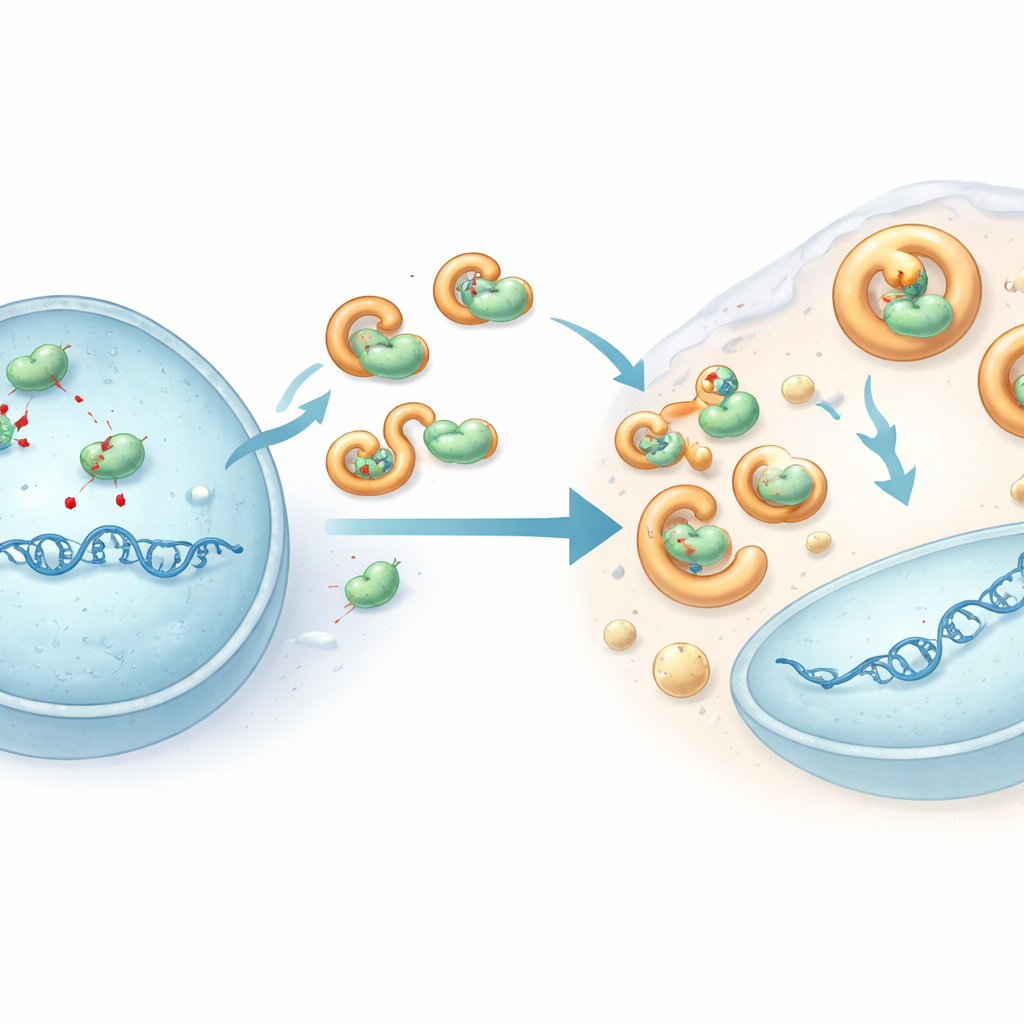
Editörü etkisiz hale getiren viral bir kalkan
HHV-6B’nin bu saldırıdan nasıl kaçtığını anlamak için araştırmacılar U28 adlı tek bir viral proteine odaklandı; bu protein birçok herpesvirüsün DNA yapımında kullandığı bir enzimin değiştirilmiş bir versiyonudur. HHV-6B ile enfekte hücrelerde APOBEC3B ve APOBEC3C, viral DNA’nın kopyalandığı çekirdekten (nükleustan) çekilerek çevresindeki sıvıya itildi ve toplam seviyeleri düştü. Tasarlanmış hücrelerde yapılan deneyler, HHV-6B U28 proteininin birkaç APOBEC3 proteinine fiziksel olarak bağlandığını, onları hücresel bertaraf yollarına bağlı sıvı‑benzeri damlacıklara çektiğini ve parçalanmalarını teşvik ettiğini gösterdi. Bu tutma, enzimleri viral DNA’dan uzak tutarak geniş çaplı hasar vermelerini engelliyordu. Enfekte hücrelerde U28 azaltıldığında APOBEC3 seviyeleri geri döndü ve HHV-6B genomları daha fazla mutasyon biriktirdi; bu da U28’in bu antivirale karşı zırh görevi gördüğünü doğruladı.
İfade düzeyindeki küçük farklar, sonuçta büyük farklılıklar
İlginç biçimde, HHV-6A’dan gelen U28 proteini dizilimi HHV-6B’dekine neredeyse özdeştir ve yapay olarak aşırı üretilirse APOBEC3 proteinlerine bağlanıp düzeylerini düşürebilir. Kritik ayrım nicelik, nitelik değil: doğal enfeksiyon sırasında HHV-6B, U28’i HHV-6A’dan çok daha güçlü açıyor. Laboratuvar enfeksiyonları ve primer kan hücrelerindeki ölçümler, HHV-6B’de çok daha yüksek U28 RNA seviyeleri ve buna paralel olarak genomunun daha iyi korunmasını gösterdi. Miras yoluyla geçen bir HHV-6A genomunun nadir reaktivasyonunda ekip, APOBEC‑benzeri mutasyonlarla dolu şaşırtıcı derecede çeşitli bir HHV-6A varyant karışımı tespit etti; bu, nakil ve ensefalit hastalarında görülen nispeten stabil HHV-6B dizileriyle tezat oluşturuyordu. Yazarlar, HHV-6A’nın zayıf U28 ifadesinin onu hücrenin DNA editörüne karşı savunmasız bıraktığını, böylece etkili şekilde çoğalmasını ve yayılmasını sınırladığını öne sürüyorlar.
Sağlık ve hastalık açısından ne anlama geliyor
Halk bakış açısından bakıldığında, HHV-6B önemli bir hücresel alarmı etkisiz hale etmeyi öğrenmiş; bu da onun DNA’sını temizce kopyalamasına ve bazen zararlı olabilen daha güçlü enfeksiyonlar kurmasına izin veriyor. HHV-6A ise bu savunmayı tam olarak susturamadığı için mutasyonlarla ağır biçimde yaralanıyor ve muhtemelen daha az çoğalıyor ve daha az belirgin hastalığa yol açıyor. Bu sonuçları U28 üretimini ne kadar güçlü kontrol ettiğini belirleyen tek bir viral anahtara bağlayarak çalışma, iki neredeyse özdeş virüsün neden bu kadar farklı klinik izler bırakabildiğine dair somut bir moleküler açıklama sunuyor. Ayrıca APOBEC3 enzimlerini viral evrimin potansiyel şekillendiricileri ve gelecekteki antiviral stratejiler için birer kaldıraç olarak vurguluyor; bu stratejiler ya hücrenin editörünü tehlikeli virüslere karşı güçlendirmeyi ya da bazı enfeksiyonların neden hafif kaldığını anlamayı hedefleyebilir.
Atıf: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Anahtar kelimeler: insan herpesvirüsü 6, APOBEC3, viral bağışıklıktan kaçış, virüs mutasyonu, U28 proteini