Clear Sky Science · it
Un antagonista virale di APOBEC3 distingue HHV-6A da HHV-6B
Perché alcuni virus comuni ci ammalano e altri restano silenziosi
La maggior parte degli adulti porta con sé diversi herpesvirus per tutta la vita, ma solo alcuni di questi ospiti causano mai malattie gravi. Questo studio pone una domanda semplice ma dalle implicazioni ampie: perché un membro della famiglia dell’herpesvirus umano 6 (HHV-6B) spesso provoca malattia nei neonati e nei pazienti trapiantati, mentre il suo quasi‑gemello (HHV-6A) di solito resta inosservato? Tracciando come questi virus si scontrano con un sistema di difesa del DNA presente nelle nostre cellule, gli autori scoprono una lotta molecolare che contribuisce a spiegare il loro comportamento clinico così diverso. 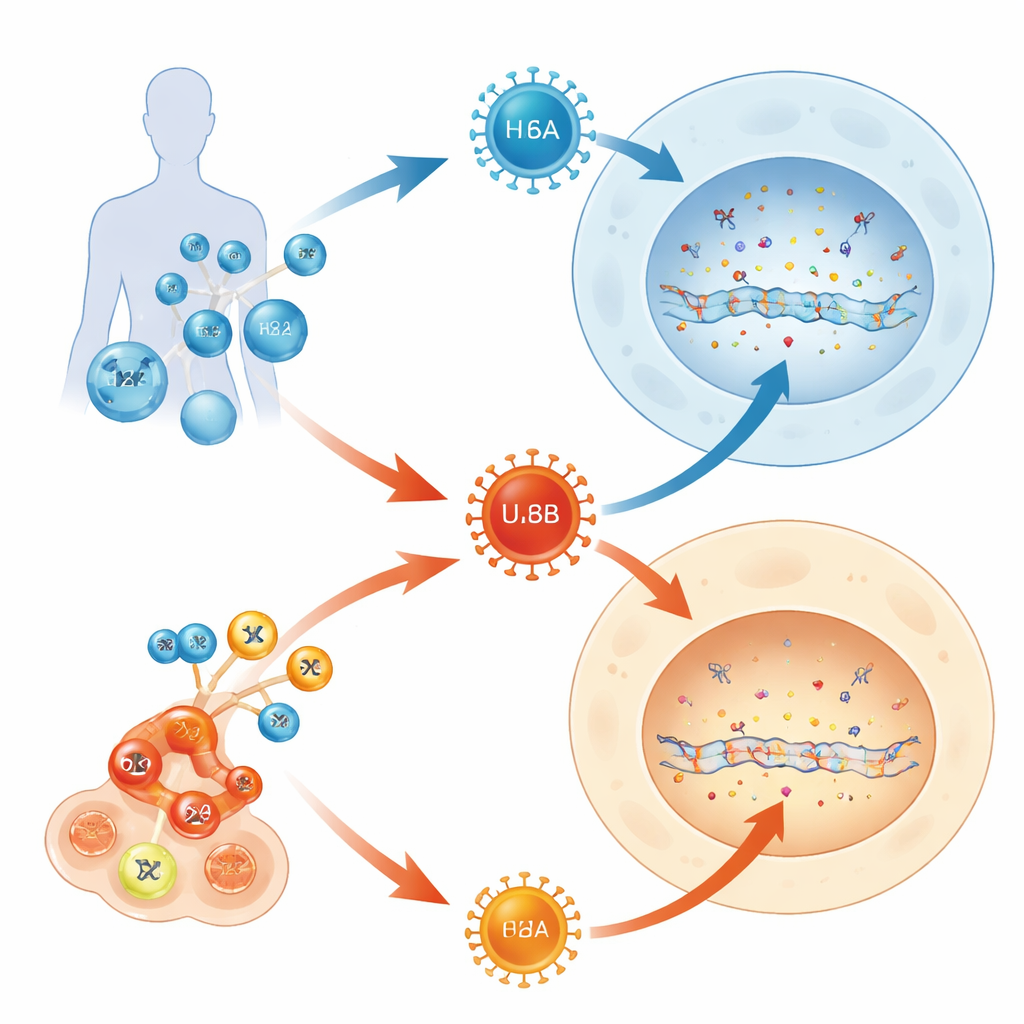
Il racconto di due virus strettamente correlati
HHV-6A e HHV-6B sono virus estremamente simili che prendono di mira gli stessi tipi di cellule immunitarie e condividono oltre il 90% dei loro geni. Eppure si comportano in modo diverso nelle persone. HHV-6B è la causa principale della roseola, un comune rash infantile che talvolta può portare a infiammazione cerebrale, specialmente in pazienti sottoposti a terapie avanzate su midollo osseo o cellule T. HHV-6A, al contrario, è di solito silente e raramente collegato a malattie evidenti. Poiché entrambi i virus utilizzano recettori noti per entrare nelle cellule, gli autori hanno ipotizzato che ciò che accade dopo l’ingresso — all’interno della macchina cellulare che gestisce il DNA — potesse essere la chiave per il loro diverso impatto.
L’editor del DNA integrato nella cellula interviene
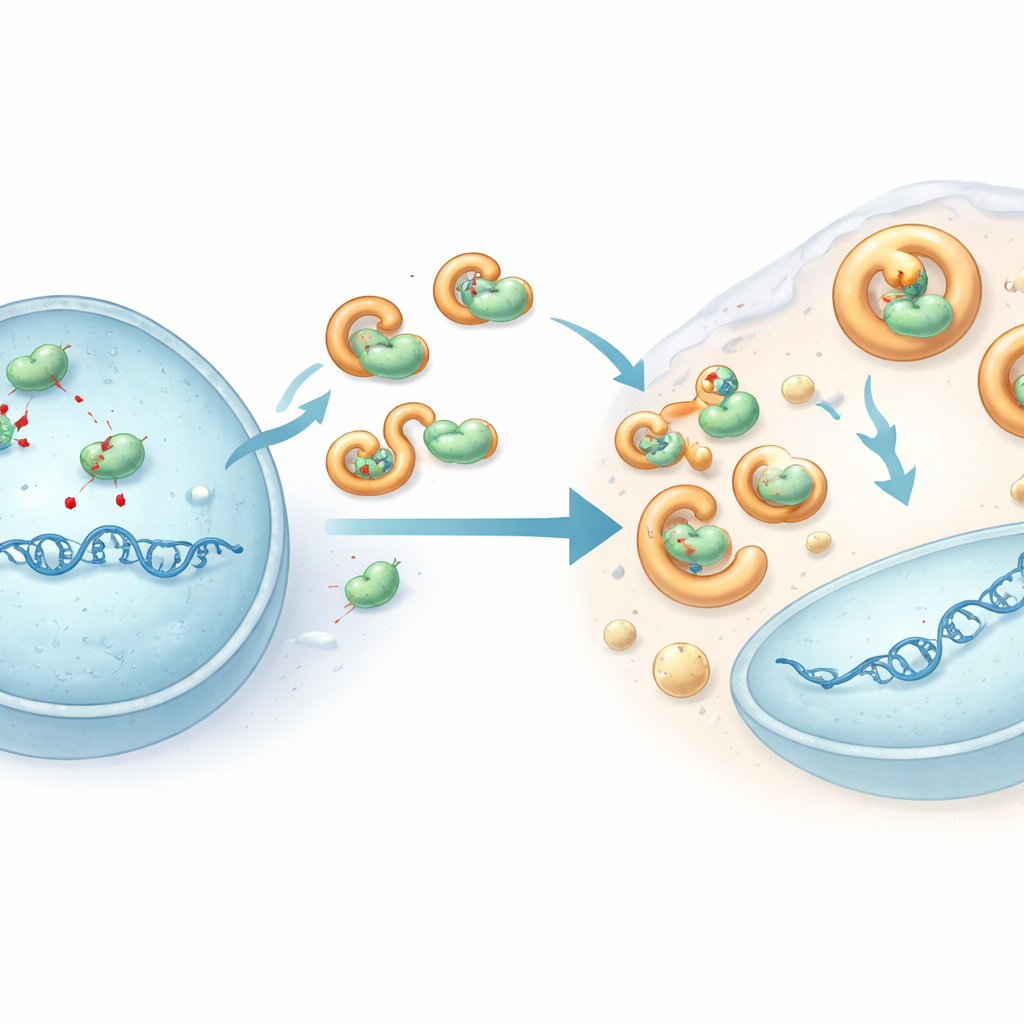
Le nostre cellule esprimono un gruppo di enzimi chiamati proteine APOBEC3 che pattugliano il DNA e possono compromettere i genomi virali convertendo chimicamente certe lettere del DNA, scatenando una tempesta di mutazioni. Confrontando l’attività genica in diverse linee di cellule T, il gruppo ha notato che vari geni APOBEC3 erano più attivi in cellule che permettevano la crescita di HHV-6B, ma non di HHV-6A. Quando hanno sequenziato un tratto ricco in GC del DNA virale proveniente da cellule infette, HHV-6A portava un pesante carico di mutazioni in stile APOBEC, mentre HHV-6B restava in gran parte intatto. Disattivare singoli geni APOBEC3, in particolare APOBEC3B e APOBEC3C, ha aumentato la replicazione di HHV-6A e ridotto nettamente il suo carico di mutazioni, dimostrando che questo sistema di difesa dell’ospite limita effettivamente HHV-6A. HHV-6B, tuttavia, sfuggiva in gran parte a questo editing del DNA nelle stesse cellule.
Uno scudo virale che disarma l’editor
Per capire come HHV-6B eluda questo attacco, i ricercatori si sono concentrati su una proteina virale chiamata U28, una versione modificata di un enzima che molti herpesvirus usano per la sintesi del DNA. Nelle cellule infettate da HHV-6B, APOBEC3B e APOBEC3C venivano spinti fuori dal nucleo (dove il DNA virale viene copiato) nel fluido circostante e i loro livelli complessivi diminuivano. Esperimenti in cellule ingegnerizzate hanno mostrato che la proteina U28 di HHV-6B si lega fisicamente a diverse proteine APOBEC3, le cattura in gocce a comportamento liquido connesse a vie di smaltimento cellulari e ne favorisce la degradazione. Questa sequestrazione mantiene gli enzimi lontani dal DNA virale e impedisce loro di infliggere danni diffusi. Quando U28 è stato ridotto nelle cellule infette, i livelli di APOBEC3 sono risaliti e i genomi di HHV-6B hanno accumulato più mutazioni, confermando che U28 agisce come un’armatura contro questo editing antivirale.
Piccole differenze nell’espressione, grandi differenze nell’esito
Curiosamente, la proteina U28 di HHV-6A è quasi identica nella sequenza a quella di HHV-6B e può anch’essa legare e ridurre le proteine APOBEC3 quando viene sovraespressa artificialmente. La distinzione cruciale è la quantità, non la qualità: durante l’infezione naturale, HHV-6B attiva U28 molto più fortemente rispetto a HHV-6A. Misurazioni in infezioni di laboratorio e in cellule del sangue primarie hanno mostrato livelli di RNA di U28 molto più alti in HHV-6B, insieme a una migliore conservazione del suo genoma. In un raro paziente con riattivazione di un genoma ereditato di HHV-6A, il gruppo ha rilevato uno sciame sorprendentemente diversificato di varianti HHV-6A cariche di mutazioni in stile APOBEC, in contrasto con le sequenze relativamente stabili di HHV-6B osservate in pazienti trapiantati e con encefalite. Gli autori propongono che la debole espressione di U28 in HHV-6A la renda vulnerabile all’editor del DNA della cellula, limitandone la capacità di replicare e diffondersi efficacemente.
Cosa significa per la salute e la malattia
Dal punto di vista divulgativo, HHV-6B ha imparato a disarmare un allarme cellulare chiave, consentendogli di copiare il proprio DNA in modo pulito e stabilire infezioni più forti e talvolta dannose. HHV-6A, che non riesce a silenziare completamente questa difesa, risulta fortemente segnato dalle mutazioni e può quindi replicare meno e causare meno malattie evidenti. Collegando questi esiti a un singolo interruttore virale che controlla quanto intensamente viene prodotto U28, lo studio offre una spiegazione molecolare concreta del perché due virus quasi identici possano avere impronte cliniche così diverse. Mettere in luce le proteine APOBEC3 sottolinea anche il loro ruolo potenziale nell’evoluzione virale e come possibili leve per strategie antivirali future: rafforzare l’editor cellulare contro virus pericolosi o capire perché alcune infezioni restano lievi.
Citazione: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Parole chiave: herpesvirus umano 6, APOBEC3, evasione immunitaria virale, mutazione virale, proteina U28