Clear Sky Science · ru
Вирусный антагонист APOBEC3 отличает HHV-6A от HHV-6B
Почему одни распространённые вирусы вызывают заболевания, а другие молчат
Большинство взрослых на всю жизнь носят в себе несколько герпесвирусов, но только некоторые из этих «попутчиков» когда‑то приводят к серьёзным болезням. В этом исследовании задан простой вопрос с далеко идущими последствиями: почему один член семейства человеческого герпесвируса 6 (HHV-6B) часто вызывает заболевание у младенцев и у реципиентов трансплантатов, в то время как его близкий двойник (HHV-6A) обычно остаётся незаметным? Отслеживая, как эти вирусы сталкиваются с встроенной в клетки системой защиты ДНК, авторы обнаруживают молекулярную борьбу, которая помогает объяснить их столь разное клиническое поведение. 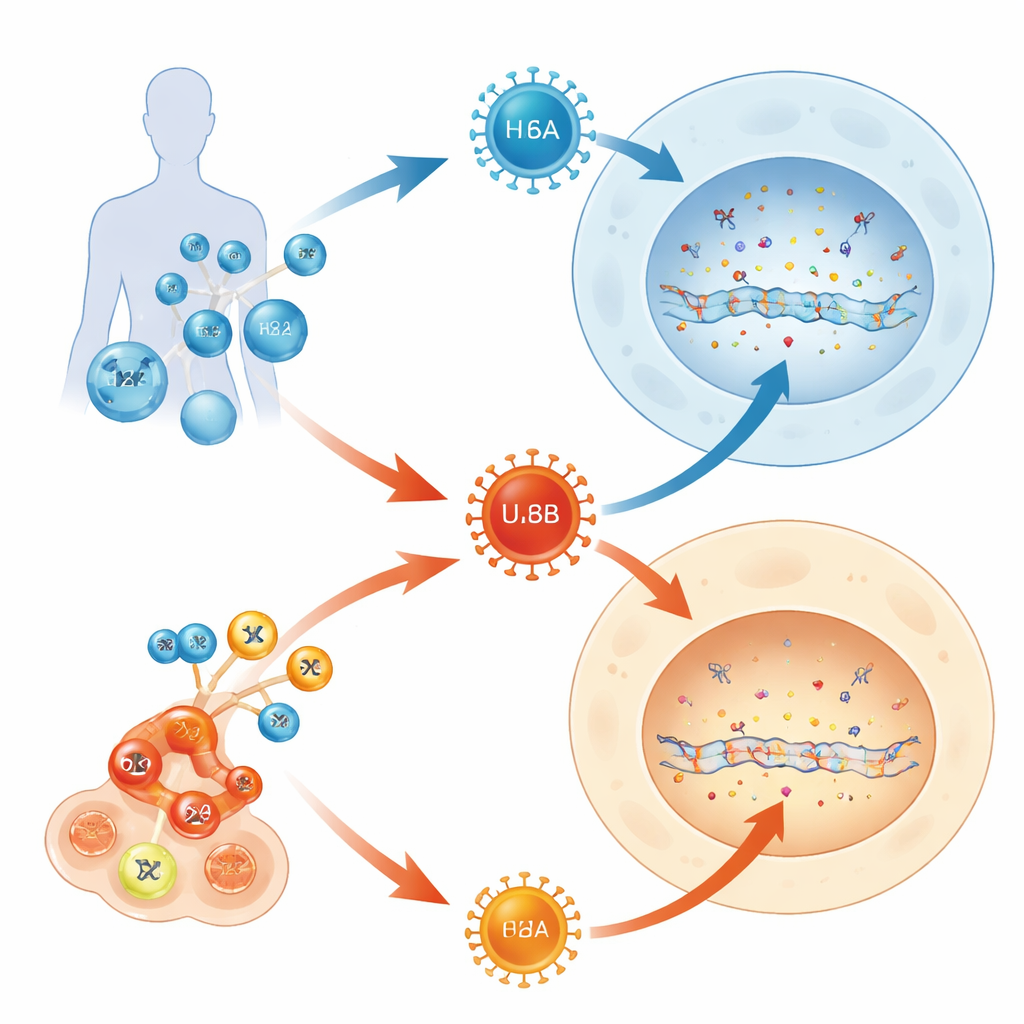
История двух тесно родственных вирусов
HHV-6A и HHV-6B — чрезвычайно похожие вирусы, которые поражают один и тот же тип иммунных клеток и делят более 90% генов. Тем не менее они ведут себя по‑разному в организме человека. HHV-6B является основной причиной розеолы, распространённой детской сыпи, которая иногда может приводить к воспалению мозга, особенно у пациентов, проходящих трансплантацию костного мозга или сложную Т‑клеточную терапию. HHV-6A, напротив, обычно молчит и редко ассоциируется с очевидными заболеваниями. Поскольку оба вируса используют известные рецепторы для проникновения в клетки, авторы предположили, что ключ к их различию может скрываться в процессах, происходящих уже после входа — внутри клеточного аппарата работы с ДНК.
Вмешивается встроенный редактор ДНК клетки
Наши клетки экспрессируют группу ферментов, называемых белками APOBEC3, которые патрулируют ДНК и способны портить вирусные геномы, химически превращая отдельные буквы ДНК и вызывая шквал мутаций. Сравнивая активность генов в разных линиях Т‑клеток, исследователи заметили, что несколько генов APOBEC3 были более активны в клетках, где хорошо размножался HHV-6A, а не HHV-6B. При секвенировании GC‑богатого участка вирусной ДНК из инфицированных клеток HHV-6A нес на себе тяжёлый груз APOBEC‑подобных мутаций, тогда как HHV-6B оставался в основном нетронутым. Отключение отдельных генов APOBEC3, особенно APOBEC3B и APOBEC3C, усиливало репликацию HHV-6A и резко снижало нагрузку мутаций, что показывает, что эта система защиты хозяина действительно ограничивает HHV-6A. HHV-6B же в тех же клетках в значительной степени избегал такого редактирования ДНК.
Вирусный щит, обезвреживающий редактор
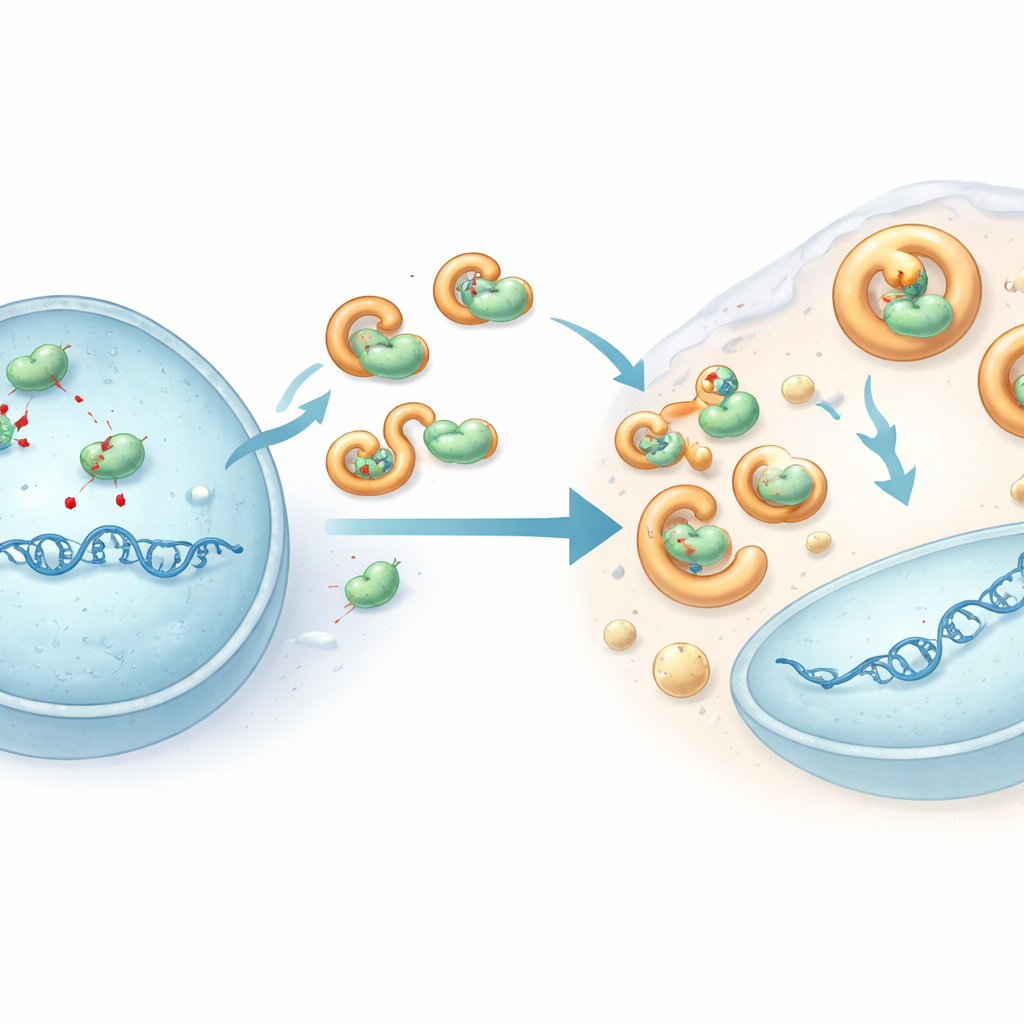
Чтобы понять, как HHV-6B ускользает от этой атаки, исследователи сосредоточились на одном вирусном белке под названием U28, модифицированной версии фермента, который многие герпесвирусы используют для работы с ДНК. В клетках, инфицированных HHV-6B, APOBEC3B и APOBEC3C выталкивались из ядра (где копируется вирусная ДНК) в цитоплазму, и их общий уровень снижался. Эксперименты на искусственно модифицированных клетках показали, что белок U28 от HHV-6B физически захватывает несколько белков APOBEC3, втягивает их в жидкоподобные капли, связанные с путями утилизации клеточных компонентов, и способствует их разрушению. Такая сепарация отбирает ферменты с пути вирусной ДНК и предотвращает нанесение ими широкомасштабного ущерба. Когда U28 снижали в инфицированных клетках, уровни APOBEC3 восставали, а геномы HHV-6B накапливали больше мутаций, что подтверждает роль U28 как «доспеха» против этого антивирусного редактирования.
Малые различия в экспрессии — большие различия в исходе
Любопытно, что белок U28 из HHV-6A по последовательности почти идентичен белку из HHV-6B и при искусственной сверхэкспрессии тоже может связывать и понижать уровни APOBEC3. Ключевое различие — в количестве, а не в качестве: при естественной инфекции HHV-6B включает экспрессию U28 значительно сильнее, чем HHV-6A. Измерения при лабораторных инфекциях и в первичных клетках крови показали намного более высокие уровни РНК U28 у HHV-6B, вместе с лучшей сохранностью его генома. У редкого пациента с реактивацией унаследованного генома HHV-6A команда обнаружила поразительно разнообразное множество вариантов HHV-6A, заполненное APOBEC‑подобными мутациями, в отличие от относительно стабильных последовательностей HHV-6B, наблюдавшихся у пациентов после трансплантации и при энцефалите. Авторы предположили, что слабая экспрессия U28 у HHV-6A делает его уязвимым для клеточного редактора ДНК, что ограничивает его способность эффективно размножаться и распространяться.
Что это значит для здоровья и болезней
Суперобобщённо, HHV-6B научился обезвреживать ключовую клеточную сигнализацию, что позволяет ему копировать свою ДНК чисто и устанавливать более устойчивые, иногда вредоносные инфекции. HHV-6A, которое не полностью подавляет эту защиту, оказывается серьёзно иссечённым мутациями и, возможно, из‑за этого реплицируется меньше и вызывает меньше явных заболеваний. Связывая эти различия с одним вирусным переключателем, контролирующим силу продукции U28, исследование даёт конкретное молекулярное объяснение тому, почему два почти идентичных вируса могут иметь столь разные клинические следы. Работа также подчёркивает роль ферментов APOBEC3 как потенциальных факторов, формирующих вирусную эволюцию, и как возможных точек воздействия для будущих антивирусных стратегий — либо чтобы усилить действие клеточного «редактора» против опасных вирусов, либо чтобы понять, почему некоторые инфекции остаются лёгкими.
Цитирование: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Ключевые слова: человеческий герпесвирус 6, APOBEC3, избегание иммунитета вирусом, мутации вируса, белок U28