Clear Sky Science · pt
Um antagonista viral do APOBEC3 distingue HHV-6A de HHV-6B
Por que alguns vírus comuns nos adoecem e outros permanecem silenciosos
A maioria dos adultos carrega vários herpesvírus pela vida, mas apenas alguns desses passageiros ocasionam doenças graves. Este estudo faz uma pergunta simples com implicações amplas: por que um membro da família do herpesvírus humano 6 (HHV-6B) frequentemente deixa bebês e receptores de transplante doentes, enquanto seu quase gêmeo (HHV-6A) geralmente passa despercebido? Ao seguir como esses vírus confrontam um sistema de defesa de DNA embutido em nossas células, os autores revelam uma disputa molecular que ajuda a explicar seus comportamentos clínicos tão distintos. 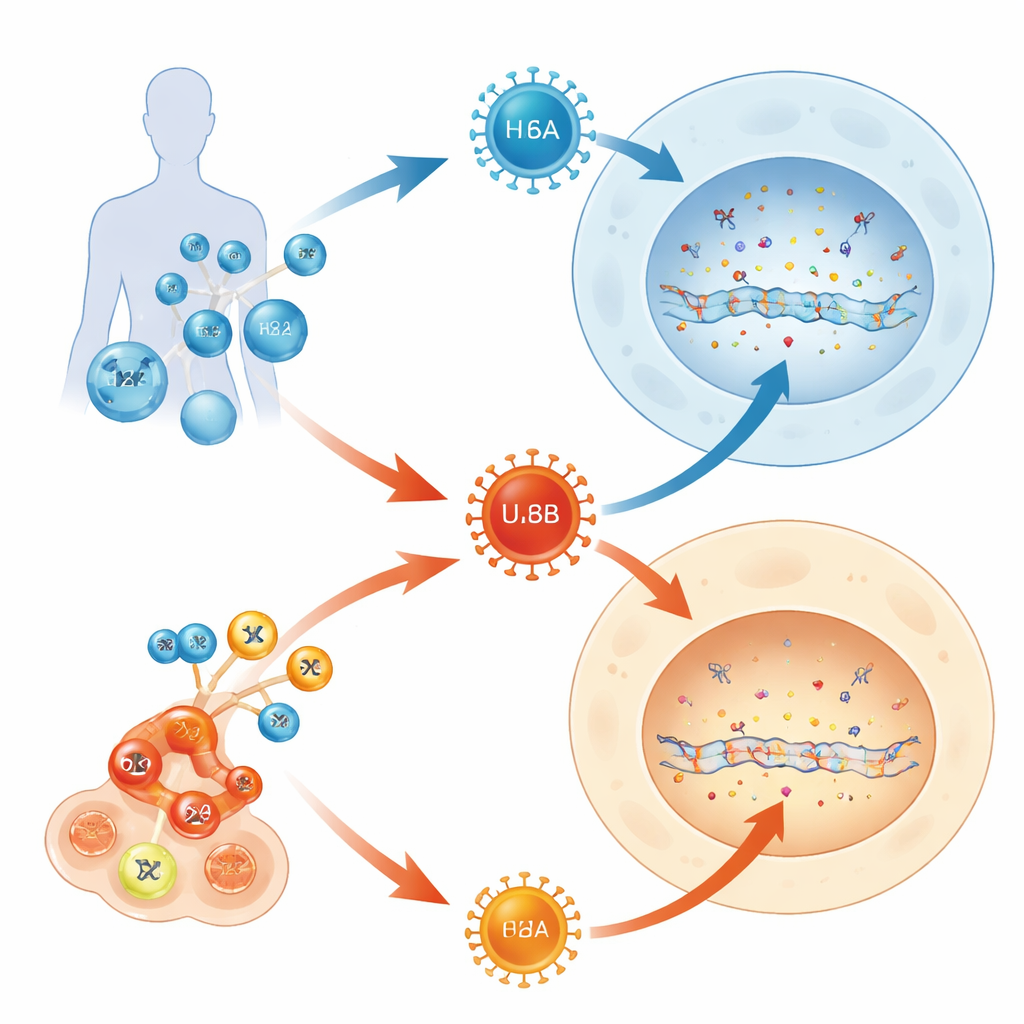
O conto de dois vírus intimamente relacionados
HHV-6A e HHV-6B são vírus extremamente semelhantes que atacam os mesmos tipos de células imunes e compartilham mais de 90% dos seus genes. Ainda assim, comportam-se de forma diferente nas pessoas. O HHV-6B é a principal causa da roséola, uma erupção infantil comum que às vezes pode levar à inflamação cerebral, especialmente em pacientes submetidos a transplante de medula óssea ou terapias avançadas com células T. Em contraste, o HHV-6A costuma permanecer silencioso e raramente é associado a doenças claras. Como ambos os vírus usam receptores conhecidos para entrar nas células, os autores suspeitaram que o que acontece após a entrada — dentro da própria maquinaria de manipulação de DNA da célula — poderia ser a chave para seu impacto diferente.
O editor de DNA embutido da célula entra em ação
Nossas células expressam um grupo de enzimas chamadas proteínas APOBEC3 que patrulham o DNA e podem sabotar genomas virais ao converter quimicamente certas letras do DNA, desencadeando uma tempestade de mutações. Ao comparar a atividade gênica em diferentes linhagens de células T, a equipe notou que vários genes APOBEC3 estavam mais ativos em células que permitem o crescimento do HHV-6B, mas não do HHV-6A. Quando sequenciaram um trecho rico em GC do DNA viral de células infectadas, o HHV-6A carregava um pesado fardo de mutações no estilo APOBEC, enquanto o HHV-6B permanecia em grande parte intacto. Desligar genes APOBEC3 individuais, especialmente APOBEC3B e APOBEC3C, aumentou a replicação do HHV-6A e reduziu drasticamente sua carga de mutação, mostrando que esse sistema de defesa do hospedeiro restringe genuinamente o HHV-6A. O HHV-6B, no entanto, em grande parte escapou dessa edição do DNA nas mesmas células.
Um escudo viral que desarma o editor
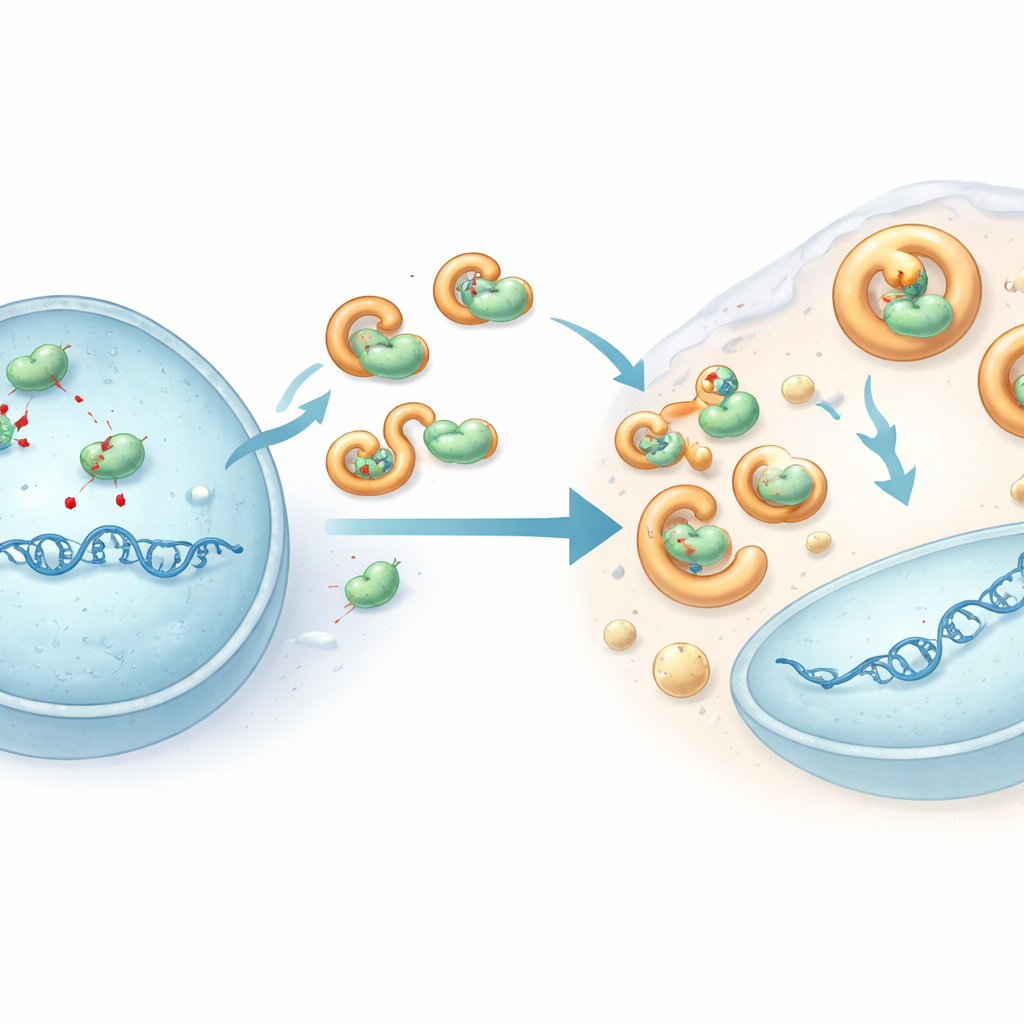
Para entender como o HHV-6B evita esse ataque, os pesquisadores focaram em uma proteína viral chamada U28, uma versão modificada de uma enzima que muitos herpesvírus usam para construção de DNA. Em células infectadas por HHV-6B, APOBEC3B e APOBEC3C eram forçadas a sair do núcleo (onde o DNA viral é copiado) para o fluido circundante e seus níveis totais caíam. Experimentos em células geneticamente modificadas mostraram que a proteína U28 do HHV-6B se liga fisicamente a várias proteínas APOBEC3, puxa‑as para gotículas com aspecto líquido ligadas a vias celulares de descarte e promove sua degradação. Essa sequestro mantém as enzimas longe do DNA viral e impede que inflijam danos generalizados. Quando U28 foi reduzida em células infectadas, os níveis de APOBEC3 recuperaram-se e os genomas do HHV-6B acumularam mais mutações, confirmando que U28 atua como uma armadura contra essa edição antiviral.
Pequenas diferenças na expressão, grandes diferenças no resultado
Curiosamente, a proteína U28 do HHV-6A é quase idêntica em sequência à do HHV-6B e também pode se ligar e reduzir proteínas APOBEC3 quando superproduzida artificialmente. A distinção crucial é quantidade, não qualidade: durante a infecção natural, o HHV-6B ativa U28 muito mais fortemente do que o HHV-6A. Medidas em infecções de laboratório e em células sanguíneas primárias mostraram níveis de RNA de U28 muito mais altos no HHV-6B, junto com melhor preservação de seu genoma. Em um paciente raro com reativação de um genoma HHV-6A herdado, a equipe detectou um enxame notavelmente diverso de variantes de HHV-6A repleto de mutações do tipo APOBEC, em contraste com as sequências relativamente estáveis do HHV-6B observadas em pacientes de transplante e encefalite. Os autores propõem que a fraca expressão de U28 do HHV-6A o deixa vulnerável ao editor de DNA da célula, limitando sua capacidade de replicar e se espalhar eficientemente.
O que isso significa para saúde e doença
Visto de forma acessível, o HHV-6B aprendeu a desarmar um alarme celular chave, permitindo copiar seu DNA de forma limpa e estabelecer infecções mais fortes e, às vezes, prejudiciais. O HHV-6A, que não consegue silenciar totalmente essa defesa, fica fortemente marcado por mutações e pode, por isso, replicar menos e causar menos doenças evidentes. Ao ligar esses resultados a um único interruptor viral que controla quão fortemente U28 é produzido, o estudo oferece uma explicação molecular concreta para por que dois vírus quase idênticos podem ter pegadas clínicas tão diferentes. Também destaca as enzimas APOBEC3 como potenciais formadoras da evolução viral e como possíveis alavancas para estratégias antivirais futuras que visem reforçar o editor celular contra vírus perigosos ou entender por que algumas infecções permanecem suaves.
Citação: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Palavras-chave: herpesvírus humano 6, APOBEC3, evasão imune viral, mutação viral, proteína U28