Clear Sky Science · de
Ein viraler APOBEC3-Gegenspieler unterscheidet HHV-6A von HHV-6B
Warum manche weit verbreitete Viren uns krank machen und andere stumm bleiben
Die meisten Erwachsenen tragen ein Leben lang mehrere Herpesviren in sich, doch nur einige dieser Dauerbewohner verursachen jemals schwere Erkrankungen. Diese Studie stellt eine einfache Frage mit weitreichenden Folgen: Warum macht ein Mitglied der Humanherpesvirus‑6‑Familie (HHV‑6B) häufig Säuglinge und Transplantatpatienten krank, während sein naher Verwandter (HHV‑6A) meist unbemerkt bleibt? Indem die Autoren nachzeichnen, wie diese Viren mit einem eingebauten DNA‑Abwehrsystem in unseren Zellen kollidieren, offenbaren sie ein molekulares Tauziehen, das dazu beiträgt, ihr sehr unterschiedliches klinisches Verhalten zu erklären. 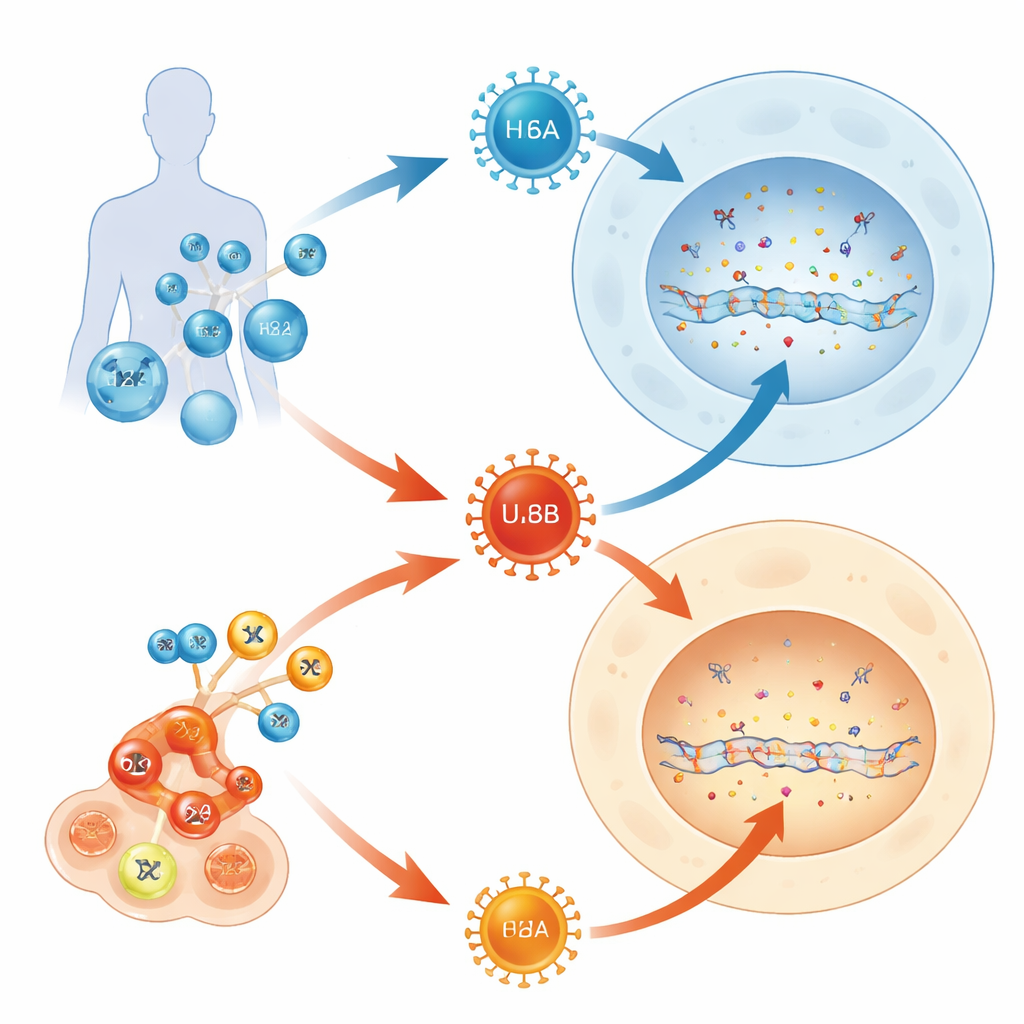
Die Geschichte von zwei eng verwandten Viren
HHV‑6A und HHV‑6B sind extrem ähnliche Viren, die dieselben Arten von Immunzellen angreifen und mehr als 90 % ihrer Gene teilen. Dennoch verhalten sie sich beim Menschen unterschiedlich. HHV‑6B ist die Hauptursache von Roseloa, einem häufigen Kinderausschlag, der gelegentlich zu Hirnentzündungen führen kann, besonders bei Patienten nach Knochenmarkstransplantation oder fortgeschrittenen T‑Zell‑Therapien. HHV‑6A dagegen ist in der Regel still und selten eindeutig mit Erkrankungen verknüpft. Da beide Viren bekannte Rezeptoren zur Zellaufnahme nutzen, vermuteten die Autoren, dass das, was nach dem Eintritt geschieht — also in der DNA‑Verwaltung der Zelle — der Schlüssel zu ihrem unterschiedlichen Einfluss sein könnte.
Der eingebaute DNA‑Editor der Zelle greift ein
Unsere Zellen produzieren eine Gruppe von Enzymen, die APOBEC3‑Proteine genannt werden; sie patrouillieren die DNA und können virale Genome sabotieren, indem sie bestimmte DNA‑Bausteine chemisch verändern und so eine Flut von Mutationen auslösen. Beim Vergleich der Genaktivität in unterschiedlichen T‑Zell‑Linien fiel dem Team auf, dass mehrere APOBEC3‑Gene in Zellen aktiver waren, die HHV‑6B, aber nicht HHV‑6A, Wachstum erlaubten. Als sie eine GC‑reiche DNA‑Region des Virus aus infizierten Zellen sequenzierten, trug HHV‑6A eine hohe Last an APOBEC‑typischen Mutationen, während HHV‑6B weitgehend unverändert blieb. Das Ausschalten einzelner APOBEC3‑Gene, insbesondere APOBEC3B und APOBEC3C, steigerte die Replikation von HHV‑6A und verringerte deutlich dessen Mutationslast, was zeigt, dass dieses Wirtsabwehrsystem HHV‑6A tatsächlich einschränkt. HHV‑6B entkam dieser DNA‑Bearbeitung in denselben Zellen jedoch größtenteils.
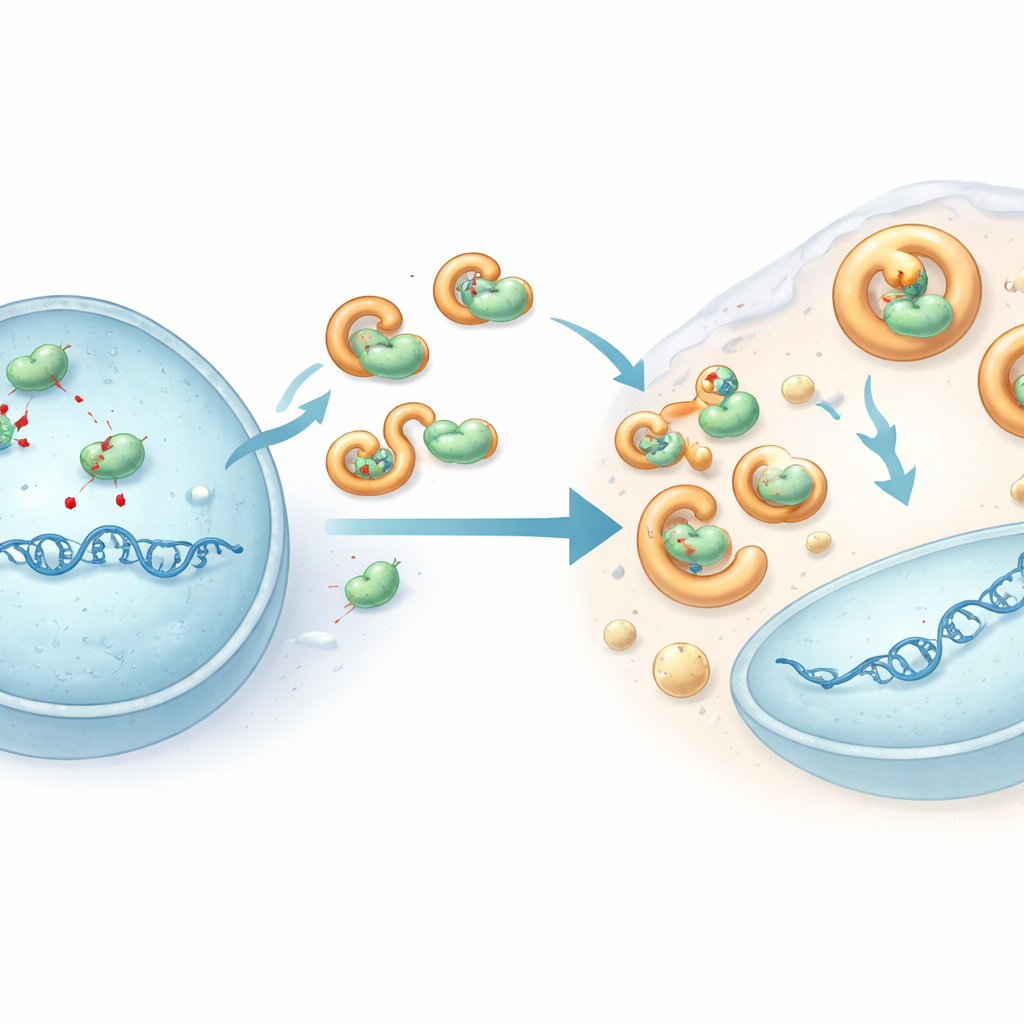
Ein viraler Schild, der den Editor entwaffnet
Um zu verstehen, wie HHV‑6B diesem Angriff entgeht, konzentrierten sich die Forschenden auf ein virales Protein namens U28, eine modifizierte Version eines Enzyms, das viele Herpesviren beim DNA‑Aufbau nutzen. In HHV‑6B‑infizierten Zellen wurden APOBEC3B und APOBEC3C aus dem Zellkern (wo virale DNA kopiert wird) ins umgebende Zytoplasma verdrängt, und ihre Gesamtmengen sanken. Experimente in gentechnisch veränderten Zellen zeigten, dass das U28‑Protein von HHV‑6B physisch an mehrere APOBEC3‑Proteine bindet, sie in flüssigkeitsähnliche Tröpfchen zieht, die mit zellulären Abbauwegen verbunden sind, und ihren Abbau fördert. Diese Absonderung hält die Enzyme von viraler DNA fern und verhindert, dass sie weitreichende Schäden anrichten. Wurde U28 in infizierten Zellen verringert, stiegen die APOBEC3‑Spiegel wieder an und HHV‑6B‑Genome häuften mehr Mutationen an — ein Beleg dafür, dass U28 als Schutzpanzer gegen diese antivirale Bearbeitung wirkt.
Kleine Unterschiede in der Expression, große Unterschiede im Ergebnis
Erstaunlicherweise ist das U28‑Protein von HHV‑6A in der Sequenz fast identisch mit dem von HHV‑6B und kann bei künstlich hoher Überproduktion ebenfalls an APOBEC3‑Proteine binden und deren Menge senken. Der entscheidende Unterschied liegt in der Menge, nicht in der Qualität: Während der natürlichen Infektion schaltet HHV‑6B U28 viel stärker ein als HHV‑6A. Messungen in Laborinfektionen und in primären Blutzellen zeigten deutlich höhere U28‑RNA‑Spiegel bei HHV‑6B sowie eine bessere Erhaltung seines Genoms. Bei einem seltenen Patienten mit Reaktivierung eines vererbten HHV‑6A‑Genoms entdeckte das Team eine auffallend vielfältige Population von HHV‑6A‑Varianten, die reich an APOBEC‑ähnlichen Mutationen war — im Gegensatz zu den relativ stabilen HHV‑6B‑Sequenzen, die bei Transplantations‑ und Enzephalitispatienten beobachtet wurden. Die Autoren schlagen vor, dass die schwache U28‑Expression von HHV‑6A es gegenüber dem zellulären DNA‑Editor verwundbar macht und dadurch seine Fähigkeit zur effizienten Replikation und Verbreitung einschränkt.
Was das für Gesundheit und Krankheit bedeutet
Laienhaft betrachtet hat HHV‑6B gelernt, einen wichtigen zellulären Alarm zu entwaffnen, wodurch es seine DNA sauber replizieren und stärkere, mitunter schädliche Infektionen etablieren kann. HHV‑6A, das diese Abwehr nicht vollständig stummschalten kann, wird stark durch Mutationen gezeichnet und repliziert möglicherweise somit weniger und verursacht seltener offensichtliche Erkrankungen. Indem die Studie diese Ergebnisse mit einem einzigen viralen Schalter verbindet, der steuert, wie stark U28 produziert wird, liefert sie eine konkrete molekulare Erklärung dafür, warum zwei nahezu identische Viren so unterschiedliche klinische Spuren hinterlassen können. Zugleich rückt sie APOBEC3‑Enzyme als mögliche Treiber der viralen Evolution und als potenzielle Ansatzpunkte für künftige antivirale Strategien in den Fokus — entweder, um den zellulären Editor gegen gefährliche Viren zu stärken oder um zu verstehen, warum manche Infektionen mild bleiben.
Zitation: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Schlüsselwörter: humanes Herpesvirus 6, APOBEC3, virale Immunflucht, Virusmutation, U28-Protein