Clear Sky Science · es
Un antagonista viral de APOBEC3 distingue HHV-6A de HHV-6B
Por qué algunos virus comunes nos enferman y otros se mantienen silenciosos
La mayoría de los adultos albergan varios herpesvirus de por vida, pero solo algunos de estos ocupantes causan enfermedades graves. Este estudio plantea una pregunta sencilla con implicaciones profundas: ¿por qué un miembro de la familia del herpesvirus humano 6 (HHV-6B) suele enfermar a lactantes y a pacientes trasplantados, mientras su casi gemelo (HHV-6A) normalmente permanece desapercibido? Al seguir cómo estos virus chocan con un sistema de defensa del ADN incorporado en nuestras células, los autores descubren una lucha molecular que ayuda a explicar su comportamiento clínico tan distinto. 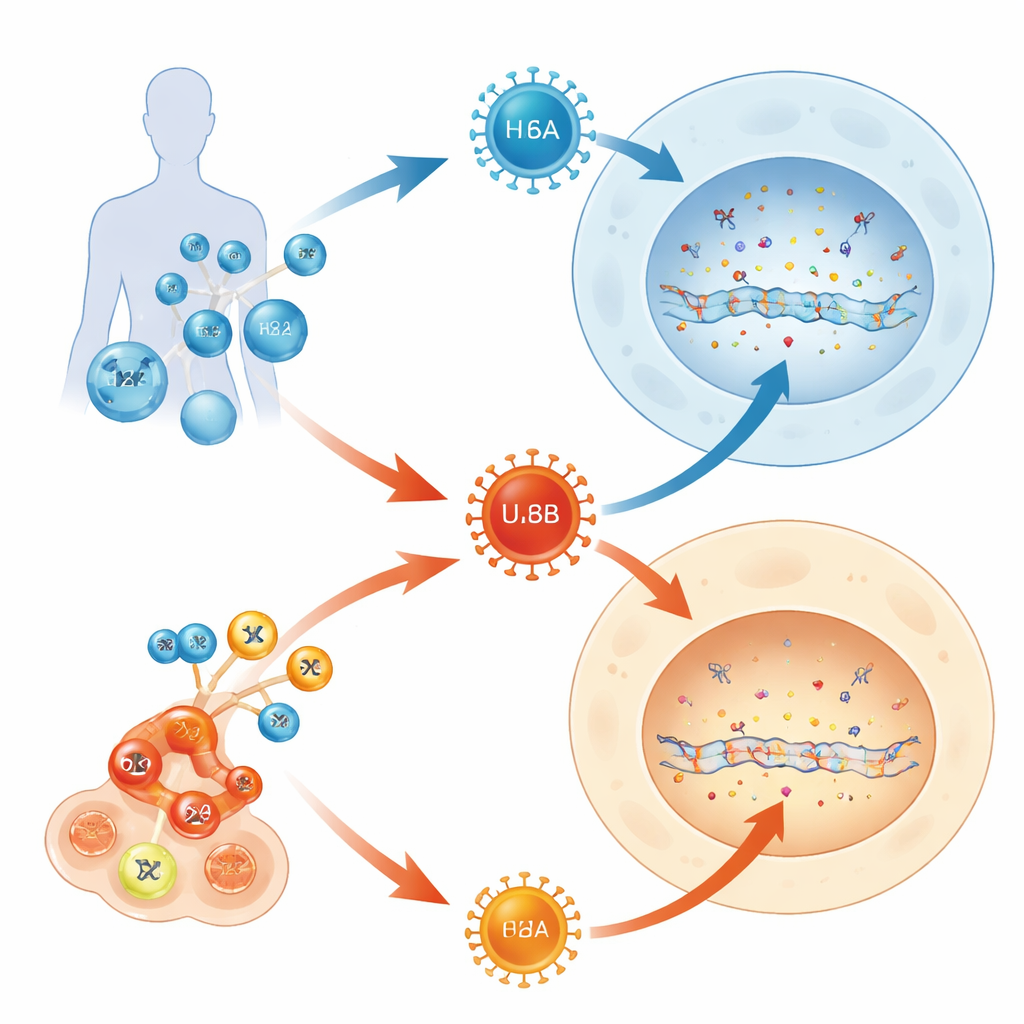
La historia de dos virus estrechamente relacionados
HHV-6A y HHV-6B son virus extremadamente similares que atacan a los mismos tipos de células inmunitarias y comparten más del 90 % de sus genes. Aun así, se comportan de forma diferente en las personas. HHV-6B es la principal causa de la roséola, una erupción infantil común que a veces puede derivar en inflamación cerebral, especialmente en pacientes sometidos a terapias avanzadas con médula ósea o células T. HHV-6A, en cambio, suele ser silencioso y rara vez se asocia a una enfermedad clara. Dado que ambos virus usan receptores conocidos para entrar en las células, los autores sospecharon que lo que ocurre tras la entrada —dentro de la propia maquinaria de manejo del ADN de la célula— podría ser la clave de su distinto impacto.
Entra el editor de ADN incorporado de la célula
Nuestras células expresan un grupo de enzimas llamadas proteínas APOBEC3 que vigilan el ADN y pueden sabotear los genomas virales al convertir químicamente ciertas letras del ADN, desencadenando una avalancha de mutaciones. Al comparar la actividad génica en distintas líneas celulares T, el equipo observó que varios genes APOBEC3 estaban más activos en células que permitían el crecimiento de HHV-6B, pero no de HHV-6A. Cuando secuenciaron un tramo rico en GC del ADN viral de células infectadas, HHV-6A mostraba una gran carga de mutaciones del tipo APOBEC, mientras que HHV-6B permanecía mayormente intacto. Apagar genes APOBEC3 individuales, especialmente APOBEC3B y APOBEC3C, aumentó la replicación de HHV-6A y redujo drásticamente su carga de mutaciones, demostrando que este sistema de defensa del huésped restringe genuinamente a HHV-6A. HHV-6B, sin embargo, en gran medida eludió esta edición del ADN en las mismas células.
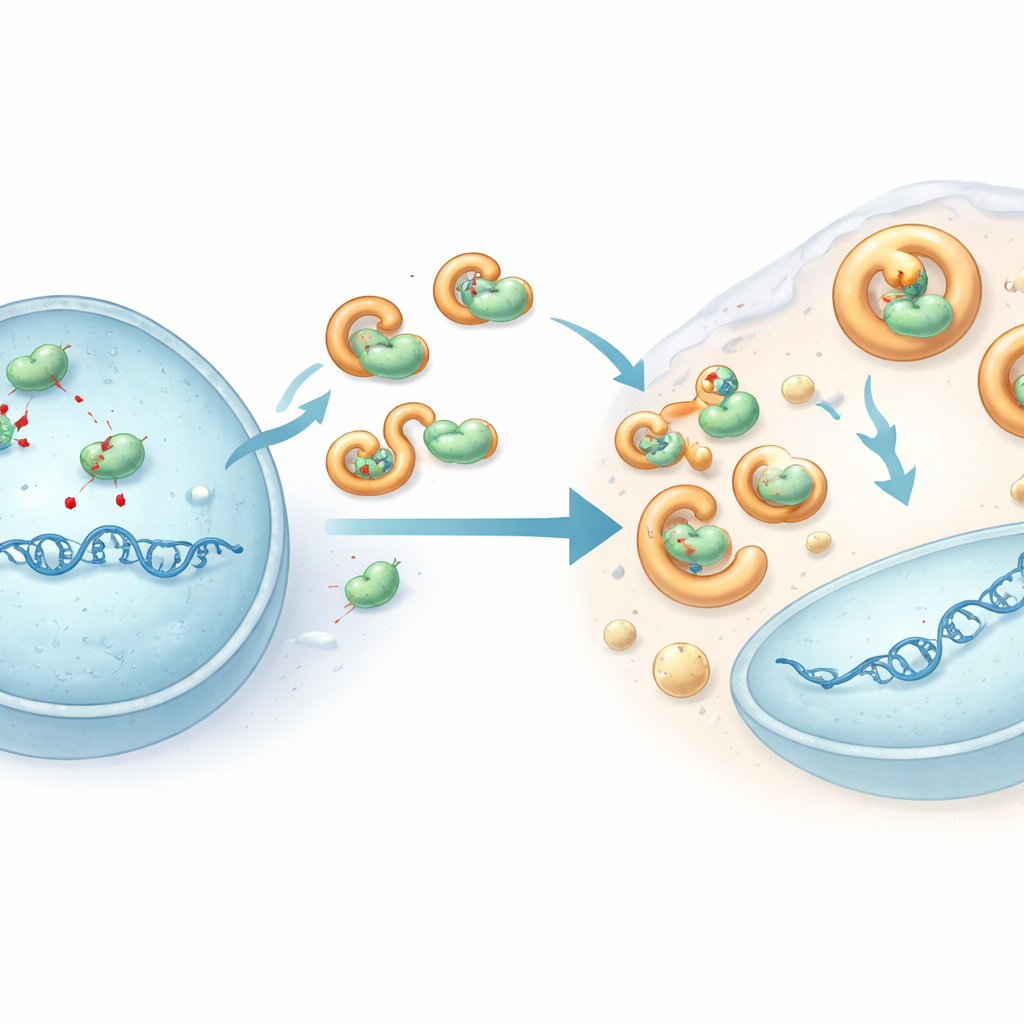
Un escudo viral que desactiva al editor
Para entender cómo HHV-6B evade este ataque, los investigadores se centraron en una proteína viral llamada U28, una versión modificada de una enzima que muchos herpesvirus usan para sintetizar ADN. En células infectadas por HHV-6B, APOBEC3B y APOBEC3C fueron expulsadas del núcleo (donde se copia el ADN viral) al fluido circundante y sus niveles totales disminuyeron. Experimentos en células diseñadas mostraron que la proteína U28 de HHV-6B se une físicamente a varias proteínas APOBEC3, las arrastra hacia gotículas de tipo líquido conectadas a vías de eliminación celular y promueve su degradación. Esta reclusión mantiene a las enzimas alejadas del ADN viral e impide que inflijan daños generalizados. Cuando se redujo U28 en células infectadas, los niveles de APOBEC3 se recuperaron y los genomas de HHV-6B acumularon más mutaciones, confirmando que U28 actúa como una armadura contra esta edición antiviral.
Pequeñas diferencias en la expresión, grandes diferencias en el resultado
Curiosamente, la proteína U28 de HHV-6A es casi idéntica en secuencia a la de HHV-6B y también puede unirse y reducir las proteínas APOBEC3 cuando se sobreexpresa artificialmente. La distinción crucial es la cantidad, no la calidad: durante la infección natural, HHV-6B activa U28 con mucha más intensidad que HHV-6A. Medidas en infecciones de laboratorio y en células sanguíneas primarias mostraron niveles de ARN de U28 mucho más altos en HHV-6B, junto con una mejor preservación de su genoma. En un caso raro de un paciente con reactivación de un genoma heredado de HHV-6A, el equipo detectó una sorprendente diversidad de variantes de HHV-6A llenas de mutaciones tipo APOBEC, en contraste con las secuencias relativamente estables de HHV-6B observadas en pacientes trasplantados y con encefalitis. Los autores proponen que la débil expresión de U28 en HHV-6A lo deja vulnerable al editor de ADN de la célula, limitando su capacidad para replicarse y propagarse eficazmente.
Qué significa esto para la salud y la enfermedad
Desde una perspectiva divulgativa, HHV-6B ha aprendido a desactivar una alarma celular clave, lo que le permite copiar su ADN de forma limpia y establecer infecciones más fuertes y, a veces, perjudiciales. HHV-6A, que no logra silenciar por completo esta defensa, queda fuertemente marcada por mutaciones y por tanto puede replicarse menos y causar menos enfermedades evidentes. Al vincular estos resultados a un único interruptor viral que controla la intensidad de producción de U28, el estudio ofrece una explicación molecular concreta de por qué dos virus casi idénticos pueden tener huellas clínicas tan diferentes. También destaca a las enzimas APOBEC3 como posibles moldeadoras de la evolución viral y como palancas potenciales para futuras estrategias antivirales destinadas a reforzar el editor de la célula frente a virus peligrosos o a comprender por qué algunas infecciones permanecen leves.
Cita: Arii, J., Aktar, S., Huang, J.R. et al. A viral APOBEC3 antagonist distinguishes HHV-6A from HHV-6B. Nat Commun 17, 3566 (2026). https://doi.org/10.1038/s41467-026-71951-6
Palabras clave: herpesvirus humano 6, APOBEC3, evasión inmunitaria viral, mutación viral, proteína U28