Clear Sky Science · zh
环状 RNA 的历史与功能
微小 RNA 环如何帮助受压大脑应对挑战
当我们睡眠不足、受伤或情绪过载时,脑细胞必须迅速调整其活动以求存活并维持电路功能。本文描述了大脑中一种不同寻常的分子——一种称为 Cdr1as 的环状 RNA,并说明它如何与其他小型 RNA 协同作用,在应激条件下微调神经细胞的通讯。理解这一隐秘的控制系统可能为中风、抑郁等脑部疾病的治疗开辟新途径——甚至有可能产生从血样远程反映大脑健康状况的检测方法。
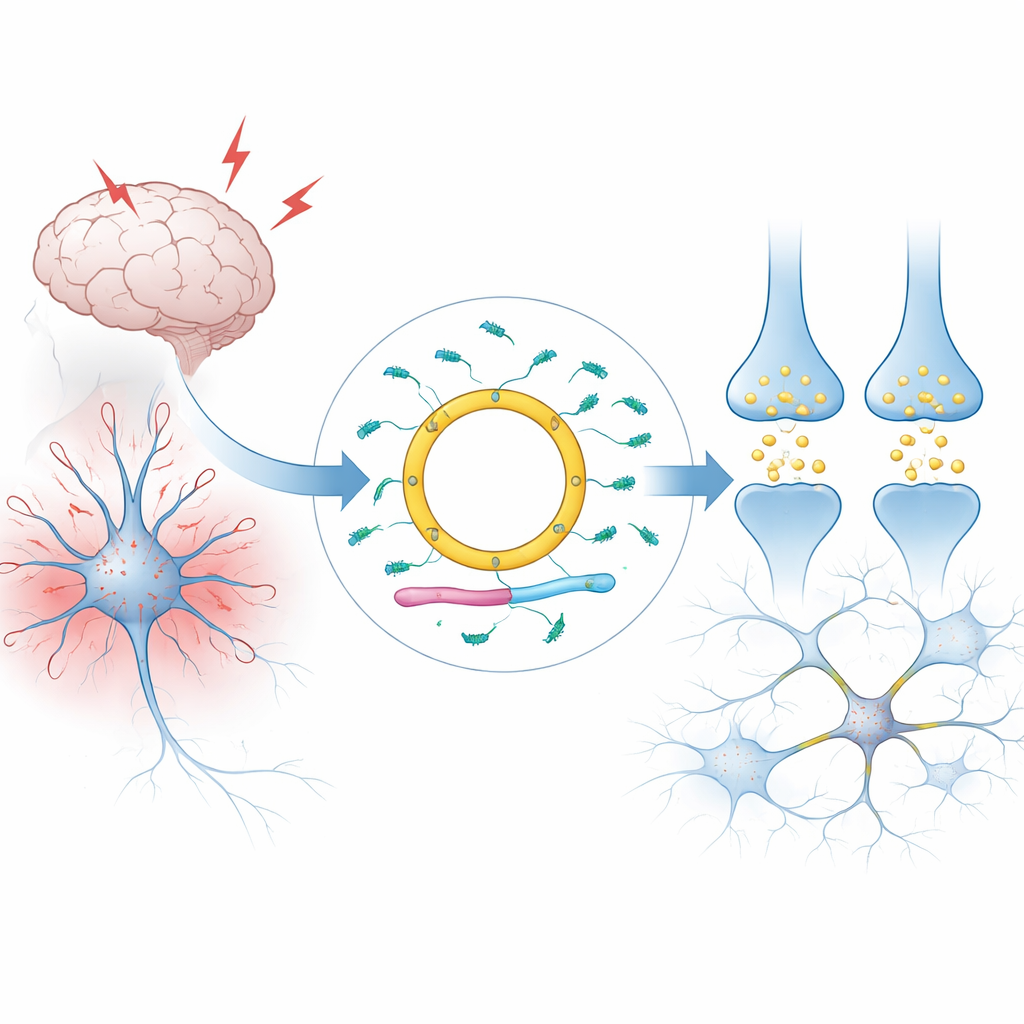
大脑细胞里的环形讯息
我们细胞中的大多数 RNA 是线性的:它们有两端且会很快被降解。Cdr1as 则不同。它形成闭合环,使其异常稳定,能够在哺乳动物的大脑中累积到很高的水平,尤其是在特定类型的神经元中。作者解释了 Cdr1as 如何从 X 染色体上的一个较大 RNA 单位产生,通过将其末端拼接在一起来形成环。在人类和小鼠中,来自该位点的几乎所有 RNA 都被转化为环状形式,几乎没有残留的线性版本。对组织和单细胞的大规模调查显示,Cdr1as 在实际意义上是一个神经元特异性的分子,在其他器官和支持性脑细胞(如胶质细胞)中稀少。
密集的微型调控网络
Cdr1as 的重要性来自于它所携带的“伙伴”。它的环状序列含有极为丰富的对接位点,可供一种名为 miR-7 的小型调控 RNA 结合——在人类约有七十个,在小鼠约有一百三十个。miR-7 属于备受关注的 microRNA 家族,这类分子最近获得诺贝尔认可,能够同时沉默许多编码蛋白的信使 RNA。在神经元中,miR-7 靶向参与应激反应和化学递质谷氨酸释放的信使。Cdr1as 在活体脑组织中结合 miR-7,影响 miR-7 的稳定性、其在神经元内的位置以及它对众多靶标的作用强度。第二种小 RNA miR-671 能切割并摧毁 Cdr1as,而一种名为 Cyrano 的长 RNA 则促使 miR-7 本身被主动降解。三种非编码 RNA 与两种 microRNA 共同构成了一个紧密相连的回路。
在压力下维持神经活动平衡
作者总结了利用缺失回路中单个组成部分的小鼠模型进行的十年研究,展示了该回路如何塑造大脑功能。去除 Cdr1as 会降低成熟 miR-7 水平并扰乱通常响应活动和应激的“即时早期”基因表达。缺失 Cdr1as 的神经元放电更为不稳定、过度兴奋,小鼠对感知刺激的反应也发生改变。相比之下,去除 Cyrano 会导致 miR-7 大量积累,反过来阻止 Cdr1as 的积累,揭示出一个反馈回路。在神经元培养皿和活体小鼠中模拟类似中风的条件的实验表明,Cdr1as、miR-7 和 Cyrano 的水平以协调的、随时间变化的方式移动。这些变化改变了突触处的谷氨酸释放,影响神经元的存活能力以及损伤后网络的恢复情况。
作为精细调控的进化附加组件
该综述还将这一回路置于进化背景中讨论。miR-7 起源古老,随首批发展出集中神经系统的动物出现,并因其在控制早期发育决策(如由主调控因子 PAX6 指导的过程)中发挥作用而高度保守。相比之下,Cyrano 在脊椎动物中出现得更晚,miR-671 在拥有原始胎盘的哺乳动物中更晚出现,而 Cdr1as 仅出现在胎盘哺乳动物中。作者认为,这些较新的 RNA 是逐步叠加到较古老的 miR-7 系统上,从而改进了在专门化的脑细胞和分泌激素的细胞中对分泌与应激反应的调节。他们提出 Cdr1as 可能充当一种运输者,将 miR-7 携带到神经末端,那里局部蛋白质合成和递质释放受到控制。
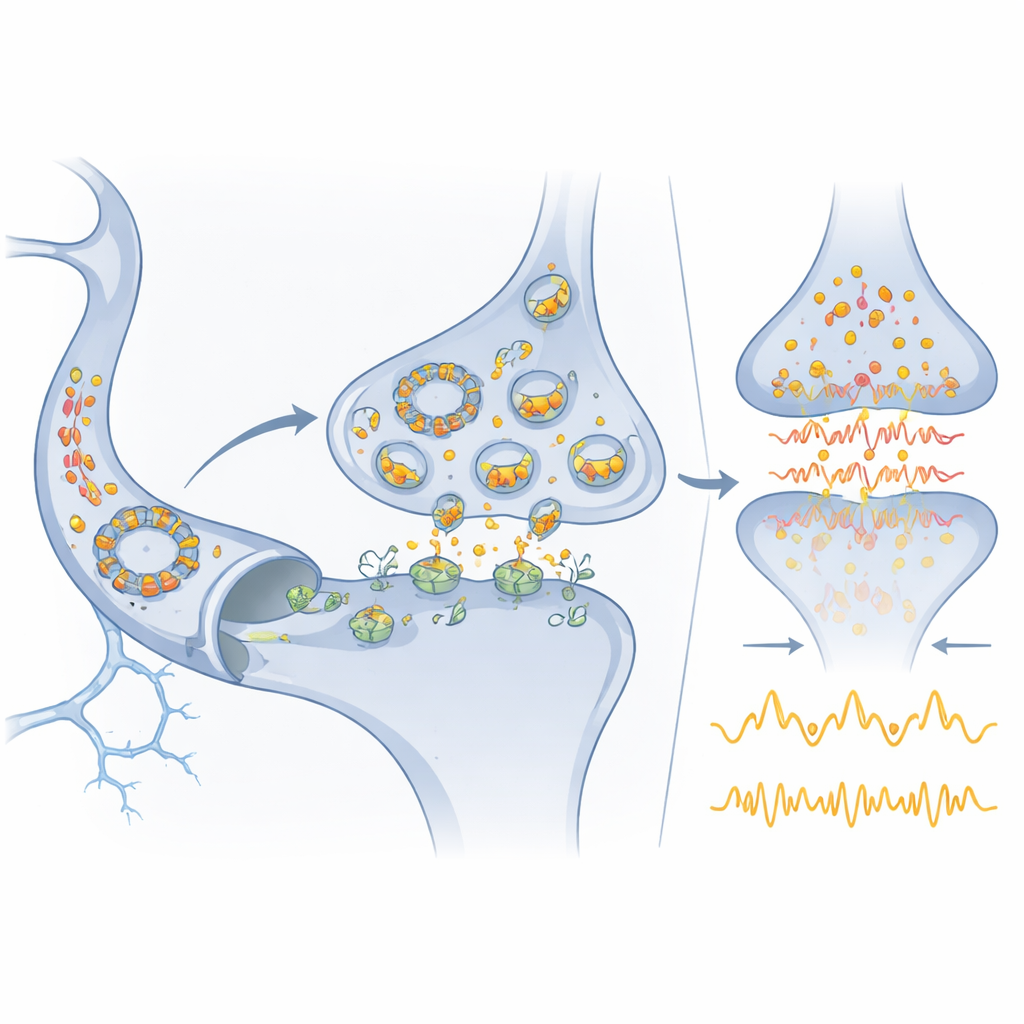
从分子回路走向医学应用
由于 Cdr1as 在大脑中高度富集且稳定性足以在血液中被检测到,它有望作为神经和精神疾病中大脑状态的便捷标志物。miR-7 已在各种体液中被检测到,可能同样有助于追踪或调节疾病过程。作者概述了未来可能针对 miR-7、Cdr1as 或 miR-671 的药物或基于 RNA 的疗法,如何在中风中抑制有害的谷氨酸激增,或在情绪与发育性疾病中重建异常放电的网络。与此同时,他们也警示,大多数被提出的环状 RNA 调控因子可能缺乏 Cdr1as 那样的极高丰度和结合能力。因此,该系统成为一个基准:它表明纯 RNA 回路在精确度和稳健性方面可以与蛋白网络抗衡,但真正作为强效调控者的环状 RNA 可能很罕见,必须通过严格、定量的测试来识别。
引用: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
关键词: 环状 RNA, microRNA-7, 神经元应激, 谷氨酸能信号传导, RNA 生物标志物