Clear Sky Science · ru
История и функция кольцевой РНК
Как крошечные РНК‑петли помогают мозгу справляться со стрессом
Когда мы лишены сна, получили травму или переживаем сильный эмоциональный стресс, клетки мозга вынуждены быстро перестраивать свою активность, чтобы выжить и сохранить работу сетей. В статье рассказывается об необычной молекуле в мозге — кольцевом фрагменте РНК под названием Cdr1as — и показано, как она взаимодействует с другими малыми РНК, чтобы тонко регулировать передачу между нервными клетками в условиях стресса. Понимание этой скрытой системы контроля может открыть новые пути лечения инсульта, депрессии и других заболеваний мозга — а также привести к созданию анализов крови, которые удалённо информировали бы о состоянии мозга.
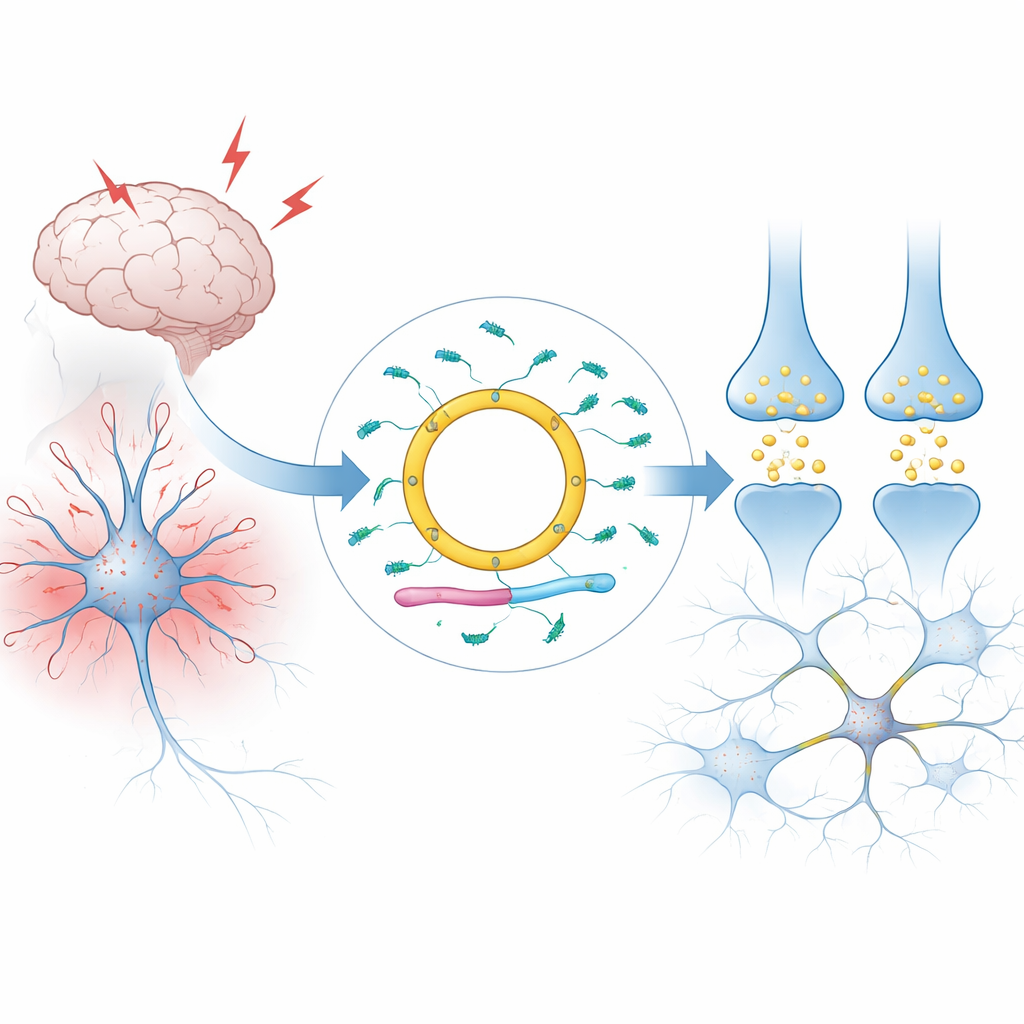
Кольцевое послание в нейронах
Большинство РНК в наших клетках линейны: у них два конца, и они быстро разрушаются. Cdr1as отличается: она образует замкнутую петлю, что делает её необычно стабильной и позволяет накапливаться в очень больших количествах в мозгах млекопитающих, особенно в определённых типах нейронов. Авторы объясняют, как Cdr1as образуется из более крупного РНК‑предшественника на X‑хромосоме в результате процесса, который сшивает её концы вместе. У человека и мыши практически вся РНК с этого локуса превращается в кольцевую форму, причём линейной версии остаётся почти ничтожно мало. Широкие исследования тканей и отдельных клеток показывают, что Cdr1as по сути является нейрон‑специфической молекулой: она редка в других органах и в вспомогательных клетках мозга, таких как глия.
Плотная сеть крошечных регуляторов
Значение Cdr1as объясняется её окружением. В её кольцевой последовательности содержится исключительное число сайтов связывания для небольшой регуляторной РНК, называемой miR‑7 — порядка семидесяти у человека и примерно 130 у мыши. miR‑7 принадлежит к знаменитому семейству микроРНК, недавно отмеченному Нобелевской премией; эти молекулы одновременно подавляют множество белок-кодирующих сообщений. В нейронах miR‑7 нацелена на транскрипты, участвующие в ответах на стресс и в высвобождении нейротрансмиттера глутамата. Cdr1as связывает miR‑7 в живой ткане мозга, влияя на продолжительность жизни miR‑7, её внутриклеточное распределение и силу воздействия на многочисленные мишени. Вторая малая РНК, miR‑671, может «рассекать» и уничтожать Cdr1as, тогда как длинная некодирующая РНК Cyrano стимулирует активный распад самой miR‑7. Вместе эти три некодирующие РНК и две микроРНК образуют тесно связанную цепочку регуляции.
Поддержание баланса нервной активности под давлением
Используя модели мышей с удалёнными составными частями этой цепочки, авторы суммируют десятилетие работ, показывающих, как она формирует функцию мозга. Удаление Cdr1as снижает уровни зрелой miR‑7 и нарушает экспрессию «немедленных ранних» генов, которые обычно реагируют на активность и стресс. Нейроны без Cdr1as работают более неустойчиво и избыточно возбудимы, а у мышей меняются реакции на сенсорные сигналы. Напротив, удаление Cyrano приводит к сильному накоплению miR‑7, что в свою очередь препятствует накоплению Cdr1as, выявляя петлю обратной связи. Эксперименты, имитирующие состояния, похожие на инсульт, в культурах нейронов и у живых мышей демонстрируют, что уровни Cdr1as, miR‑7 и Cyrano скоординированно изменяются во времени. Эти сдвиги влияют на высвобождение глутамата в синапсах, что сказывается на способности нейронов выживать и на восстановлении сетей после повреждения.
Эволюционное надстроение для тонкой настройки
Обзор также рассматривает эту цепочку в эволюционном контексте. miR‑7 древняя: она появилась с первыми животными, у которых развивались централизованные нервные системы, и глубоко консервативна, поскольку участвует в контроле ранних решений развития, например тех, которыми управляет главный регулятор PAX6. В то же время Cyrano возникла позже у позвоночных, miR‑671 — ещё позже у млекопитающих с плацентой, а Cdr1as встречается только у плацентарных млекопитающих. Авторы полагают, что эти более новые РНК постепенно наслоились на старую систему miR‑7, чтобы уточнить управление секрецией и реакциями на стресс в специализированных клетках мозга и гормонопродуцирующих клетках. Они предполагают, что Cdr1as может действовать как переносчик, доставляя miR‑7 в нервные окончания, где регулируются локальный синтез белка и высвобождение нейромедиатора.
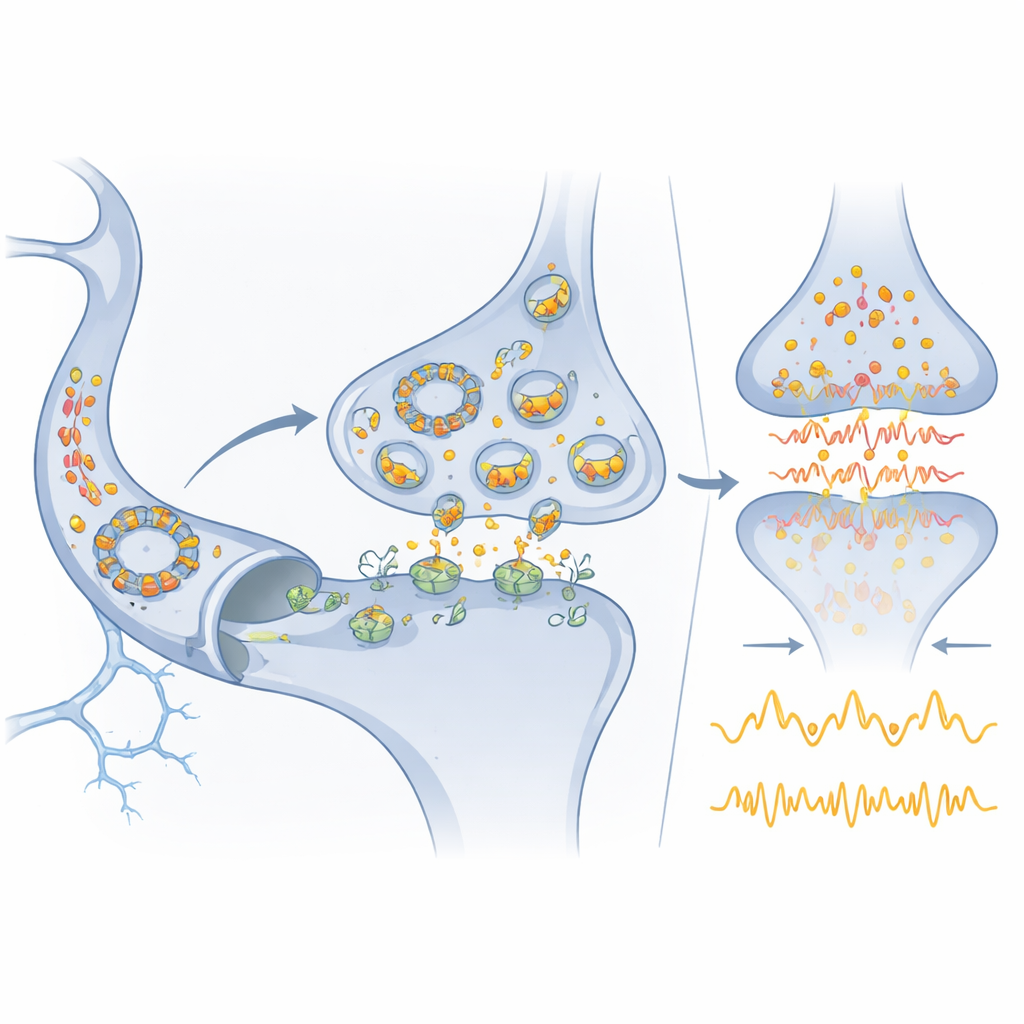
От молекулярной схемы к медицине
Поскольку Cdr1as настолько обогащена в мозге и при этом достаточно стабильна, чтобы её можно было обнаружить в крови, она может служить удобным маркером состояния мозга при неврологических и психиатрических заболеваниях. miR‑7, уже выявленная в различных биологических жидкостях, может аналогично помочь отслеживать или модифицировать болезненные процессы. Авторы описывают, как лекарства или РНК‑ориентированные терапии, нацеленные на miR‑7, Cdr1as или miR‑671, могли бы однажды ослаблять повреждающие всплески глутамата при инсульте или восстанавливать равновесие в неверно работающих сетях при расстройствах настроения и развитии. В то же время они предупреждают, что большинство предполагаемых регуляторных кольцевых РНК, вероятно, не обладают исключительной абундантностью и связывающей ёмкостью Cdr1as. В результате эта система становится эталоном: она демонстрирует, что РНК‑только цепочки регуляции могут соперничать с белковыми сетями по точности и надёжности, но также что истинные «тяжеловесы» среди кольцевых РНК, вероятно, редки и требуют строгой количественной проверки для их выявления.
Цитирование: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Ключевые слова: кольцевая РНК, microRNA-7, нейрональный стресс, глутаматергическая сигнализация, РНК‑биомаркеры