Clear Sky Science · de
Die Geschichte und Funktion einer zirkulären RNA
Wie winzige RNA‑Schleifen gestresste Gehirne beim Ausgleich helfen
Wenn wir schlaflos, verletzt oder emotional überfordert sind, müssen sich Gehirnzellen rasch anpassen, um zu überleben und die Schaltkreise funktionsfähig zu halten. Dieser Artikel beschreibt ein ungewöhnliches Molekül im Gehirn, ein kreisförmiges RNA‑Stück namens Cdr1as, und zeigt, wie es gemeinsam mit anderen kleinen RNAs die Kommunikation von Nervenzellen unter Stress fein abstimmt. Das Verständnis dieses verborgenen Kontrollsystems könnte neue Wege zur Behandlung von Schlaganfall, Depression und anderen Hirnerkrankungen eröffnen – und möglicherweise sogar Bluttests liefern, die aus der Ferne über den Zustand des Gehirns informieren.
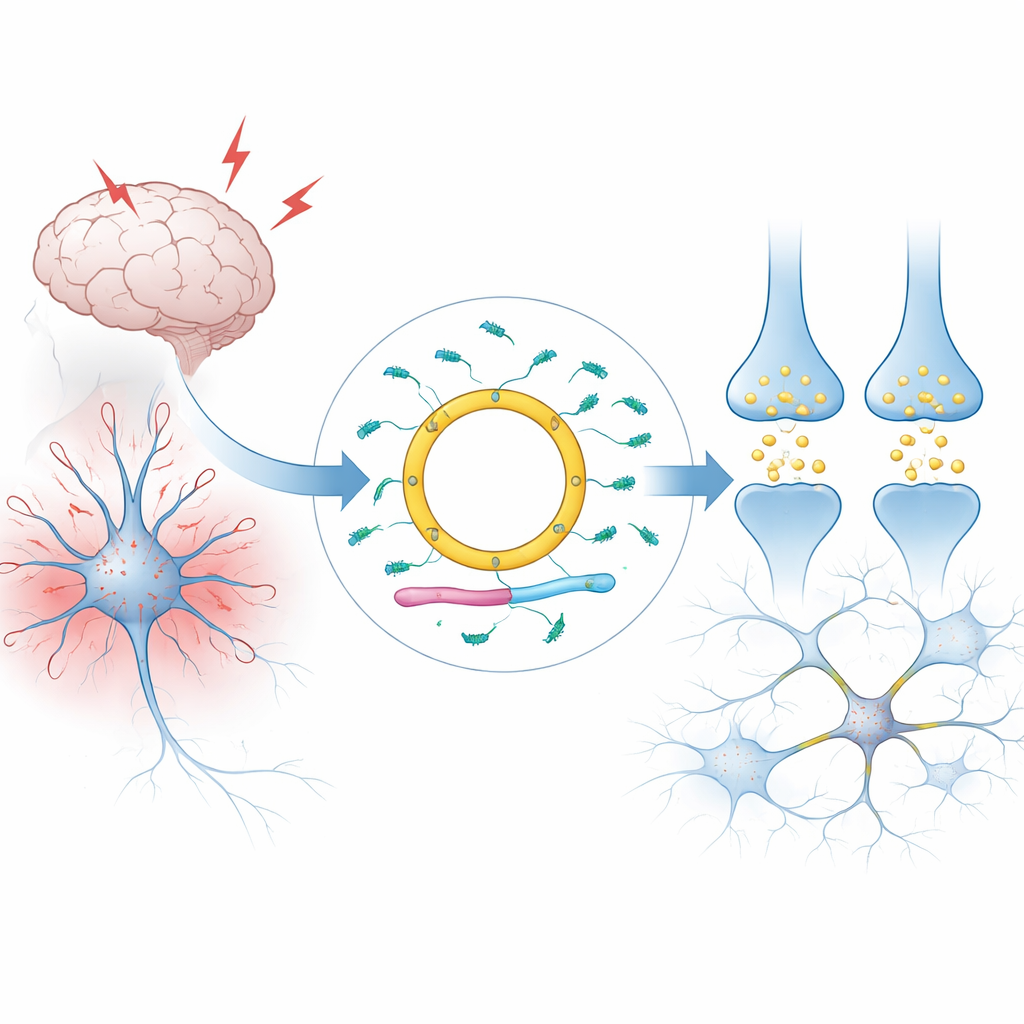
Eine kreisförmige Botschaft in Gehirnzellen
Die meisten RNAs in unseren Zellen sind linear: Sie haben zwei Enden und werden rasch abgebaut. Cdr1as ist anders. Es bildet eine geschlossene Schleife, wodurch es ungewöhnlich stabil ist und sich in Säugetiergehirnen in sehr hohen Mengen ansammeln kann, insbesondere in bestimmten Neuronentypen. Die Autoren erklären, wie Cdr1as aus einer größeren RNA‑Einheit auf dem X‑Chromosom entsteht, indem seine Enden miteinander verknüpft werden. Beim Menschen und bei Mäusen wird nahezu die gesamte RNA von diesem Lokus in die zirkuläre Form umgewandelt, während nur kaum eine lineare Version übrigbleibt. Umfangreiche Gewebe‑ und Einzelzellanalysen zeigen, dass Cdr1as praktisch ein neuronenspezifisches Molekül ist, das in anderen Organen und in unterstützenden Gehirnzellen wie Glia selten vorkommt.
Ein dichtes Netzwerk winziger Regulatoren
Cdr1as gewinnt seine Bedeutung durch die Moleküle, mit denen es zusammenarbeitet. Seine zirkuläre Sequenz trägt eine außergewöhnlich hohe Zahl an Andockstellen für eine kleine regulatorische RNA namens miR‑7 – etwa siebzig beim Menschen und rund 130 bei Mäusen. miR‑7 gehört zur bekannten Familie der microRNAs, jüngst mit einem Nobelpreis gewürdigter Moleküle, die viele proteinkodierende Botschaften gleichzeitig stilllegen. In Neuronen richtet sich miR‑7 gegen Botschaften, die an Stressreaktionen und an die Freisetzung des Neurotransmitters Glutamat beteiligt sind. Cdr1as bindet miR‑7 im lebenden Gehirngewebe und beeinflusst, wie lange miR‑7 überdauert, wo es innerhalb des Neurons lokalisiert ist und wie stark es auf seine vielen Ziele einwirken kann. Eine zweite kleine RNA, miR‑671, kann Cdr1as zerschneiden und zerstören, während eine lange RNA namens Cyrano den aktiven Abbau von miR‑7 selbst auslöst. Zusammen bilden diese drei nichtkodierenden RNAs und zwei microRNAs einen eng gekoppelten Regelkreis.
Aktivität der Nervenzellen unter Druck im Gleichgewicht halten
Mithilfe von Mausmodellen, denen einzelne Teile dieses Kreises fehlen, fassen die Autoren ein Jahrzehnt Forschung zusammen, das zeigt, wie dieser Kreis die Gehirnfunktion formt. Das Entfernen von Cdr1as reduziert die reifen miR‑7‑Spiegel und stört die Expression sogenannter „immediate early“-Gene, die normalerweise auf Aktivität und Stress reagieren. Neuronen ohne Cdr1as feuern unregelmäßiger und übererregbar, und Mäuse zeigen veränderte Reaktionen auf sensorische Reize. Im Gegensatz dazu führt das Entfernen von Cyrano zu einer starken Anhäufung von miR‑7, die wiederum die Ansammlung von Cdr1as verhindert – ein Hinweis auf eine Rückkopplungsschleife. Experimente, die schlaganfallähnliche Bedingungen in Zellkulturen und bei lebenden Mäusen nachahmen, zeigen, dass sich die Mengen von Cdr1as, miR‑7 und Cyrano koordiniert und zeitabhängig verändern. Diese Verschiebungen beeinflussen die Glutamatausschüttung an Synapsen und damit, wie gut Neuronen überleben und wie Netzwerke sich nach einer Verletzung erholen.
Eine evolutionäre Ergänzung zur feinen Steuerung
Die Übersichtsarbeit ordnet diesen Regelkreis auch in einen evolutionären Kontext ein. miR‑7 ist uralt, es tauchte mit den ersten Tieren auf, die zentrale Nervensysteme entwickelten, und ist tief konserviert, weil es frühe Entwicklungsentscheidungen mitsteuert, etwa solche, die vom Masterregulator PAX6 gesteuert werden. Im Gegensatz dazu entstand Cyrano später bei Wirbeltieren, miR‑671 noch später bei Säugetieren mit primitiven Plazenten, und Cdr1as nur bei plazentalen Säugetieren. Die Autoren argumentieren, dass diese neueren RNAs schrittweise auf das ältere miR‑7‑System aufgesetzt wurden, um zu verfeinern, wie Sekretion und Stressreaktionen in spezialisierten Gehirn‑ und Hormonsekretionszellen abgestimmt werden. Sie schlagen vor, dass Cdr1as als Transporteur wirken könnte, indem es miR‑7 in Nervenendigungen trägt, wo lokale Proteinsynthese und Neurotransmitterausschüttung kontrolliert werden.
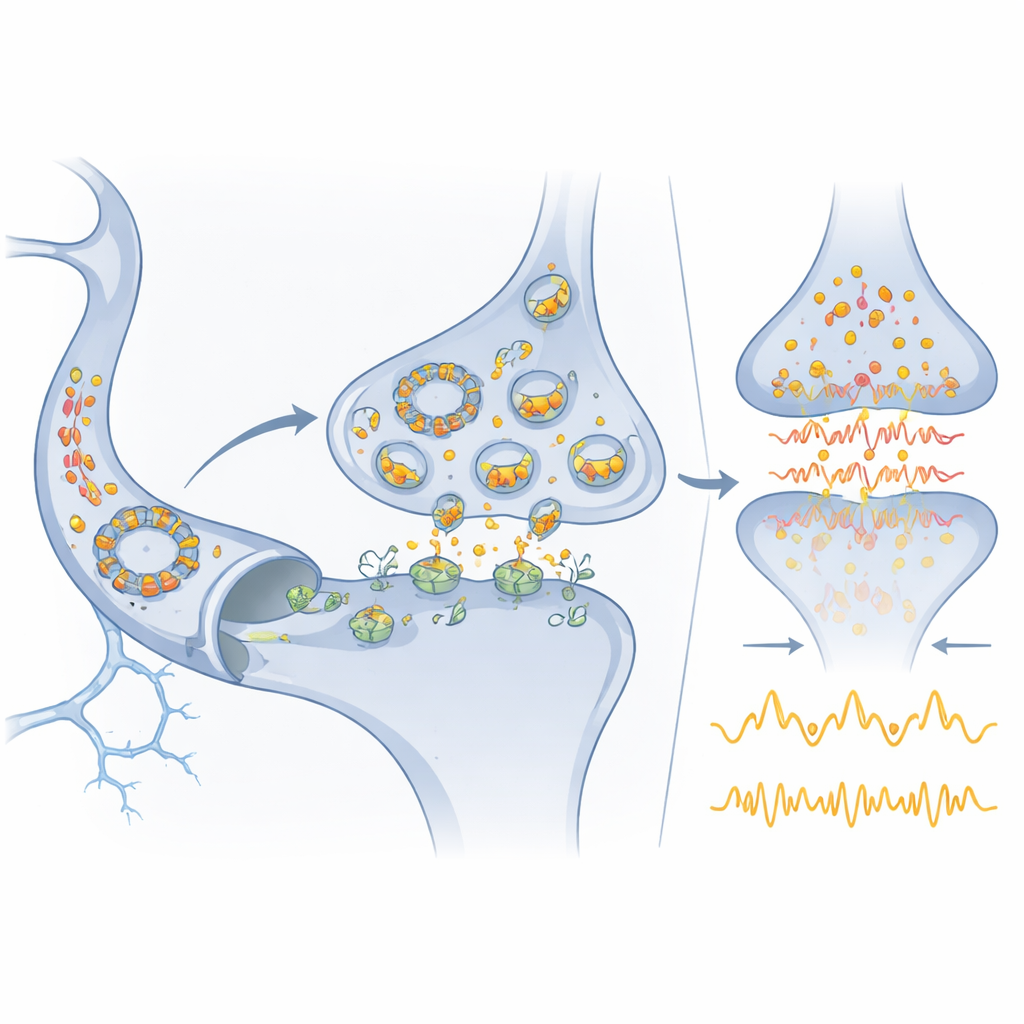
Vom molekularen Schaltkreis zur Medizin
Weil Cdr1as im Gehirn stark angereichert und zugleich stabil genug ist, um im Blut nachgewiesen zu werden, könnte es als praktischer Marker für den Zustand des Gehirns bei neurologischen und psychiatrischen Erkrankungen dienen. miR‑7, das bereits in verschiedenen Körperflüssigkeiten nachgewiesen wurde, könnte ebenfalls helfen, Krankheitsprozesse zu verfolgen oder zu beeinflussen. Die Autoren skizzieren, wie Medikamente oder RNA‑basierte Therapien, die auf miR‑7, Cdr1as oder miR‑671 abzielen, eines Tages schädliche Glutamat‑Exzesse bei Schlaganfällen dämpfen oder fehlregulierte Netzwerke bei Stimmungs‑ und Entwicklungsstörungen neu ausbalancieren könnten. Gleichzeitig warnen sie, dass die meisten vorgeschlagenen zirkulären RNA‑Regulatoren wahrscheinlich nicht die außergewöhnliche Häufigkeit und Bindungskapazität von Cdr1as besitzen. Dadurch wird dieses System zu einem Maßstab: Es zeigt, dass rein RNA‑basierte Schaltkreise mit Proteinnetzwerken in Präzision und Robustheit konkurrieren können, aber auch, dass echte regulatorische Schwergewichte unter den zirkulären RNAs vermutlich selten sind und mit strengen, quantitativen Tests identifiziert werden müssen.
Zitation: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Schlüsselwörter: zirkuläre RNA, microRNA-7, neuraler Stress, glutamaterges Signalwesen, RNA-Biomarker