Clear Sky Science · es
La historia y la función de un ARN circular
Cómo pequeños bucles de ARN ayudan al cerebro estresado a adaptarse
Cuando estamos privados de sueño, heridos o emocionalmente desbordados, las células cerebrales deben ajustar rápidamente su actividad para sobrevivir y mantener el funcionamiento de los circuitos. Este artículo describe una molécula inusual en el cerebro, un fragmento circular de ARN llamado Cdr1as, y muestra cómo actúa junto a otros ARN pequeños para afinar la comunicación neuronal bajo estrés. Comprender este sistema oculto de control podría abrir nuevas vías para tratar el ictus, la depresión y otros trastornos cerebrales, e incluso podría dar lugar a análisis sanguíneos que informen sobre la salud cerebral a distancia.
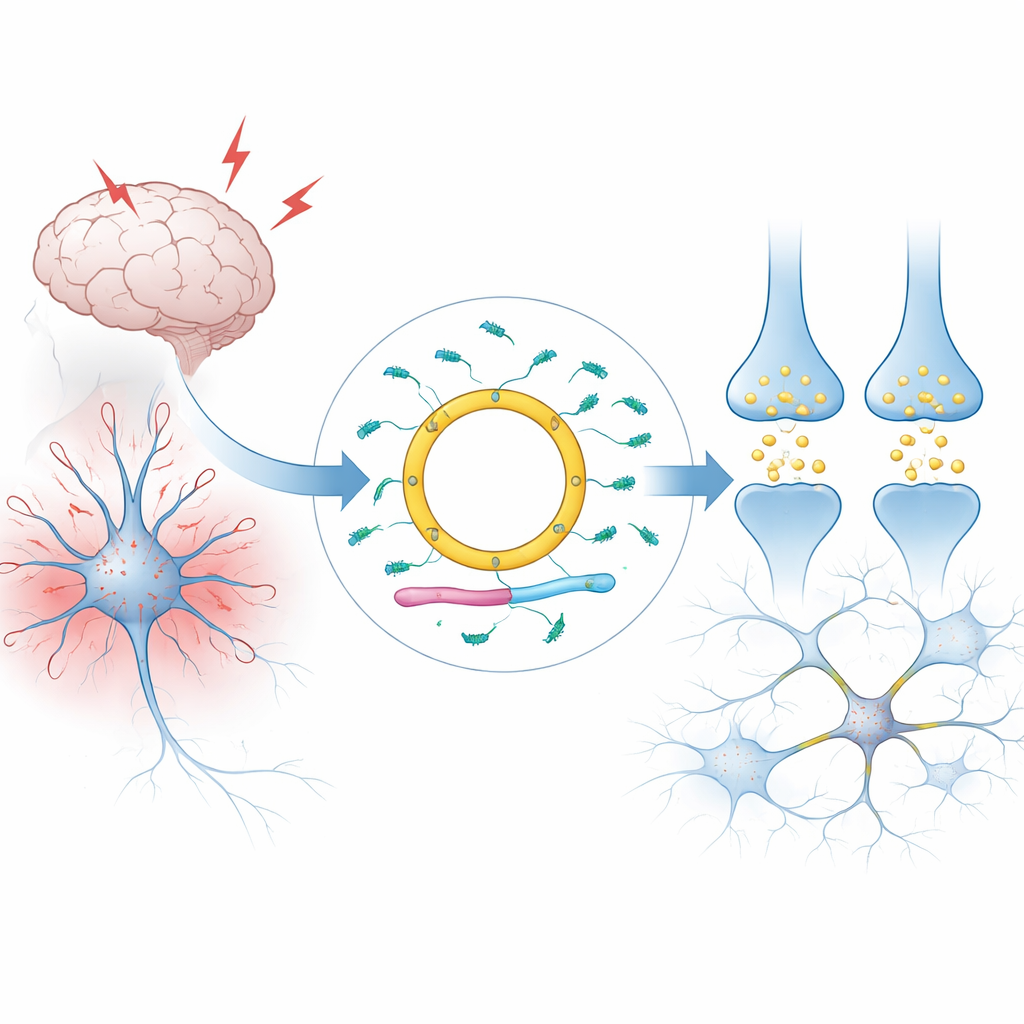
Un mensaje circular en las células cerebrales
La mayoría de los ARN en nuestras células son lineales: tienen dos extremos y se degradan rápidamente. Cdr1as es diferente. Forma un bucle cerrado, lo que lo hace inusualmente estable y le permite acumularse en niveles muy altos en cerebros de mamíferos, especialmente en tipos neuronales concretos. Los autores explican cómo Cdr1as se produce a partir de una unidad de ARN mayor en el cromosoma X mediante un proceso que empalma sus extremos. En humanos y ratones, casi todo el ARN de este locus se convierte en la forma circular, quedando apenas versión lineal residual. Amplios estudios de tejidos y de células individuales muestran que, a efectos prácticos, Cdr1as es una molécula específica de neuronas que escasea en otros órganos y en células de apoyo cerebral como la glía.
Una densa red de reguladores diminutos
Cdr1as adquiere importancia por la compañía que mantiene. Su secuencia circular porta un número excepcional de sitios de anclaje para un pequeño ARN regulador llamado miR-7—alrededor de setenta en humanos y unas 130 en ratones. miR-7 pertenece a la célebre familia de los microARN, moléculas recientemente reconocidas con el Nobel que silencian a muchos mensajes codificadores de proteínas a la vez. En neuronas, miR-7 tiene como dianas mensajes implicados en respuestas al estrés y en la liberación del neurotransmisor glutamato. Cdr1as se une a miR-7 en tejido cerebral vivo, afectando la duración de la vida de miR-7, su localización dentro de la neurona y la intensidad con la que puede actuar sobre sus múltiples dianas. Un segundo ARN pequeño, miR-671, puede cortar y destruir Cdr1as, mientras que un ARN largo llamado Cyrano provoca la degradación activa del propio miR-7. En conjunto, estos tres ARN no codificantes y los dos microARN forman un circuito estrechamente conectado.
Mantener el equilibrio de la actividad neuronal bajo presión
Utilizando modelos de ratón que carecen de piezas individuales de este circuito, los autores resumen una década de trabajo que muestra cómo moldea la función cerebral. Eliminar Cdr1as reduce los niveles de miR-7 maduro y altera la expresión de genes “inmediatos tempranos” que normalmente responden a la actividad y al estrés. Las neuronas sin Cdr1as disparan de forma más errática y excesivamente excitable, y los ratones muestran reacciones alteradas a señales sensoriales. Por el contrario, eliminar Cyrano conduce a una fuerte acumulación de miR-7 que, a su vez, impide que Cdr1as se acumule, revelando un bucle de retroalimentación. Experimentos que imitan condiciones similares a un ictus en cultivos neuronales y en ratones vivos demuestran que los niveles de Cdr1as, miR-7 y Cyrano cambian de manera coordinada y dependiente del tiempo. Estos cambios modifican la liberación de glutamato en las sinapsis, influyendo en la supervivencia neuronal y en la capacidad de recuperación de las redes tras una lesión.
Un añadido evolutivo para un control fino
La revisión sitúa también este circuito en un contexto evolutivo. miR-7 es antiguo, apareció con los primeros animales que desarrollaron sistemas nerviosos centralizados, y está profundamente conservado porque ayuda a controlar decisiones tempranas del desarrollo, como las guiadas por el regulador maestro PAX6. En contraste, Cyrano surgió más tarde en los vertebrados, miR-671 aún después en mamíferos con placentas primitivas, y Cdr1as sólo en mamíferos placentarios. Los autores sostienen que estos ARN más recientes se fueron superponiendo gradualmente al sistema antiguo de miR-7 para refinar cómo se regulan la secreción y las respuestas al estrés en células especializadas del cerebro y en células secretoras de hormonas. Proponen que Cdr1as puede actuar como un transportador, llevando miR-7 hasta las terminaciones nerviosas donde se controla la síntesis proteica local y la liberación de neurotransmisores.
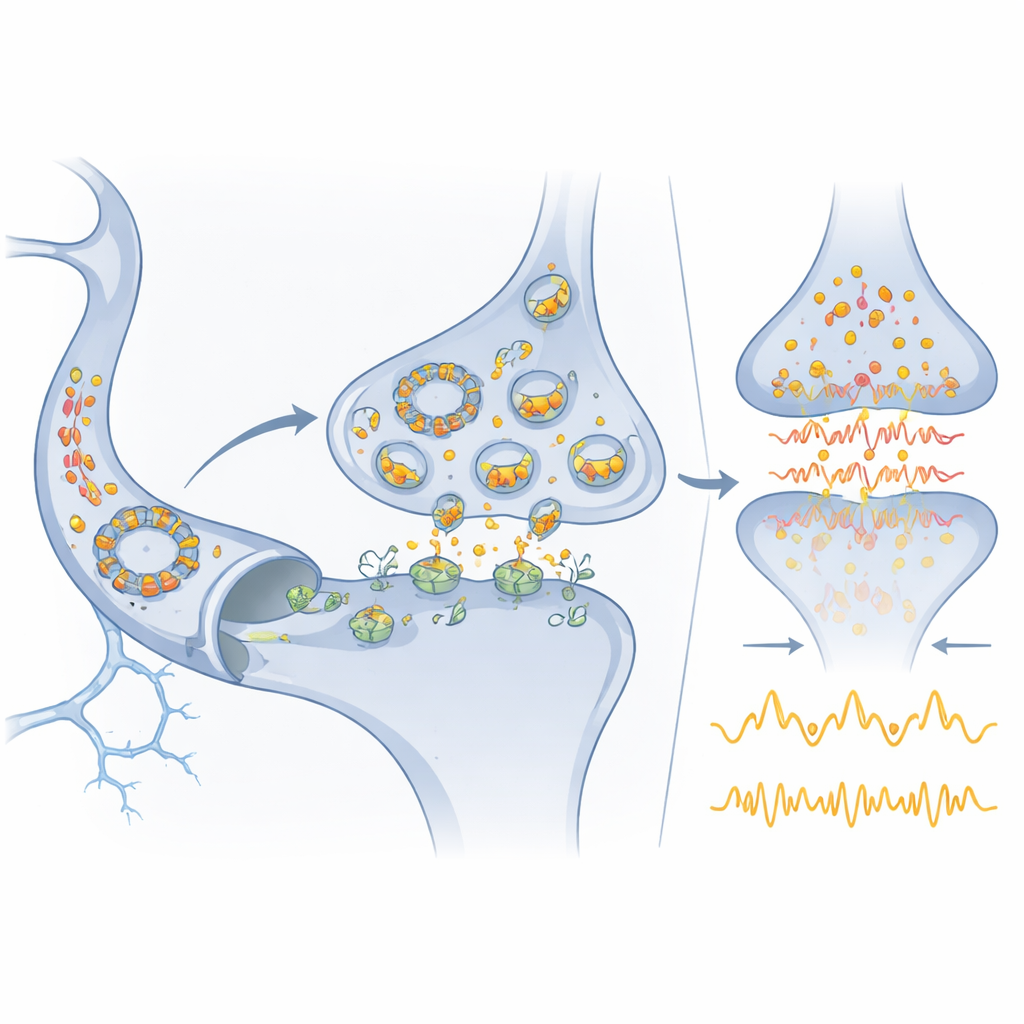
Del circuito molecular a la medicina
Debido a que Cdr1as está tan enriquecido en el cerebro y, al mismo tiempo, es lo bastante estable como para detectarse en sangre, podría servir como un marcador conveniente del estado cerebral en enfermedades neurológicas y psiquiátricas. miR-7, ya detectado en diversos fluidos corporales, podría igualmente ayudar a rastrear o modificar procesos patológicos. Los autores describen cómo fármacos o terapias basadas en ARN dirigidas a miR-7, Cdr1as o miR-671 podrían algún día mitigar picos dañinos de glutamato en el ictus o reequilibrar redes que funcionan mal en trastornos del estado de ánimo y del desarrollo. Al mismo tiempo, advierten que la mayoría de los supuestos reguladores por ARN circular probablemente carecen de la abundancia y capacidad de unión excepcionales de Cdr1as. En consecuencia, este sistema se convierte en un punto de referencia: demuestra que los circuitos formados solo por ARN pueden rivalizar con las redes proteicas en precisión y robustez, pero también que los verdaderos pesos pesados regulatorios entre los ARN circulares probablemente son raros y deben identificarse con pruebas rigurosas y cuantitativas.
Cita: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Palabras clave: ARN circular, microARN-7, estrés neuronal, señalización glutamatérgica, biomarcadores de ARN