Clear Sky Science · sv
Historien och funktionen hos ett cirkulärt RNA
Hur små RNA‑slingor hjälper stressade hjärnor att klara sig
När vi är sömnbristiga, skadade eller känslomässigt överväldigade måste hjärnceller snabbt anpassa sin aktivitet för att överleva och hålla kretsar fungerande. Denna artikel beskriver en ovanlig molekyl i hjärnan, en cirkulär bit RNA kallad Cdr1as, och förklarar hur den samverkar med andra små RNA för att finjustera nervcellers kommunikation under stress. Att förstå detta dolda kontrollsystem kan öppna nya vägar för behandling av stroke, depression och andra hjärnsjukdomar — och kan till och med leda till blodprov som på distans rapporterar om hjärnans hälsa.
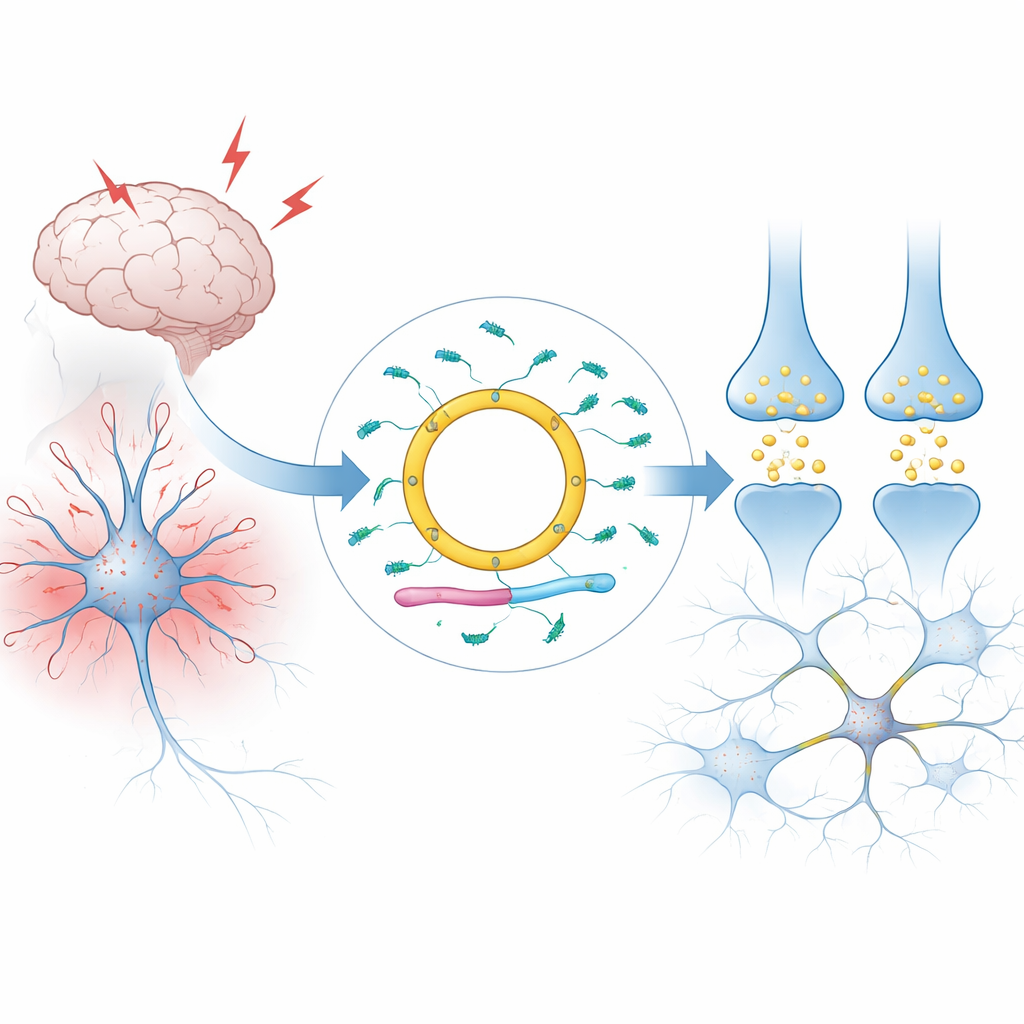
Ett cirkulärt budskap i hjärnceller
De flesta RNA i våra celler är linjära: de har två ändar och bryts snabbt ner. Cdr1as är annorlunda. Den bildar en sluten ring, vilket gör den ovanligt stabil och tillåter den att ackumuleras till mycket höga nivåer i däggdjurshjärnor, särskilt i specifika nervcellstyper. Författarna förklarar hur Cdr1as bildas från en större RNA‑enhet på X‑kromosomen genom en process som sammanfogar dess ändar. Hos människor och möss omvandlas nästan allt RNA från denna locus till den cirkulära formen, med knappt någon kvarvarande linjär version. Stora studier av vävnader och enskilda celler visar att Cdr1as, för praktiska syften, är en neuron‑specifik molekyl som är sällsynt i andra organ och i stödjeceller i hjärnan såsom gliaceller.
Ett tätt nätverk av små regulatorer
Cdr1as får sin betydelse av de molekyler den finns tillsammans med. Dess cirkulära sekvens bär ett exceptionellt antal fästanordningar för ett litet reglerande RNA kallat miR‑7 — ungefär sjuttio hos människor och cirka 130 hos möss. miR‑7 tillhör den välkända familjen microRNA, nyligen Nobel‑erkända molekyler som tystar många protein‑kodande budskap samtidigt. I neuroner riktar sig miR‑7 mot budskap involverade i stressresponser och frisättning av transmittorn glutamat. Cdr1as binder miR‑7 i levande hjärnvävnad, vilket påverkar hur länge miR‑7 överlever, var det är lokaliserat inne i neuronen och hur starkt det kan påverka sina många mål. Ett annat litet RNA, miR‑671, kan skära itu och förstöra Cdr1as, medan ett långt RNA kallat Cyrano orsakar aktiv nedbrytning av miR‑7 själv. Tillsammans bildar dessa tre icke‑kodande RNA och två microRNA en tätt kopplad krets.
Hålla nervaktiviteten i balans under påfrestning
Genom att använda musmodeller som saknar individuella delar av denna krets sammanfattar författarna ett decennium av arbete som visar hur den formar hjärnfunktionen. Borttagning av Cdr1as minskar nivåerna av moget miR‑7 och rubbar uttrycket av ”immediate early”‑gener som normalt svarar på aktivitet och stress. Neuroner utan Cdr1as avfyrar mer oregelbundet och överdrivet exciterat, och möss visar förändrade reaktioner på sensoriska signaler. I kontrast leder borttagning av Cyrano till en kraftig uppbyggnad av miR‑7, vilket i sin tur förhindrar att Cdr1as ackumuleras, och avslöjar en negativ återkopplingsslinga. Experiment som efterliknar stroke‑lika förhållanden i cellodlingsrätter med neuroner och i levande möss visar att nivåerna av Cdr1as, miR‑7 och Cyrano skiftar på ett koordinerat, tidsberoende sätt. Dessa förändringar påverkar glutamatfrisättning vid synapser och därigenom hur väl neuroner överlever och hur nätverk återhämtar sig efter skada.
En evolutionär tillägg för finreglering
Översikten placerar också denna krets i ett evolutionärt sammanhang. miR‑7 är gammalt, det uppträdde med de första djur som utvecklade centraliserade nervsystem och är djupt bevarat eftersom det hjälper till att styra tidiga utvecklingsbeslut, exempelvis de som styrs av huvudregulatorn PAX6. Däremot uppstod Cyrano senare hos ryggsträngsdjur, miR‑671 ännu senare hos däggdjur med mer utvecklade moderkakor, och Cdr1as först hos moderkakslevande däggdjur. Författarna menar att dessa nyare RNA gradvis lagts på det äldre miR‑7‑systemet för att förfina hur utsöndring och stressresponser ställs in i specialiserade hjärn‑ och hormonproducerande celler. De föreslår att Cdr1as kan fungera som en transportör, som för miR‑7 in i nervändarna där lokal proteinsyntes och transmittorfrisättning styrs.
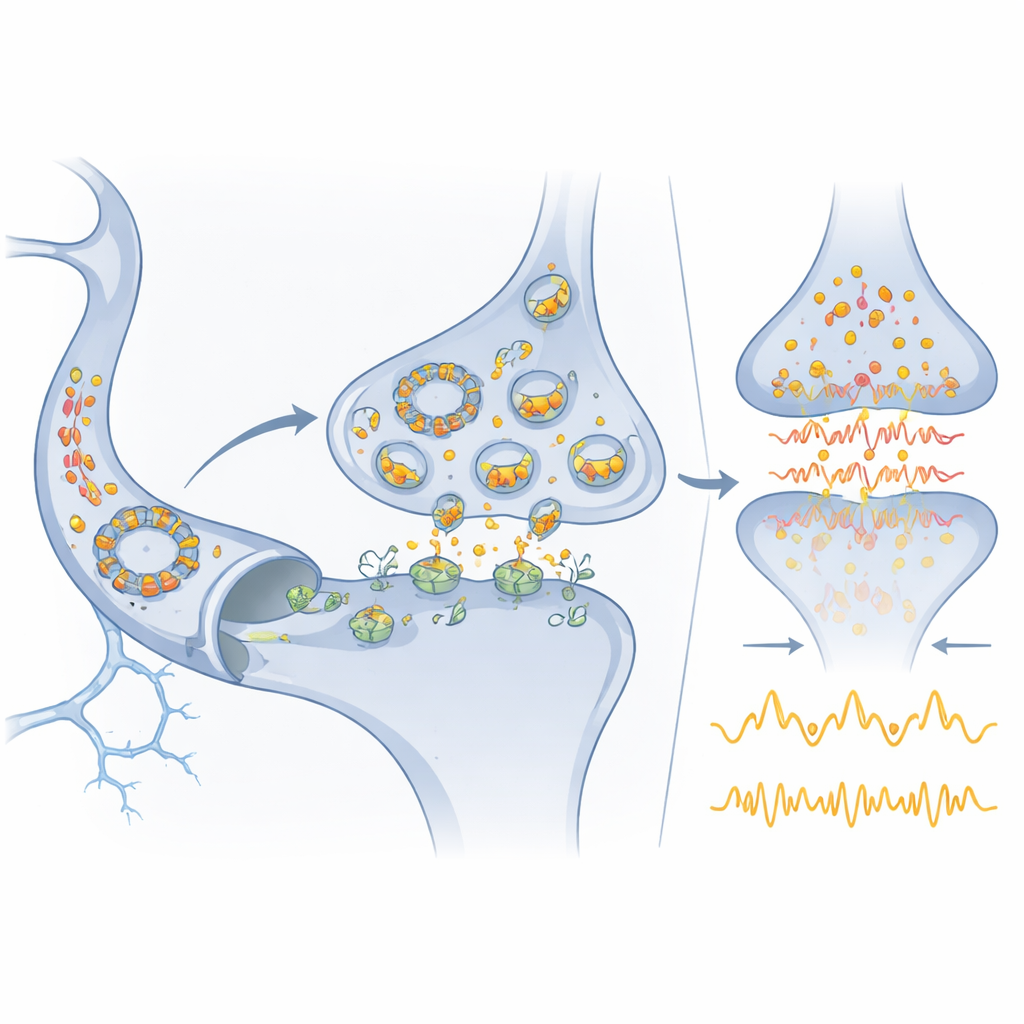
Från molekylär krets till medicin
Eftersom Cdr1as är så hjärnberikat men tillräckligt stabilt för att detekteras i blod, kan det fungera som en praktisk markör för hjärnans tillstånd vid neurologiska och psykiatriska sjukdomar. miR‑7, som redan påträffats i olika kroppsvätskor, kan på liknande sätt hjälpa till att spåra eller påverka sjukdomsprocesser. Författarna skisserar hur läkemedel eller RNA‑baserade terapier riktade mot miR‑7, Cdr1as eller miR‑671 en dag skulle kunna dämpa skadliga glutamatsurgar vid stroke eller återställa balans i felaktigt fungerande nätverk vid humör‑ och utvecklingsstörningar. Samtidigt varnar de för att de flesta föreslagna cirkulära RNA‑regulatorer sannolikt saknar Cdr1as exceptionella överflöd och bindningskapacitet. Som en följd blir detta system en referenspunkt: det visar att enbart RNA‑kretsar kan mäta sig med proteinnätverk i precision och robusthet, men också att verkliga tungviktare bland cirkulära RNA förmodligen är sällsynta och måste identifieras med rigorösa, kvantitativa tester.
Citering: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Nyckelord: cirkulärt RNA, microRNA-7, neuronal stress, glutamatergisk signalering, RNA-biomarkörer