Clear Sky Science · nl
De geschiedenis en functie van een circulair RNA
Hoe kleine RNA-lussen gestreste hersenen helpen zich aan te passen
Als we slaapgebrek hebben, gewond raken of emotioneel overbelast zijn, moeten hersencellen hun activiteit snel aanpassen om te overleven en netwerken te laten functioneren. Dit artikel beschrijft een ongewone molecule in de hersenen, een circulair stukje RNA dat Cdr1as wordt genoemd, en laat zien hoe het samenwerkt met andere kleine RNA’s om de communicatie tussen zenuwcellen onder stress fijn af te stellen. Inzicht in dit verborgen regelsysteem kan nieuwe wegen openen voor de behandeling van beroerte, depressie en andere hersenaandoeningen — en mogelijk zelfs bloedtesten opleveren die op afstand informatie geven over de gezondheid van de hersenen.
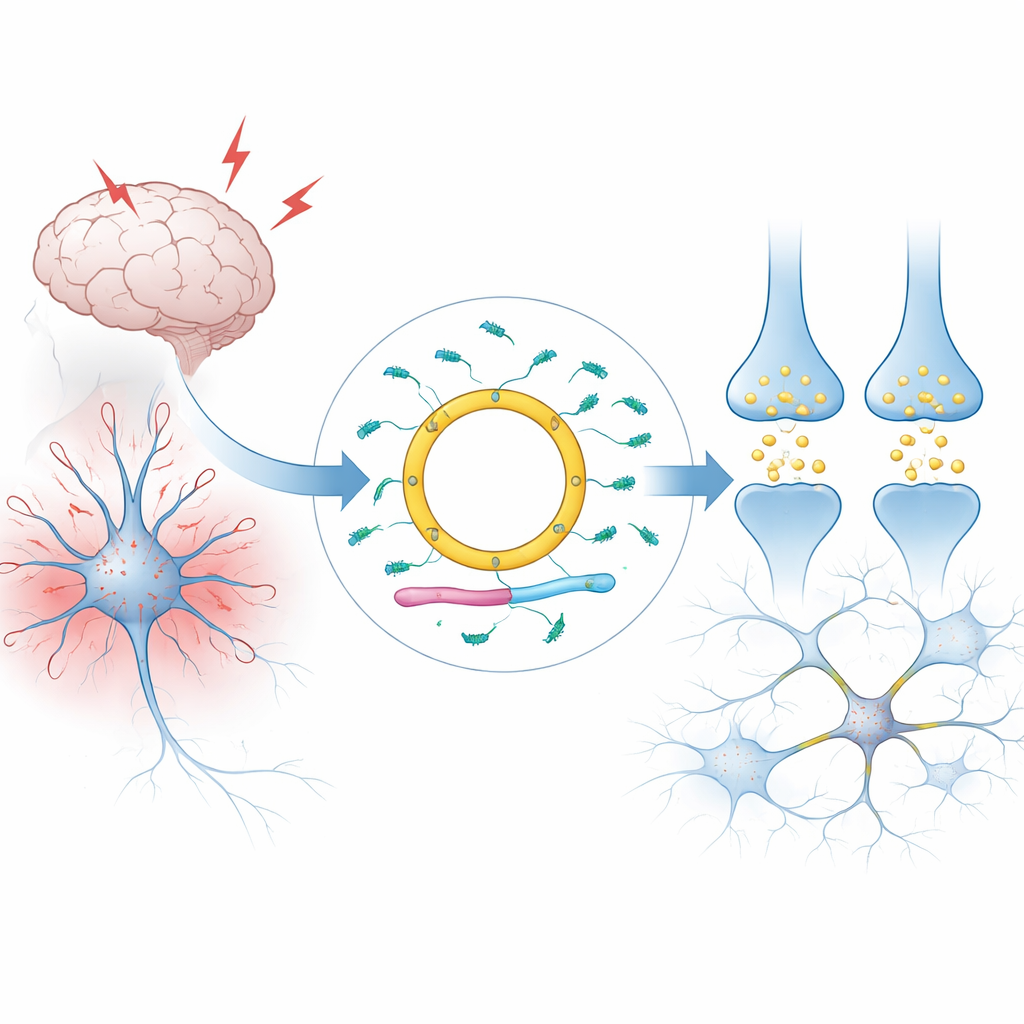
Een circulaire boodschap in hersencellen
De meeste RNA’s in onze cellen zijn lineair: ze hebben twee uiteinden en worden snel afgebroken. Cdr1as is anders. Het vormt een gesloten lus, waardoor het uitzonderlijk stabiel is en zich in zoogdierenhersenen in zeer hoge concentraties kan ophopen, vooral in specifieke typen neuronen. De auteurs leggen uit hoe Cdr1as wordt geproduceerd uit een groter RNA-stuk op het X-chromosoom door een proces dat de uiteinden aan elkaar splice. Bij mensen en muizen wordt bijna al het RNA van deze locus omgezet in de circulaire vorm, met nauwelijks enige lineaire restvorm. Grote onderzoeken van weefsels en individuele cellen tonen aan dat Cdr1as, in praktische zin, een neuron-specifieke molecule is die schaars is in andere organen en in ondersteunende hersencellen zoals gliacellen.
Een dicht web van kleine regulatoren
Cdr1as ontleent zijn belang aan de partners waarmee het optreedt. Zijn circulaire sequentie draagt een uitzonderlijk aantal aanhechtingsplaatsen voor een klein regulerend RNA genaamd miR-7 — ongeveer zeventig in mensen en rond de 130 in muizen. miR-7 behoort tot de befaamde familie van microRNA’s, recentelijk met een Nobelprijs erkende moleculen die vele coderende boodschappen tegelijk onderdrukken. In neuronen richt miR-7 zich op boodschappers die betrokken zijn bij stressreacties en de afgifte van de signaalstof glutamaat. Cdr1as bindt miR-7 in levend hersenweefsel, wat van invloed is op hoe lang miR-7 overleeft, waar het zich binnen het neuron bevindt en hoe sterk het op zijn vele doelwitten kan inwerken. Een tweede klein RNA, miR-671, kan Cdr1as doorsnijden en vernietigen, terwijl een lang RNA genaamd Cyrano de actieve afbraak van miR-7 zelf veroorzaakt. Samen vormen deze drie niet-coderende RNA’s en twee microRNA’s een nauw verbonden circuit.
Het in balans houden van zenuwactiviteit onder druk
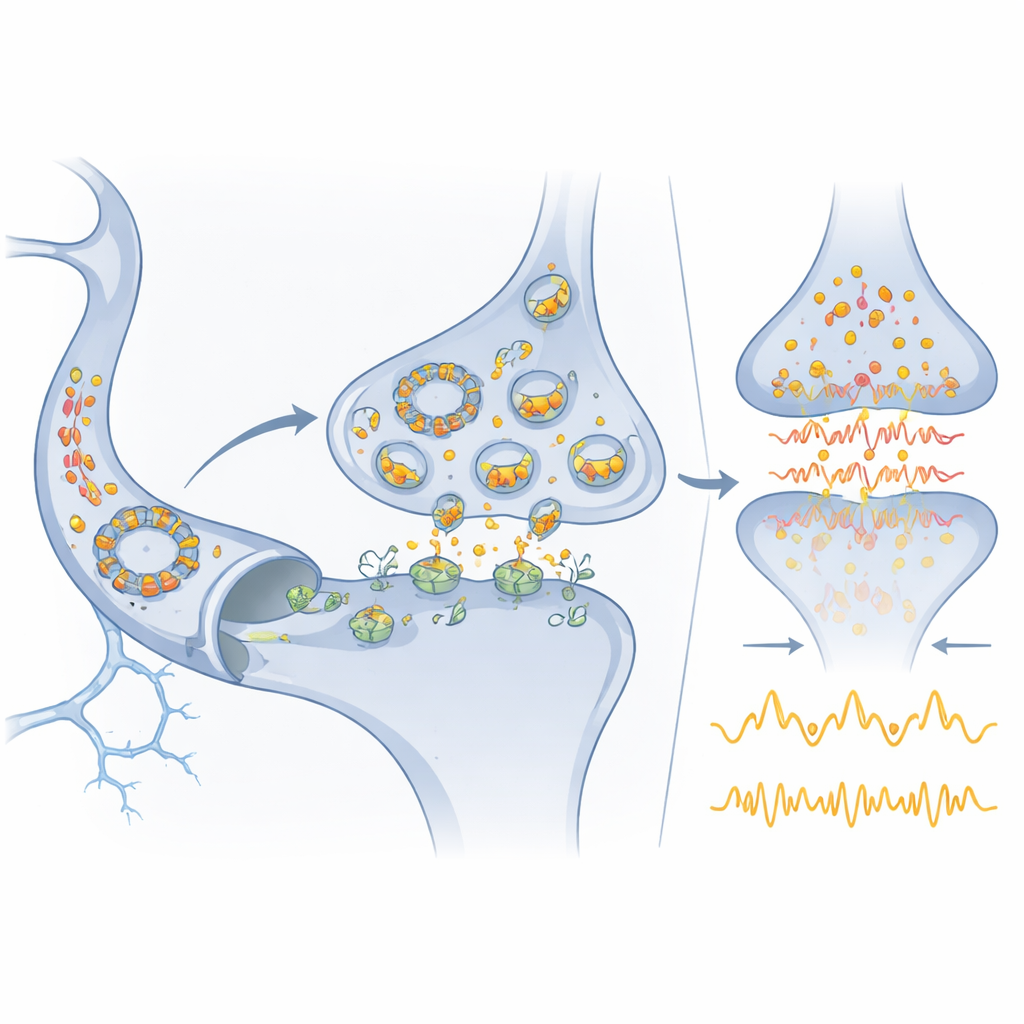
Met behulp van muismodellen die afzonderlijke onderdelen van dit circuit missen, vatten de auteurs een decennium van werk samen dat laat zien hoe het de hersenfunctie vormgeeft. Het verwijderen van Cdr1as verlaagt niveaus van rijp miR-7 en verstoort de expressie van “immediate early”-genen die normaal reageren op activiteit en stress. Neuronen zonder Cdr1as vuren op een meer grillige, overprikkelbare manier, en muizen tonen veranderde reacties op zintuiglijke prikkels. Daarentegen leidt verwijdering van Cyrano tot een sterke ophoping van miR-7, wat op zijn beurt hindert dat Cdr1as zich ophoopt, wat een terugkoppelingslus onthult. Proeven die beroerteachtige omstandigheden nabootsen in kweekjes van neuronen en in levende muizen tonen aan dat de niveaus van Cdr1as, miR-7 en Cyrano op gecoördineerde, tijdsafhankelijke wijze verschuiven. Deze verschuivingen veranderen de glutamaatafgifte aan synapsen, wat beïnvloedt hoe goed neuronen overleven en hoe netwerken herstellen na letsel.
Een evolutionaire aanvulling voor fijne controle
De review plaatst dit circuit ook in evolutionaire context. miR-7 is oud, het verscheen bij de eerste dieren met gecentraliseerde zenuwstelsels, en is diep geconserveerd omdat het helpt vroege ontwikkelingsbeslissingen te regelen, zoals die worden gestuurd door de meesterregelaar PAX6. Daartegenover ontstond Cyrano later bij gewervelden, miR-671 nog later bij zoogdieren met primitieve placenta’s, en Cdr1as alleen bij placentale zoogdieren. De auteurs betogen dat deze nieuwere RNA’s geleidelijk op het oudere miR-7-systeem werden aangebracht om te verfijnen hoe secretie en stressreacties worden afgestemd in gespecialiseerde hersen- en hormoonafscheidende cellen. Zij stellen voor dat Cdr1as mogelijk fungeert als een transporter, die miR-7 naar zenuwuiteinden brengt waar lokale eiwitsynthese en neurotransmitterafgifte worden geregeld.
Van moleculair circuit naar geneeskunde
Omdat Cdr1as zo hersenrijk is en toch stabiel genoeg om in bloed te worden gedetecteerd, zou het kunnen dienen als een handig merkteken van de hersentoestand bij neurologische en psychiatrische aandoeningen. miR-7, dat al in verschillende lichaamsvloeistoffen is aangetroffen, kan op vergelijkbare wijze helpen bij het volgen of beïnvloeden van ziekteprocessen. De auteurs schetsen hoe geneesmiddelen of RNA-gebaseerde therapieën gericht op miR-7, Cdr1as of miR-671 op den duur schadelijke glutamaatpieken bij beroerte zouden kunnen dempen of ontregelde netwerken in stemmings- en ontwikkelingsstoornissen zouden kunnen herstellen. Tegelijk waarschuwen zij dat de meeste voorgestelde circulaire RNA-regulatoren waarschijnlijk niet de uitzonderlijke overvloed en bindingscapaciteit van Cdr1as hebben. Als gevolg daarvan wordt dit systeem een maatstaf: het laat zien dat uitsluitend RNA-circuits kunnen wedijveren met eiwitnetwerken in precisie en robuustheid, maar ook dat echte zware regulatoren onder circulaire RNA’s waarschijnlijk zeldzaam zijn en met rigoureuze, kwantitatieve tests moeten worden geïdentificeerd.
Bronvermelding: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Trefwoorden: circulair RNA, microRNA-7, neurale stress, glutamatergische signalering, RNA-biomarkers